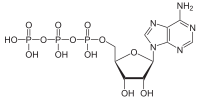
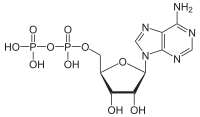
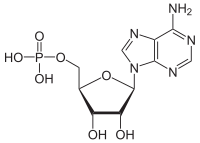
АТФазы ( EC 3.6.1.3, Аденозин -5'- Трифосфатаза , аденилпирофосфатаза, АТФ-монофосфатаза, трифосфатаза, Т-антиген SV40, АТФ-гидролаза, комплекс V (митохондриальный транспорт электронов), ( Ca 2+ + Mg 2+ ) -АТФаза, НСО 3 - -АТФаза, аденозинтрифосфатаза) — класс ферментов , катализирующих распад АТФ на АДФ и свободный фосфат-ион [1] [2] [3] [4] [5] [ 6 ] или обратная реакция. Эта реакция дефосфорилирования высвобождает энергию , которую фермент (в большинстве случаев) использует для запуска других химических реакций , которые в противном случае не произошли бы. Этот процесс широко используется во всех известных формах жизни .
Некоторые такие ферменты представляют собой интегральные мембранные белки (закрепленные внутри биологических мембран ) и перемещают растворенные вещества через мембрану, обычно против градиента их концентрации. Их называют трансмембранными АТФазами.

Трансмембранные АТФазы импортируют метаболиты, необходимые для клеточного метаболизма , и экспортируют токсины, отходы и растворенные вещества, которые могут препятствовать клеточным процессам. Важным примером является натриево-калиевый насос (Na + /K + АТФаза), поддерживающий потенциал клеточной мембраны . Другим примером является водородно-калиевая АТФаза (H + /K + АТФаза или желудочный протонный насос), которая подкисляет содержимое желудка. АТФаза генетически консервативна у животных; следовательно, карденолиды , которые представляют собой токсичные стероиды, вырабатываемые растениями и действующими на АТФазы, образуют общие и эффективные токсины для животных, действующие в зависимости от дозы. [7]
Помимо обменников, другие категории трансмембранных АТФаз включают котранспортеры и насосы (однако некоторые обменники также являются насосами). Некоторые из них, например Na + /K + АТФаза, вызывают чистый поток заряда, а другие — нет. Их называют электрогенными транспортерами и электронейтральными транспортерами соответственно. [8]
«Связанная с мембраной медь-транспортирующая аденозинтрифосфатаза (Cu-АТФаза), которая избирательно связывает ионы меди, транспортирует ионы меди в клетки и из них (Harris et al. 1998)». Источник: https://www.atsdr.cdc.gov/ToxProfiles/tp132.pdf с. 73
Мотивы Уокера представляют собой характерный мотив белковой последовательности для связывания и гидролиза нуклеотидов. Помимо этой широкой функции, мотивы Уокера можно обнаружить почти во всех природных АТФазах, за заметным исключением тирозинкиназ . [9] Мотивы Уокера обычно образуют бета-лист -поворот- альфа-спираль , которая самоорганизуется как гнездо (структурный мотив белка) . Считается, что это связано с тем, что современные АТФазы произошли от небольших NTP-связывающих пептидов, которые должны были самоорганизоваться. [10]
Дизайн белка позволил воспроизвести функцию АТФазы (слабо) без использования природных последовательностей или структур АТФазы. Важно отметить, что хотя все природные АТФазы имеют некоторую структуру бета-листа, разработанная «Альтернативная АТФаза» не имеет структуры бета-листа, что демонстрирует, что эта жизненно важная функция возможна с последовательностями и структурами, не встречающимися в природе. [11]
АТФаза (также называемая F 0 F 1 -АТФ-синтаза) представляет собой комплекс переноса заряда, который катализирует АТФ для осуществления синтеза АТФ путем перемещения ионов через мембрану. [12]
Сочетание гидролиза и транспорта АТФ представляет собой химическую реакцию, в которой на каждую гидролизованную молекулу АТФ переносится фиксированное количество молекул растворенного вещества; для Na + /K + -обменника это три иона Na + вне клетки и два иона K+ внутри на одну гидролизованную молекулу АТФ.
Трансмембранные АТФазы используют химическую потенциальную энергию АТФ, совершая механическую работу: они транспортируют растворенные вещества в направлении, противоположном их термодинамически предпочтительному направлению движения, то есть со стороны мембраны с низкой концентрацией на сторону с высокой концентрацией. Этот процесс называется активным транспортом .
Например, ингибирование везикулярных H + -АТФаз приведет к повышению pH внутри везикул и снижению pH цитоплазмы.
Все АТФазы имеют общую базовую структуру. Каждая ротационная АТФаза состоит из двух основных компонентов: F 0 /A 0 /V 0 и F 1 /A 1 /V 1 . Их соединяют 1-3 стебля для сохранения устойчивости, контроля вращения и предотвращения вращения в другую сторону. Один рычаг используется для передачи крутящего момента. [13] Количество периферических стеблей зависит от типа АТФазы: у F-АТФазы — одна, у А-АТФазы — две, а у V-АТФазы — три. Каталитический домен F 1 расположен на N-стороне мембраны и участвует в синтезе и деградации АТФ, а также участвует в окислительном фосфорилировании . Трансмембранный домен F 0 участвует в перемещении ионов через мембрану. [12]
Бактериальная F 0 F 1 -АТФаза состоит из растворимого домена F 1 и трансмембранного домена F 0 , который состоит из нескольких субъединиц с различной стехиометрией. Есть две субъединицы, γ и ε, которые образуют центральный стебель и связаны с F 0 . F 0 содержит олигомер c-субъединицы в форме кольца (c-кольца). Субъединица α близка к субъединице b 2 и составляет ножку, соединяющую трансмембранные субъединицы с субъединицами α3β3 и δ. F-АТФ-синтазы идентичны по внешнему виду и функциям, за исключением митохондриальной F 0 F 1 -АТФ-синтазы, которая содержит 7-9 дополнительных субъединиц. [12]
Электрохимический потенциал — это то, что заставляет c-кольцо вращаться по часовой стрелке для синтеза АТФ. Это приводит к изменению формы центрального стебля и каталитического домена. Вращение c-кольца вызывает образование трех молекул АТФ, что затем заставляет H + перемещаться с P-стороны мембраны на N-сторону мембраны. Вращение c-кольца против часовой стрелки обусловлено гидролизом АТФ, и ионы перемещаются со стороны N на сторону P, что способствует созданию электрохимического потенциала. [12]
АТФ- синтаза митохондрий и хлоропластов представляет собой анаболический фермент, который использует энергию трансмембранного протонного градиента в качестве источника энергии для добавления неорганической фосфатной группы к молекуле аденозиндифосфата (АДФ) с образованием молекулы аденозинтрифосфата (АТФ).
Этот фермент работает, когда протон движется вниз по градиенту концентрации, придавая ферменту вращательное движение. Это уникальное вращательное движение связывает АДФ и Р вместе, образуя АТФ.
АТФ-синтаза может также функционировать в обратном направлении, то есть использовать энергию, выделяемую при гидролизе АТФ, для перекачки протонов против их электрохимического градиента.
Существуют разные типы АТФаз, которые могут различаться по функциям (синтез и/или гидролиз АТФ), структуре (F-, V- и А-АТФазы содержат вращательные двигатели) и типу ионов, которые они транспортируют.
P-АТФазы (иногда известные как АТФазы E1-E2) обнаружены у бактерий, а также в плазматических мембранах и органеллах эукариот. Его название связано с кратковременным присоединением неорганического фосфата к остаткам аспартата во время активации. Функция P-АТФазы заключается в транспортировке различных соединений, таких как ионы и фосфолипиды, через мембрану с использованием гидролиза АТФ для получения энергии. Существует много разных классов Р-АТФаз, которые транспортируют ионы определенного типа. Р-АТФазы могут состоять из одного или двух полипептидов и обычно могут иметь две основные конформации: Е1 и Е2.