AICD (клеточная смерть, вызванная активацией) — это запрограммированная клеточная смерть , вызванная взаимодействием рецепторов Fas (Fas, CD95) и лигандов Fas (FasL, лиганд CD95). [1] AICD — это отрицательный регулятор активированных Т-лимфоцитов , который возникает в результате повторной стимуляции их Т-клеточных рецепторов (TCR) и помогает поддерживать периферическую иммунную толерантность . [2] Изменение этого процесса может привести к аутоиммунным заболеваниям . [1]
Эффекторная клетка AICD — это та, которая экспрессирует FasL, и апоптоз индуцируется в клетке, экспрессирующей рецептор Fas. Как активированные Т-клетки, так и В-клетки экспрессируют Fas и подвергаются клональной делеции с помощью механизма AICD. [3] [4] Активированные Т-клетки, которые экспрессируют как Fas, так и FasL, могут быть убиты сами по себе или друг другом. [1]
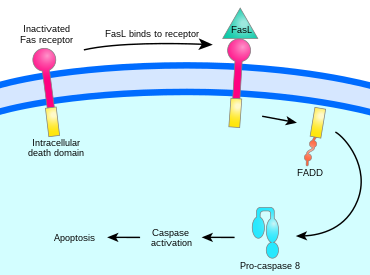
Связывание лиганда Fas с рецептором Fas запускает тримеризацию Fas, цитоплазматический домен которого затем способен связывать домен смерти адаптерного белка FADD (Fas-ассоциированный белок с доменом смерти). Прокаспаза 8 связывается с эффекторным доменом смерти FADD (DED) и протеолитически самоактивируется как каспаза 8. Fas, FADD и прокаспаза 8 вместе образуют сигнальный комплекс, индуцирующий смерть (DISC). Активированная каспаза 8 высвобождается в цитозоль, где она активирует каскад каспазы , который инициирует апоптоз. [5] [1]
FasL в первую очередь регулируется на уровне транскрипции. (Другой вариант — регуляция сигнала, исходящего от самого рецептора смерти , контролирующего чувствительность к индукции апоптоза.) [3] NFAT , активированный стимуляцией TCR, активирует транскрипцию FasL, возможно, косвенно, путем повышения регуляции ранних белков ответа роста . [1] Транскрипция FasL , вызванная активацией Т-клеток, далее регулируется гетеродимерами c-Myc – MAX и может быть заблокирована снижением регуляции c-Myc. [1] Факторы регуляции интерферона IRF1 и IRF2 также повышают регуляцию транскрипции FasL, напрямую связываясь с промотором FasL . [1]
Не так много известно о регуляции Fas и других рецепторов смерти. Однако, повышенная экспрессия белка CFLAR (каспаза и FADD-подобный регулятор апоптоза) ингибирует Fas-опосредованный апоптоз. [6]