Реакция Воля -Циглера [1] [2]
представляет собой химическую реакцию , включающую аллильное или бензильное бромирование углеводородов с использованием N -бромсукцинимида и радикального инициатора . [3]

Наилучшие выходы достигаются при использовании N -бромсукцинимида в растворителе четыреххлористом углероде . Опубликовано несколько обзоров. [4] [5]
В типичной установке к раствору субстрата в CCl 4 добавляют стехиометрическое количество раствора N -бромсукцинимида и небольшое количество инициатора , реакционную смесь перемешивают и нагревают до температуры кипения. На начало реакции указывает более бурное кипение; иногда может потребоваться удаление источника тепла. Как только весь N -бромсукцинимид (который более плотен, чем растворитель) превращается в сукцинимид (который всплывает сверху), реакция завершается. Из-за высокой токсичности и озоноразрушающей природы четыреххлористого углерода трифтортолуол был предложен в качестве альтернативного растворителя, подходящего для бромирования Воль-Циглера. [6]
Соответствующую реакцию хлорирования обычно невозможно осуществить с помощью N- хлорсукцинимида [7] , хотя были разработаны более специализированные реагенты [8] , и реакцию можно осуществить в промышленных масштабах с использованием газообразного хлора. [9]
Механизм
Механизм, по которому протекает реакция Воля-Циглера, был предложен Полом Голдфингером в 1953 году, и его механизм реакции представляет собой один из двух предполагаемых путей, по которым происходит алифатическое, аллильное и бензильное бромирование N -бромсукцинимидом (NBS). [10] Было показано, что механизм Голдфингера является подходящим механизмом в отличие от ранее принятого механизма, предложенного Джорджем Блумфилдом, который, хотя и был последовательным в ходе исследований селективности, оказался чрезмерно упрощенным. [10]
Генерация радикалов NBS, описанная в механизме Блумфилда, оказалась гораздо более сложной, чем предполагалось, когда она была предложена, поэтому на протяжении многих лет она не удалась как правильная модель; однако данные свидетельствуют о том, что механизм Блумфилда все еще приемлем для окисления спиртов с использованием NBS. [10] В механизме Голдфингера целью NBS является просто поддержание очень низкой концентрации молекулярного брома, тогда как в механизме Блумфилда его целью является генерация исходного радикала, используемого в реакции, [11] который снова может быть довольно трудным процессом. [12] Это связано с тем, что поведение радикала NBS требует особого рассмотрения; единственный способ, которым он может функционировать, как это предложено в механизме Блумфилда, - это если энергия диссоциации связи N-Br в NBS меньше, чем у Br 2 , и было замечено много свидетельств, предполагающих противоположное поведение. [12] [13] Предложенный Голдфингером механизм не требует каких-либо особых соображений, поскольку все радикальные виды ведут себя нормально, и отчасти из-за этого его механизм считается правильным. [12]
 [10]
[10]
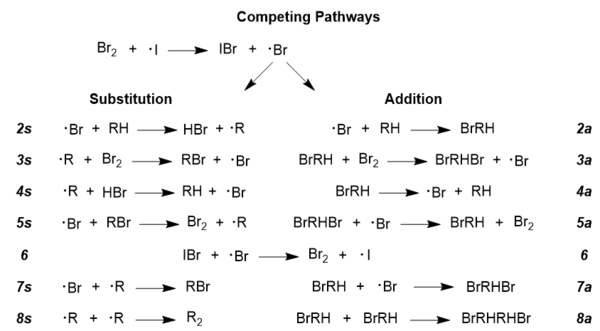
Для дальнейшего изучения принятого механизма реакции необходимо понимать, что в любой радикальной реакции существуют конкурирующие радикальные пути; в данном случае то же самое, поскольку пути присоединения и замещения конкурируют. [14] Для получения желаемого бромированного продукта необходимо, чтобы путь замещения был доминирующим, и условиями реакции действительно можно манипулировать, чтобы продвинуть этот путь по сравнению с менее желательным путем присоединения. [13] Ниже показаны оба пути в полном объеме; для полноты картины на этот рисунок включены побочные реакции, такие как этапы 6 и 8; эти пути являются общими почти для всех радикальных реакций, поэтому NBS здесь не показан, но его роль будет обсуждаться ниже.
 [13]
[13]- Роль NBS в механизме Голдфингера заключается в содействии регенерации молекулярного брома, [10] но одним из дополнительных преимуществ использования NBS является то, что он поддерживает низкую концентрацию молекулярного брома, что является ключом к стимулированию замещения вместо присоединения. [13] Были разработаны законы скорости, описывающие конкурентное поведение этой реакции, и они показывают сильную зависимость от концентрации молекулярного брома; Ниже приведены два уравнения: одно для высоких концентраций брома и одно для низких концентраций брома. [13]
- Высокие концентрации брома: r(a/s) = k 2a /k 2s (1 + k 4a /k 3a [Br 2 ]), где r(a/s) — отношение присоединения к замещению, а значения k соответствуют константы, описывающие конкретные этапы реакции, изображенные выше в разделе «Конкурирующие пути». [13]
- Низкие концентрации брома: r(a/s) = k 2a k 3a [Br 2 ]/k 2s k 4a , где члены имеют то же определение, что и в предыдущем уравнении. [13] Можно видеть, что в уравнении для низких концентраций брома соотношение добавления и замещения прямо пропорционально концентрации молекулярного брома, поэтому снижение концентрации брома будет ингибировать путь присоединения и способствовать большей степени бромирования продукта. формирование. [13]
Смотрите также
Рекомендации
- ^ Альфред Воль (1919). «Бромирование с N-бром-ацетамидом, ein Beitrag zur Lehre vom Verlauf chemischer Vorgänge». Берихте дер немецкое химическое общество . 52 : 51–63. дои : 10.1002/cber.19190520109.
- ^ Циглер, К. , Г. Шенк, Э.В. Кроков, А. Зиберт, А. Венц, Х. Вебер (1942). «Синтез кантаридинов». «Анналы химии» Юстуса Либиха . 551 : 1–79. дои : 10.1002/jlac.19425510102.
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Гринвуд, Флорида; Келлерт, доктор медицины; Седлак, Дж. (1963). «4-Бром-2-гептен». Органические синтезы; Сборник томов , т. 4, с. 108.
- ^ К. Джерасси (1948). «Бромирование N-бромсукцинимидом и родственными соединениями. Реакция Воля – Циглера». хим. Откр. 43 (2): 271–317. дои : 10.1021/cr60135a004. ПМИД 18887958.
- ^ Хорнер, Л; Винкельман, Э.М. (1959). «Neuere Methoden der Präparative Organischen Chemie II 14. N-Бромсукцинимид, Eigenschaften und Reaktionsweisen Studien zum Ablauf der Substitution XV». Энджью. хим. 71 (11): 349. Бибкод : 1959AngCh..71..349H. дои : 10.1002/ange.19590711102.
- ^ Суарес, Диана; Лаваль, Жиль; Ту, Шан-Мин; Цзян, Донг; Робинсон, Клэр Л.; Скотт, Ричард; Голдинг, Бернард Т. (июнь 2009 г.). «Бензилброминирование N-бромсукцинимидом в (трифторметил)бензоле». Синтез . 2009 (11): 1807–1810. дои : 10.1055/s-0029-1216793. ISSN 1437-210Х.
- ^ Джерасси, Карл. (01.10.1948). «Бромирование N-бромсукцинимидом и родственными соединениями. Реакция Воля-Циглера». Химические обзоры . 43 (2): 271–317. дои : 10.1021/cr60135a004. ISSN 0009-2665. ПМИД 18887958.
- ^ Тейлакер, Уолтер; Вессель, Хайнц (1967). «Олефинреакция, I. Хлорирование в аллил-Стеллунге». Юстус Либигс Annalen der Chemie (на немецком языке). 703 (1): 34–36. дои : 10.1002/jlac.19677030105. ISSN 1099-0690.
- ^ Крелинг, Людгер; Крей, Юрген; Якобсон, Джеральд; Гролиг, Иоганн; Микше, Леопольд (2000), «Аллиловые соединения», Энциклопедия промышленной химии Ульмана , Американское онкологическое общество, doi : 10.1002/14356007.a01_425, ISBN 9783527306732
- ^ abcde Инкремона, Дж. Х.; Мартин, Джей Си (1970). «N-Бромсукцинимид. Механизмы аллильного бромирования и родственные реакции». Варенье. хим. Соц . 92 (3): 627–634. дои : 10.1021/ja00706a034.
- ^ Блумфилд, GF (1944). «Каучук, полиизопрены и родственные соединения. Часть VI. Механизм реакций галогензамещения и аддитивное галогенирование каучука и дигидромирцена». Варенье. хим. Соц. : 114–120. дои : 10.1039/JR9440000114.
- ^ abc Нонхебель, округ Колумбия; Уолтон, Дж. К. (1974). Свободнорадикальная химия: структура и механизм . Лондон: Издательство Кембриджского университета. стр. 191–193. ISBN 978-0521201490.
- ^ abcdefgh Адам, Дж.; Госслен, Пенсильвания; Голдфингер, П. (1953). «Законы присоединения и замещения в атомных реакциях галогенов». Природа . 171 (4355): 704–705. Бибкод : 1953Natur.171..704A. дои : 10.1038/171704b0. S2CID 4285312.
- ^ Нойман, RC (1992). Органическая химия . Онлайн: Роберт К. Нойман-младший.
 [13]
[13]