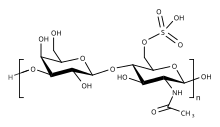
Кератансульфат ( KS ), также называемый кератосульфатом , представляет собой один из нескольких сульфатированных гликозаминогликанов (структурных углеводов), которые обнаружены особенно в роговице , хрящах и костях . Он также синтезируется в центральной нервной системе , где участвует как в развитии [1] , так и в формировании глиального рубца после травмы. [2] Кератансульфаты представляют собой крупные, сильно гидратированные молекулы, которые в суставах могут выступать в качестве подушки, поглощающей механические удары .
Как и другие гликозаминогликаны, кератансульфат представляет собой линейный полимер , состоящий из повторяющихся дисахаридных звеньев. Кератансульфат представляет собой протеогликан (PG), в котором цепи KS прикреплены к белкам клеточной поверхности или внеклеточного матрикса , называемым коровыми белками. Коровые белки KS включают люмикан , кератокан , мимекан , фибромодулин , PRELP , остеоадгерин и аггрекан .
Основной повторяющейся дисахаридной единицей в составе кератансульфата является -3 Gal β1-4 GlcNAc6S β1-. Он может быть сульфатирован по положению углерода 6 (C6) одного или обоих моносахаридов Gal или GlcNAc . Однако детальную первичную структуру конкретных типов КС лучше всего рассматривать как состоящую из трех областей: [3]
Моносахарид манноза находится в области связи кератансульфата типа I (KSI). Дисахариды в повторяющейся области KSII могут быть фукозилированы , а N-ацетилнейраминовая кислота блокирует концы всех цепей кератансульфата типа II (KSII) и до 70% цепей типа KSI. [4]
Обозначения KSI и KSII первоначально были присвоены в зависимости от типа ткани, из которой был выделен кератансульфат. KSI выделяли из ткани роговицы , а KSII — из скелетной ткани. [5] [6] Незначительные различия в составе моносахаридов существуют между KS, извлеченным из обоих источников, и даже между KS, извлеченным из одного и того же источника. Однако основные различия происходят в том, как каждый тип KS соединяется со своим основным белком. [7] Обозначения KSI и KSII теперь основаны на этих различиях в белковых связях. KSI N - связан со специфическими аминокислотами аспарагина через N -ацетилглюкозамин , а KSII O -связан со специфическими аминокислотами серина или треонина через N -ацетилгалактозамин . [8] Тканевой классификации СК больше не существует, поскольку было показано, что типы СК не являются тканеспецифичными. [4] Третий тип KS (KSIII) также был выделен из ткани головного мозга , которая O -связана со специфическими аминокислотами серином или треонином через маннозу . [9]
Количество КС в роговице в 10 раз выше, чем в хряще и в 2-4 раза выше, чем в других тканях. [10] Он вырабатывается кератоцитами роговицы [11] и, как полагают, играет роль динамического буфера гидратации роговицы. При редком прогрессирующем заболевании, называемом макулярной дистрофией роговицы (MCDC), синтез кератансульфата либо отсутствует (MCDC типа I), либо нарушен (MCDC типа II). [12]
Остеоадгерин , фибромодулин и PRELP — это основные белки костей и хрящей, модифицированные N-связанными KS-цепями. Цепи KS, связанные с остеоадгерином и фибромодулином, короче, чем цепи, обнаруженные в роговице, обычно составляют 8-9 дисахаридных единиц в длину. [13] Тогда как KSI роговицы состоит из ряда доменов с различной степенью сульфатации, самый длинный из которых может иметь длину 8-32 дисахаридных единицы. Невосстанавливающий конец фибромодулина KS по структуре больше похож на невосстанавливающий конец кератансульфата типа KSII, чем на роговичный KSI. Таким образом, считается, что структура KS определяется тканеспецифичной доступностью гликозилтрансфераз , а не типом связи с коровым белком. [4]
Хрящ KSII почти полностью сульфатирован и состоит из дисульфатированных мономеров , иногда прерываемых одним моносульфатированным мономером лактозамина . [8] Фукозилирование также часто встречается при наличии альфа-связанной фукозы в положении углерода 3 сульфатированного GlcNAc , за исключением случая трахеального KSII, где эта особенность отсутствует.