Легочная микробиота представляет собой легочное микробное сообщество, состоящее из сложного разнообразия микроорганизмов , обнаруженных в нижних дыхательных путях , особенно на слизистом слое и на эпителиальных поверхностях. К этим микроорганизмам относятся бактерии , грибы , вирусы и бактериофаги . Бактериальная часть микробиоты изучена более тщательно. Состоит из ядра из девяти родов : Prevotella , Sphingomonas , Pseudomonas , Acinetobacter , Fusobacterium , Megasphaera , Veillonella , Staphylococcus и Streptococcus . [1] [2] [3] Это аэробы, а также анаэробы и аэротолерантные бактерии. Микробные сообщества весьма разнообразны у отдельных особей и состоят примерно из 140 различных семейств. Например, бронхиальное дерево содержит в среднем 2000 бактериальных геномов на см 2 поверхности. Вредные или потенциально вредные бактерии также регулярно выявляются в образцах дыхательных путей. Наиболее значимыми являются Moraxella cataralis , Haemophilus influenzae и Streptococcus pneumoniae . Известно, что они вызывают респираторные нарушения при определенных условиях, а именно при нарушении иммунной системы человека. Механизм, посредством которого они сохраняются в нижних дыхательных путях у здоровых людей, неизвестен.
Роды грибов, которые обычно встречаются, составляют микобиом легких , в микробиоте легких, и включают Candida , Malassezia , Neosartorya , Saccharomyces и Aspergillus , среди других. [4] [5]
Эпителий дыхательных путей вместе с альвеолярными макрофагами и дендритными клетками играют важную роль в первичном распознавании продуктов бактерий, попадающих в нижние дыхательные пути с воздухом. Поскольку некоторые из этих продуктов являются мощными провоспалительными раздражителями, для иммунной системы чрезвычайно важно различать патогены и непатогенные комменсалы. Это предотвращает развитие постоянного воспаления и формирует толерантность к безвредной микробиоте. [6]
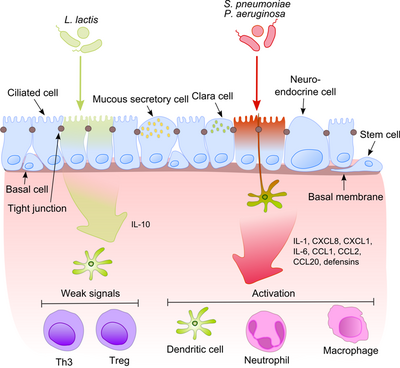
Этот процесс становится гораздо более интригующим, если принять во внимание, что комменсалы часто разделяют свои поверхностные молекулы с патогенами. Эпителиальные клетки оснащены очень чувствительными инструментами распознавания – толл-подобными рецепторами (TLR), нуклеотид-связывающими доменами олигомеризации (NOD)-подобными рецепторами (NLR) и рецепторами, индуцируемыми ретиноевой кислотой (RIG)-I-подобными рецепторами (RLR), которые распознают широкий спектр микробных структурных компонентов. После распознавания патогенных бактерий активируются провоспалительные пути и к очагу инфекции привлекаются клеточные компоненты адаптивного и врожденного иммунитета. [7] Одним из ключевых регуляторов этого процесса является NF-κB , который перемещается из цитоплазмы в ядро и активирует провоспалительные гены в эпителиальных клетках и макрофагах. ДНК-связывающий белковый комплекс распознает дискретную нуклеотидную последовательность (5'-GGG ACT TTC T-3') в расположенной выше области различных генов ответа. Активация NF-κB рядом стимулов: стенками бактериальных клеток или воспалительными цитокинами приводит к его транслокации в ядро.
Напротив, безвредные бактерии не вызывают транслокацию NF-κB в ядро, тем самым предотвращая воспаление, хотя они могут выражать те же молекулярные паттерны, связанные с микробами (MAMP). Один из возможных механизмов, объясняющих этот эффект, был предложен Нейшем, показавшим, что непатогенные S. typhimurium PhoPc и S. pullorum способны запрещать убиквитинирование молекулы-ингибитора NF-κB, ядерного фактора энхансера гена легкого полипептида NF-κB в ингибиторе B-клеток. альфа (IκB-κ). [8] Другое объяснение комменсальной толерантности эпителия относится к посттрансляционной модификации белка путем ковалентного присоединения одного или нескольких мономеров убиквитина (Ub). Ингибирование убиквитинирования приводит к уменьшению воспаления, поскольку только полиубиквитинированный (IκB-κ подвергается деградации с помощью 26S-протеасомы, что позволяет транслокировать NF-κB в ядро и активировать транскрипцию эффекторных генов (например, IL-8). Пробиотические бактерии, такие как лактобациллы , способны модулировать активность убикбиб-протеасомной системы, индуцируя выработку активных форм кислорода (АФК) в эпителиальных клетках. Было показано, что в клетках млекопитающих АФК служат важными вторичными посредниками в многочисленных путях передачи сигнала. ответ на провоспалительные цитокины. Бактериально-индуцированные АФК вызывают окислительную инактивацию каталитического остатка цистеина Ub 12, что приводит к неполной, но временной потере неддиляции куллина-1 и последующему воздействию на передачу сигналов NF-κB и β-катенина. Другой комменсальный вид, B. thetaiotaomicron. , ослабляет экспрессию провоспалительных цитокинов, способствуя ядерному экспорту субъединицы RelA NF-κB через путь, зависимый от рецептора γ, активируемого пролифератором пероксисом (PPAR-γ). PPAR-γ нацелен на транскрипционно активный Rel A и индуцирует ранний ядерный клиренс, ограничивая продолжительность действия NF-κB.
Баланс между возбудителями и комменсалами чрезвычайно важен для поддержания гомеостаза в дыхательных путях.
Дыхательные пути постоянно подвергаются воздействию множества микроорганизмов, некоторые из которых способны персистировать и даже колонизировать дыхательные пути. Это возможно благодаря наличию питательных веществ, кислорода и оптимальной температуры роста. Существует несколько источников питательных веществ, полученных от хозяина, для микробов-резидентов: секреты эпителиальных клеток дыхательных путей (особенно бокаловидных клеток), секреты подслизистых желез и транссудат из плазмы. Более того, пул доступных питательных веществ увеличивается за счет деятельности некоторых представителей микробиоты. Макромолекулярные компоненты респираторного секрета (белки, гликопротеины, липиды, нуклеиновые кислоты) превращаются в питательные вещества (например, углеводы, аминокислоты). Таким образом, метаболическая активность нынешних бактерий позволяет колонизировать новые виды. Комменсальные бактерии непатогенны и защищают наши дыхательные пути от патогенов. Существует несколько возможных механизмов. Комменсалы являются естественными конкурентами болезнетворных бактерий, поскольку имеют тенденцию занимать одну и ту же экологическую нишу внутри организма человека. Во-вторых, они способны вырабатывать антибактериальные вещества, называемые бактериоцинами, которые подавляют рост болезнетворных микроорганизмов.
Роды Bacillus , Lactobacillus , Lactococcus , Staphylococcus , Streptococcus и Streptomyces являются основными продуцентами бактериоцинов в дыхательных путях. Кроме того, известно, что комменсалы индуцируют ответ Th1 и выработку противовоспалительного интерлейкина (IL)-10, антимикробных пептидов, FOXP3, секреторного иммуноглобулина А (sIgA).

Изменения в составе микробного сообщества, по-видимому, играют роль в прогрессировании таких легочных заболеваний, как хроническая обструктивная болезнь легких (ХОБЛ), астма и муковисцидоз . [9] [10] У людей S. aureus является частью нормальной микробиоты , присутствующей в верхних дыхательных путях, [11] а также на коже и слизистой оболочке кишечника. [12] S. aureus , наряду с аналогичными видами, которые могут колонизировать и действовать симбиотически, но могут вызывать заболевания, если начинают захватывать колонизированные ими ткани или проникать в другие ткани, были названы «патобионтами». [11] MRSA может аналогичным образом колонизировать людей, не вызывая у них заболевания. [13] Наличие таких родов, как Mycoplasma , Pseudomonas и Staphylococcus, коррелирует со стабильным состоянием ХОБЛ. С другой стороны, Prevotella , Mesorhizobium , Microbacterium , Micrococcus , Veillonela , Rhizobium , Stenotropomonas и Lactococcus присутствуют преимущественно в когорте здоровых людей. Относительная численность протеобактерий повышена у детей-астматиков. У больных муковисцидозом чаще всего обнаруживают Pseudomonas aeruginosa , Staphylococcus aureus и Burkholderia cepacia .
Высокопроизводительное секвенирование и полногеномное секвенирование предоставят дополнительную информацию о сложности и физиологическом значении комменсальных бактерий в нижних дыхательных путях.
Рисунок 2: Распределение родов грибов в разных участках тела.
{{cite journal}}: Внешняя ссылка |quote=