ДНК-примаза — это фермент , участвующий в репликации ДНК , разновидность РНК-полимеразы . Примаза катализирует синтез короткого сегмента РНК (или ДНК в некоторых живых организмах [1] ), называемого праймером , комплементарным матрице оцДНК (одноцепочечная ДНК). После удлинения участок РНК удаляется экзонуклеазой с 5'-3'-конца и заполняется ДНК.

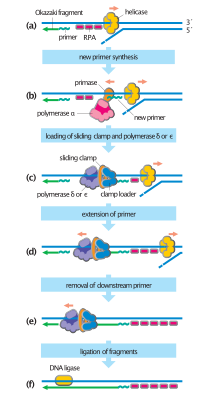
У бактерий примаза связывается с ДНК-хеликазой, образуя комплекс, называемый примосомой . Примаза активируется хеликазой, где она затем синтезирует короткий праймер РНК длиной примерно 11 ± 1 нуклеотид , к которому с помощью ДНК-полимеразы могут быть добавлены новые нуклеотиды. Примазы архей и эукариот представляют собой гетеродимерные белки с одной большой регуляторной и одной крошечной каталитической субъединицей. [2]
Сегменты РНК сначала синтезируются примазой, а затем удлиняются ДНК-полимеразой. [3] Затем ДНК-полимераза образует белковый комплекс с двумя субъединицами примазы, образуя комплекс альфа-ДНК-полимеразы-примазы. Примаза — одна из наиболее склонных к ошибкам и медленных полимераз. [3] Примазы в таких организмах, как E. coli , синтезируют от 2000 до 3000 праймеров со скоростью один праймер в секунду. [4] Примаза также действует как механизм остановки, не позволяя ведущей цепи опережать отстающую цепь , останавливая продвижение репликационной вилки . [5] Стадией, определяющей скорость примазы, является образование первой фосфодиэфирной связи между двумя молекулами РНК. [3]
Механизмы репликации различаются у разных бактерий и вирусов , где примаза ковалентно связана с хеликазой в вирусах, таких как бактериофаг Т7 . [5] В таких вирусах, как вирус простого герпеса (ВПГ-1), примаза может образовывать комплексы с геликазой. [6] Комплекс примаза-геликаза используется для раскручивания дцДНК (двухцепочечной) и синтеза отстающей цепи с использованием праймеров РНК. [6] Большинство праймеров, синтезируемых примазой, имеют длину от двух до трех нуклеотидов. [6]
Существует два основных типа примаз: DnaG , обнаруженный у большинства бактерий, и суперсемейство AEP (архео-эукариотические примазы), обнаруженное у архейных и эукариотических примаз. В то время как бактериальные примазы ( тип DnaG ) состоят из одной белковой единицы (мономера) и синтезируют праймеры РНК, примазы AEP обычно состоят из двух разных единиц примазы (гетеродимера) и синтезируют двухчастные праймеры с компонентами как РНК, так и ДНК. . [7] Хотя эти два суперсемейства примаз функционально схожи, они развивались независимо друг от друга.
Кристаллическая структура примазы в E. coli с ядром, содержащим белок DnaG , была определена в 2000 году. [4] Комплекс DnaG и примазы имеет форму кешью и содержит три субдомена. [4] Центральный субдомен образует складку топрима, состоящую из пяти бета-листов и шести альфа-спиралей . [4] [8] Складка топрима используется для связывания регуляторов и металлов. Примаза использует фосфопереносной домен для координации переноса металлов, что отличает ее от других полимераз. [4] Боковые субъединицы содержат терминали NH 2 и COOH , состоящие из альфа-спиралей и бета-листов. [4] Конец NH 2 взаимодействует с доменом связывания цинка и COOH-концевой областью, которая взаимодействует с DnaB-ID. [4]
Складка Топрима также обнаружена в топоизомеразе и митохондриальной примазе /хеликазе Твинкл. [8] Некоторые DnaG-подобные (бактериоподобные; InterPro : IPR020607 ) примазы были обнаружены в геномах архей. [9]
Эукариотные и архейные примазы, как правило, более похожи друг на друга с точки зрения структуры и механизма, чем на бактериальные примазы. [10] [11] Суперсемейство архей-эукариотических примаз (AEP), к которому принадлежит большинство каталитических субъединиц эукариальных и архейных примаз, недавно было переопределено как семейство примаз-полимераз в знак признания многих других ролей, которые играют ферменты в этом семействе. . [12] Эта классификация также подчеркивает широкое происхождение примас AEP; теперь считается, что суперсемейство осуществляет переход между функциями РНК и ДНК. [13]
Примазы архей и эукариот представляют собой гетеродимерные белки с одной большой регуляторной ( PRIM2 человека , p58) и одной малой каталитической субъединицей ( PRIM1 человека , p48/p49). [2] Большая субъединица содержит N-концевой кластер 4Fe–4S, расщепленный у некоторых архей как PriX/PriCT. [14] Большая субъединица участвует в улучшении активности и специфичности малой субъединицы. Например, удаление части, соответствующей большой субъединице, в слитом белке PolpTN2 приводит к более медленному ферменту с активностью обратной транскриптазы. [13]

Семейство примаз-полимераз AEP обладает разнообразными особенностями, помимо создания только праймеров. В дополнение к праймированию ДНК во время репликации, ферменты AEP могут выполнять дополнительные функции в процессе репликации ДНК, такие как полимеризация ДНК или РНК, терминальный перенос , синтез транслейкоза (TLS) , негомологическое соединение концов (NHEJ) [ 12] и возможно, при перезапуске остановленных вилок репликации. [15] Примазы обычно синтезируют праймеры из рибонуклеотидов (NTP); однако примазы с полимеразными способностями также обладают сродством к дезоксирибонуклеотидам (дНТФ). [16] [11] Примазы с терминальной трансферазной функциональностью способны добавлять нуклеотиды к 3'-концу цепи ДНК независимо от матрицы. Другие ферменты, участвующие в репликации ДНК, например хеликазы, также могут проявлять примазную активность. [17]
Человеческий PrimPol (ccdc111 [16] ) выполняет функции как примазы, так и полимеразы, как и многие архейные примазы; проявляет терминальную трансферазную активность в присутствии марганца; и играет значительную роль в синтезе транслейкоза [18] и в перезапуске остановленных репликационных вилок. PrimPol активно рекрутируется в поврежденные участки посредством взаимодействия с RPA, белком-адаптером, который облегчает репликацию и восстановление ДНК. [15] PrimPol имеет домен цинкового пальца, аналогичный домену некоторых вирусных примаз, который важен для синтеза транслейкоза и активности примазы и может регулировать длину праймера. [18] В отличие от большинства примаз, PrimPol обладает уникальной способностью начинать цепи ДНК с dNTP. [16]
PriS, малая субъединица примазы архей, играет роль в синтезе транслейкоза (TLS) и может обходить распространенные повреждения ДНК. У большинства архей отсутствуют специализированные полимеразы, которые осуществляют TLS у эукариот и бактерий. [19] PriS сам по себе преимущественно синтезирует цепочки ДНК; но в сочетании с PriL активность большой субъединицы РНК-полимеразы увеличивается. [20]
У Sulfolobus solfataricus гетеродимер примазы PriSL может действовать как примаза, полимераза и терминальная трансфераза. Считается, что PriSL инициирует синтез праймеров с помощью NTP, а затем переключается на dNTP. Фермент может полимеризовать цепи РНК или ДНК, при этом длина продуктов ДНК достигает 7000 нуклеотидов (7 т.п.н.). Предполагается, что эта двойная функциональность может быть общей чертой архейных примат. [11]
Многофункциональные примазы АЭП появляются также у бактерий и фагов, их заражающих. Они могут отображать новые организации доменов с доменами, которые приносят еще больше функций, помимо полимеризации. [14]
Бактериальный LigD ( A0R3R7 ) в первую очередь участвует в пути NHEJ. Он имеет полимеразный/примазный домен суперсемейства AEP, 3'-фосфоэстеразный домен и лигазный домен. Он также способен проявлять активность примазы, ДНК и РНК-полимеразы и терминальной трансферазы. Активность полимеризации ДНК может образовывать цепи длиной более 7000 нуклеотидов (7 т.п.н.), тогда как полимеризация РНК дает цепи длиной до 1 т.п.н. [21]
Ферменты AEP широко распространены, и их можно обнаружить закодированными в мобильных генетических элементах, включая вирусы/фаги и плазмиды. Они используют их либо в качестве единственного белка репликации, либо в сочетании с другими белками, связанными с репликацией, такими как хеликазы и, реже, ДНК-полимеразы. [22] В то время как присутствие AEP в эукариотических и архейных вирусах ожидается, поскольку они отражают своих хозяев, [22] бактериальные вирусы и плазмиды также часто кодируют ферменты суперсемейства AEP, как и примазы семейства DnaG. [14] В результате сравнительных геномных исследований в различных бактериальных плазмидах было обнаружено большое разнообразие семейств AEP . [14] Их эволюционная история в настоящее время неизвестна, поскольку они, обнаруженные в бактериях и бактериофагах, слишком отличаются от своих архео-эукариотических гомологов для недавнего горизонтального переноса генов . [22]
MCM-подобная геликаза в штамме Bacillus cereus ATCC 14579 (BcMCM; Q81EV1 ) представляет собой геликазу SF6, слитую с примазой AEP. Помимо функции геликазы, фермент выполняет функции как примазы, так и полимеразы. Ген, кодирующий его, находится в профаге. [17] Он имеет гомологию с ORF904 плазмиды pRN1 из Sulfolobus Islandicus , которая имеет домен AEP PrimPol. [23] Вирус осповакцины D5 и примаза простого герпеса также являются примерами слияния AEP-хеликазы. [12] [6]
PolpTN2 представляет собой примазу архей, обнаруженную в плазмиде TN2. Представляя собой слияние доменов, гомологичных PriS и PriL, он проявляет как примазную, так и ДНК-полимеразную активность, а также функцию терминальной трансферазы. В отличие от большинства примаз, PolpTN2 образует праймеры, состоящие исключительно из dNTP. [13] Неожиданно, когда PriL-подобный домен был усечен, PolpTN2 также мог синтезировать ДНК на матрице РНК, т.е. действовать как РНК-зависимая ДНК-полимераза (обратная транскриптаза). [13]
Даже примасы DnaG могут иметь дополнительные функции, если им предоставлены правильные домены. Фаг T7 gp4 представляет собой слияние примазы и геликазы DnaG и выполняет обе функции при репликации. [5]