Родоцен представляет собой химическое соединение формулы [Rh(C 5 H 5 ) 2 ] . Каждая молекула содержит атом родия , связанный между двумя плоскими ароматическими системами из пяти атомов углерода , известными как циклопентадиенильные кольца, в сэндвич -расположении. Это металлоорганическое соединение , поскольку оно имеет ( гаптические ) ковалентные связи родий-углерод. [2] Радикал [Rh(C 5 H 5 ) 2 ] обнаруживается при температуре выше 150 °C (302 °F) или при улавливании при охлаждении до температуры жидкого азота (-196 °C [-321 °F]). При комнатной температуре пары этих радикалов соединяются через свои циклопентадиенильные кольца, образуя димер — твердое вещество желтого цвета. [1] [3] [4]
История металлоорганической химии включает в себя открытия в XIX веке соли Цейзе [5] [6] [7] и тетракарбонила никеля . [2] Эти соединения представляли собой проблему для химиков, поскольку они не соответствовали существующим моделям химической связи . Дальнейшая проблема возникла с открытием ферроцена , [8] железного аналога родоцена и первого представителя класса соединений, теперь известных как металлоцены . [9] Было обнаружено, что ферроцен необычайно химически стабилен , [10] как и аналогичные химические структуры, включая родоцений, униположительный катион родоцена [Примечание 1] и его кобальтовые и иридиевые аналоги. [11] Изучение металлоорганических соединений, в том числе и этих, в конечном итоге привело к разработке новых моделей связей, которые объяснили их образование и стабильность. [12] [13] Работа над сэндвич-соединениями, включая систему родоцений-родоцен, принесла Джеффри Уилкинсону и Эрнсту Отто Фишеру Нобелевскую премию по химии 1973 года . [14] [15]
Благодаря своей стабильности и относительной простоте получения соли родоцения являются обычным исходным материалом для получения родоцена и замещенных родоценов, которые все нестабильны. В первоначальном синтезе использовались циклопентадиенильный анион и трис(ацетилацетонато)родий(III) ; [11] с тех пор сообщалось о многочисленных других подходах, включая газофазное окислительно-восстановительное трансметаллирование [16] и использование полусэндвичевых предшественников. [17] Октафенилродоцен (производное с восемью присоединенными фенильными группами ) был первым замещенным родоценом, выделенным при комнатной температуре, хотя он быстро разлагается на воздухе. Рентгеновская кристаллография подтвердила, что октафенилродоцен имеет сэндвичевую структуру с шахматной конформацией . [18] В отличие от кобальтоцена, который стал полезным одноэлектронным восстановителем в исследованиях, [19] ни одно из обнаруженных производных родоцена не является достаточно стабильным для таких применений.
Биомедицинские исследователи изучили применение соединений родия и их производных в медицине [20] и сообщили об одном потенциальном применении производного родоцена в качестве радиофармацевтического препарата для лечения небольших видов рака . [21] [22] Производные родоцена используются для синтеза связанных металлоценов, чтобы можно было изучать взаимодействия металл-металл; [23] потенциальные применения этих производных включают молекулярную электронику и исследование механизмов катализа . [24]

Открытия в металлоорганической химии привели к важному пониманию химической связи . О соли Цейзе , K[PtCl 3 (C 2 H 4 )]·H 2 O , сообщалось в 1831 году [5] , а открытие Мондом тетракарбонила никеля ( Ni(CO) 4 ) произошло в 1888 году. [27] Каждый из них содержал связь. между металлическим центром и небольшой молекулой, этиленом в случае соли Цейзе и монооксидом углерода в случае тетракарбонила никеля. [6] Заполняющая пространство модель аниона соли Цейзе (изображение слева) [25] [26] показывает прямую связь между металлическим платиновым центром (показано синим цветом) и атомами углерода (показаны черным) этилена. лиганд ; такие связи металл-углерод являются определяющей характеристикой металлоорганических соединений . Модели связи не могли объяснить природу таких связей металл-алкен до тех пор, пока в 1950-х годах не была предложена модель Дьюара-Чатта-Дункансона . [12] [7] [28] [29] Первоначальная формулировка охватывала только связи металл-алкен [27] , но со временем модель была расширена, чтобы охватить такие системы, как карбонилы металлов (включая [Ni(CO) 4 ] ), где π-связь это важно. [29]
Ферроцен , [Fe(C 5 H 5 ) 2 ] , был впервые синтезирован в 1951 году во время попытки получить фульвален ( C
10ЧАС
8) окислительной димеризацией циклопентадиена ; Было обнаружено, что полученный продукт имеет молекулярную формулу C.
10ЧАС
10Fe и сообщил, что демонстрирует «замечательную стабильность». [10] Это открытие вызвало существенный интерес в области металлоорганической химии, [8] [9] отчасти потому, что структура, предложенная Паусоном и Кили, не соответствовала существовавшим на тот момент моделям связи и не объясняла ее неожиданную стабильность. Следовательно, первоначальная задача заключалась в том, чтобы окончательно определить структуру ферроцена в надежде, что тогда будут понятны его связи и свойства. Сэндвич-структура была выведена и сообщена независимо тремя группами в 1952 году: Роберт Бернс Вудворд и Джеффри Уилкинсон исследовали реакционную способность, чтобы определить структуру [30] и продемонстрировали, что ферроцен подвергается реакциям, аналогичным типичным ароматическим молекулам (таким как бензол ), [31] Эрнст Отто Фишер вывел сэндвич-структуру, а также начал синтезировать другие металлоцены , включая кобальтоцен ; [32] Эйланд и Пепинский предоставили рентгеновское кристаллографическое подтверждение сэндвич-структуры. [33] Применение теории валентных связей к ферроцену с учетом Fe2+
центр и два циклопентадиенид-аниона (C 5 H 5 - ), которые, как известно , согласно правилу Хюккеля являются ароматическими и, следовательно, очень стабильными, позволили правильно предсказать геометрию молекулы. После того, как теория молекулярных орбиталей была успешно применена, причины удивительной стабильности ферроцена стали ясны. [13]
Свойства кобальтоцена, о которых сообщили Уилкинсон и Фишер, показали, что униположительный катион кобальтициния [Co(C 5 H 5 ) 2 ] + проявляет стабильность, аналогичную стабильности самого ферроцена. Это наблюдение не является неожиданным, учитывая, что катион кобальтициния и ферроцен являются изоэлектронными , хотя в то время связь не была понятна. Тем не менее это наблюдение побудило Уилкинсона и Ф. Альберта Коттона попытаться синтезировать соли родоцения [Примечание 1] и иридоцения . [11] Они сообщили о синтезе многочисленных солей родоцения, в том числе содержащих трибромид ( [ Rh(C 5 H 5 ) 2 ]Br 3 ), перхлорат ( [Rh(C 5 H 5 ) 2 ]ClO 4 ) и ринекат. ( [Rh(C 5 H 5 ) 2 ] [Cr(NCS) 4 (NH 3 ) 2 ]·H 2 O ) анионы и обнаружили, что добавление дипикриламина дает соединение состава [Rh(C 5 H 5 ) 2 ] [N(C 6 H 2 N 3 O 6 ) 2 ] . [11] В каждом случае было обнаружено, что катион родоцения обладает высокой стабильностью. Уилкинсон и Фишер получили Нобелевскую премию по химии 1973 года «за новаторскую работу, выполненную независимо друг от друга, по химии металлоорганических, так называемых сэндвичевых соединений ». [14] [15]
Стабильность металлоценов можно напрямую сравнить, посмотрев на потенциалы восстановления одноэлектронного восстановления униположительного катиона. Следующие данные представлены относительно насыщенного каломельного электрода (НКЭ) в ацетонитриле :
Эти данные ясно указывают на стабильность нейтрального ферроцена и катионов кобальтоцения и родоцения. Родоцен составляет ок. На 500 мВ более восстанавливающий, чем кобальтоцен, что указывает на то, что он более легко окисляется и, следовательно, менее стабилен. [1] Более раннее полярографическое исследование перхлората родоцения при нейтральном pH показало пик катодной волны при -1,53 В (по сравнению с SCE) на падающем ртутном электроде , что соответствует образованию родоцена в растворе, но исследователи не смогли выделить нейтральный продукт. из решения. В том же исследовании попытки обнаружить иридоцен путем воздействия на соли иридоцения окислительных условий не увенчались успехом даже при повышенном pH. Эти данные согласуются с высокой нестабильностью родоцена и могут указывать на то, что иридоцен еще более нестабилен. [11]
Правило 18 электронов является эквивалентом правила октетов в химии основной группы и обеспечивает полезное руководство для прогнозирования стабильности металлоорганических соединений . [35] Он предсказывает, что металлоорганические соединения, «в которых сумма валентных электронов металла плюс электронов, пожертвованных группами лигандов, составляет 18, вероятно, будут стабильными». [35] Это помогает объяснить необычно высокую стабильность, наблюдаемую для ферроцена [10] и катионов кобальтициния и родоцения [32] – все три вида имеют аналогичную геометрию и представляют собой изоэлектронные 18-валентные электронные структуры. Нестабильность родоцена и кобальтоцена также понятна с точки зрения правила 18 электронов, поскольку оба представляют собой структуры с 19 валентными электронами; этим объясняются первые трудности с выделением родоцена из растворов родоцена. [11] В химии родоцена доминирует стремление достичь 18-электронной конфигурации. [35]
Родоцен существует в виде [Rh(C 5 H 5 ) 2 ] , парамагнитного 19-валентного электронно- радикального мономера только при температуре или ниже -196 °C (-320,8 °F) ( температура жидкого азота ) или выше 150 °C (302 °F). ) в газовой фазе . [1] [3] [4] Именно эта мономерная форма демонстрирует типичную шахматную сэндвич-структуру металлоцена . При комнатной температуре (25 °C [77 °F]) время жизни мономерной формы в ацетонитриле составляет менее двух секунд; [1] и родоцен образует [Rh(C 5 H 5 ) 2 ] 2 , диамагнитную димерную анса - металлоценовую структуру с 18-валентными электронными мостиками . [36] Электронно-спиновый резонанс (ЭПР), ядерный магнитный резонанс (ЯМР) и инфракрасная спектроскопия (ИК) указывают на наличие равновесия , взаимно превращающего мономерные и димерные формы. [4] Данные ЭПР подтверждают, что мономер обладает осью симметрии высокого порядка (C n , n > 2) с зеркальной плоскостью (σ), перпендикулярной ей в качестве элементов симметрии ; это экспериментально демонстрирует, что мономер действительно обладает типичной сэндвич-структурой металлоцена [3] [примечание 2], хотя интерпретация данных ЭПР подвергается сомнению. [36] Путь разложения мономера также был изучен с помощью масс-спектрометрии . [37] Димеризация представляет собой окислительно-восстановительный процесс; димер представляет собой разновидность родия (I), а мономер имеет центр родия (II). [Примечание 3] В своих стабильных соединениях родий обычно занимает степени окисления +I или +III. [38]
Общий эффект этого процесса димеризации заключается в уменьшении количества электронов вокруг родиевого центра с 19 до 18. Это происходит потому, что окислительное сочетание двух циклопентадиенильных лигандов приводит к образованию нового лиганда с более низкой гаптичностью , который отдает меньше электронов металлическому центру. Термин «гаптичность» используется для обозначения «количества атомов углерода (или других атомов), посредством которых [лиганд] связывает ( n )» [39] с металлическим центром, и обозначается как η n . Например, этиленовый лиганд в соли Цейзе связан с платиновым центром через оба атома углерода и, следовательно, формально имеет формулу K[PtCl 3 (η 2 -C 2 H 4 )]·H 2 O . [6] Каждый карбонильный лиганд в тетракарбониле никеля связан только через атом углерода и, следовательно, описывается как моногаптолиганды, но обозначения η 1 -обычно опускаются в формулах. Циклопентадиенильные лиганды во многих металлоценовых и полусэндвич-соединениях представляют собой пентагаптолиганды, отсюда и формула [Rh(η 5 -C 5 H 5 ) 2 ] для мономера родоцена. В димере родоцена связанные циклопентадиенильные лиганды являются 4-электронными тетрагаптодонорами каждого металлического центра родия(I), в отличие от 6-электронных [ примечание 4] пентагаптоциклопентадиенильных доноров. Повышенная стабильность димера родия (I) с 18 валентными электронами по сравнению с мономером родия (II) с 19 валентными электронами, вероятно, объясняет, почему мономер обнаруживается только в экстремальных условиях. [1] [4]
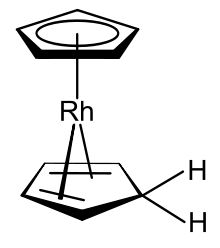
Коттон и Уилкинсон показали [11] , что 18-валентный электрон катиона родия(III) [Rh(η 5 -C 5 H 5 ) 2 ] + может быть восстановлен в водном растворе до мономерной формы; им не удалось изолировать нейтральный продукт, поскольку он не только может димеризоваться, радикальный мономер родия(II) также может спонтанно образовывать стабильные частицы родия(I) со смешанной гаптичностью [(η 5 -C 5 H 5 )Rh(η 4 -C 5 H 6 )] . [3] Различия между родоценом и этим производным обнаруживаются в двух областях:
Эти два изменения делают производную разновидностью электронов с 18 валентностями. Фишер и его коллеги предположили, что образование этого производного родоцена может происходить на отдельных стадиях протонирования и восстановления, но не опубликовали никаких доказательств, подтверждающих это предположение. [3] (η 4 -Циклопентадиен)(η 5 -циклопентадиенил)родий(I), образующееся соединение, представляет собой необычный металлоорганический комплекс, поскольку в качестве лигандов он имеет как циклопентадиенильный анион, так и сам циклопентадиен. Показано, что это соединение можно получить также восстановлением боргидридом натрия раствора родоцения в водном этаноле ; Исследователи, сделавшие это открытие, охарактеризовали продукт как гидрид бисциклопентадиенилродия. [40]
Фишер и его коллеги также изучали химию иридоцена, аналога родоцена и кобальтоцена третьего переходного ряда, обнаружив, что химический состав родоцена и иридоцена в целом схож. Описан синтез многочисленных солей иридоцения, включая трибромид и гексафторфосфат . [4] Так же, как и родоцен, иридоцен димеризуется при комнатной температуре, но форма мономера может быть обнаружена при низких температурах и в газовой фазе, а измерения ИК, ЯМР и ЭПР указывают на наличие химического равновесия и подтверждают сэндвич-структуру мономера иридоцена. . [3] [4] Комплекс [(η 5 -C 5 H 5 )Ir(η 4 -C 5 H 6 )] , аналог производного родоцена, о котором сообщил Фишер, [3] также был изучен и демонстрирует согласующиеся свойства. с большей степенью π-основной связи в системах иридия (I), чем в аналогичных случаях кобальта (I) или родия (I). [41]
Впервые о солях родоцена сообщалось [11] через два года после открытия ферроцена. [10] Эти соли были получены путем взаимодействия карбанионного реактива Гриньяра с циклопентадиенилмагнийбромидом ( C
5ЧАС
5MgBr ) с трис(ацетилацетонато)родием(III) (Rh(acac) 3 ). Совсем недавно катионы родоцена в газовой фазе были получены в результате окислительно-восстановительной реакции трансметаллирования ионов родия (I) с ферроценом или никельоценом . [16]
Сообщалось также о современных методах микроволнового синтеза . [42] Гексафторфосфат родоцения образуется в результате реакции циклопентадиена и гидрата хлорида родия (III) в метаноле после обработки метанольным гексафторфосфатом аммония ; Выход реакции превышает 60% всего за 30 секунд воздействия микроволнового излучения . [43]
Сам родоцен затем образуется путем восстановления солей родоцения расплавленным натрием . [3] Если расплав, содержащий родоцений, обработать металлами натрия или калия, а затем сублимировать на холодный палец, охлаждаемый жидким азотом, образуется черный поликристаллический материал. [36] При нагревании этого материала до комнатной температуры образуется желтое твердое вещество, которое, как было подтверждено, является димером родоцена. Подобный метод можно использовать для получения димера иридоцена. [36]
Разработаны новые подходы к синтезу замещенных циклопентадиенильных комплексов с использованием замещенного винилциклопропенового исходного сырья. [44] [45] [46] Реакции перегруппировки винилциклопропана с расширением кольца с образованием циклопентенов хорошо известны [47] и служат прецедентом перегруппировки винилциклопропенов в циклопентадиены. Катион [(η 5 -C 5 t Bu 3 H 2 )Rh(η 5 -C 5 H 5 )] + был получен в результате последовательности реакций, начинающихся с добавления димера хлорбиметилродия(I), [(η 2 - C 2 H 4 ) 2 Rh(μ-Cl)] 2 , до 1,2,3-три- трет -бутил-3-винил-1-циклопропена с последующей реакцией с циклопентадиенидом таллия : [44] [45]
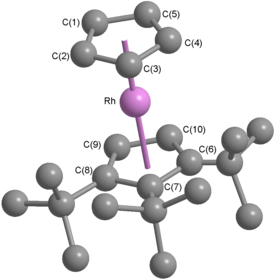
Пентадиедиил родия(III) с 18-валентными электронами, образующийся в результате этой реакции, снова демонстрирует нестабильность родоценового фрагмента, поскольку его можно кипятить с обратным холодильником в толуоле в течение нескольких месяцев без образования 1,2,3-три-трет- бутилродоцена , но при окислении. В условиях быстро образуется катион 1,2,3-три- трет -бутилродоцения. [44] Циклическая вольтамперометрия использовалась для детального исследования этого и подобных процессов. [44] [45] Показано, что механизм реакции включает потерю одного электрона пентадиендиильным лигандом с последующей быстрой перегруппировкой (с потерей атома водорода) с образованием 1,2,3-тритрет-лиганда . -бутилродоцениевый катион. [45] Как тетрафторборатная , так и гексафторофосфатная соли этого катиона были структурно охарактеризованы методом рентгеновской кристаллографии. [45]
[(η 5 -C 5 t Bu 3 H 2 )Rh(η 5 -C 5 H 5 )]BF 4 образует бесцветный центросимметричный моноклинный кристалл, принадлежащий пространственной группе P 2 1 /c , и плотностью 1,486 г. см -3 . [45] Глядя на ORTEP- диаграмму структуры катиона (справа), становится очевидным, что он обладает типичной геометрией, ожидаемой от катиона родоцена или родоцения. Два циклопентадиенильных кольца близки к параллельным ( угол центроид -Rh-центроид составляет 177,2 °), а родиевый центр немного ближе к замещенному циклопентадиенильному кольцу (расстояния Rh-центроид составляют 1,819 Å и 1,795 Å), наблюдение, приписываемое большее индуктивное действие трет -бутильных групп на замещенный лиганд. [45] Диаграмма ORTEP показывает, что катион принимает затменную конформацию в твердом состоянии. Кристаллическая структура гексафторфосфатной соли содержит три кристаллографически независимых катиона: один затменный, один шахматно-ориентированный и один вращательно-неупорядоченный. [45] Это говорит о том, что принятая конформация зависит от присутствующего аниона, а также о том, что энергетический барьер вращения низок - в ферроцене известно, что вращательный энергетический барьер составляет ~ 5 кДж моль -1 как в растворе, так и в газовой фазе. [13]

На диаграмме выше показаны расстояния связи родий-углерод ( красный цвет, внутренние пятиугольники слева) и углерод-углерод ( синий цвет, внешние пятиугольники слева) для обоих лигандов, а также валентные углы ( зеленый цвет, внутренние пятиугольники слева). справа) внутри каждого циклопентадиенильного кольца. Используемые метки атомов такие же, как показано на кристаллической структуре выше. Внутри незамещенного циклопентадиенильного лиганда длины связей углерод-углерод варьируются от 1,35 до 1,40 Å, а внутренние углы связи варьируются от 107 ° до 109 °. Для сравнения: внутренний угол в каждой вершине правильного пятиугольника равен 108°. Длины связей родий-углерод варьируются от 2,16 до 2,18 Å. [45] Эти результаты согласуются с η 5 -координацией лиганда с металлическим центром. В случае замещенного циклопентадиенильного лиганда наблюдается несколько больший разброс: длины связей углерод-углерод варьируются от 1,39 Å до 1,48 Å, внутренние валентные углы варьируются от 106 ° до 111 °, а длины связей родий-углерод варьируются от 2,14. Å и 2,20 Å. Большая вариация замещенного лиганда объясняется искажениями, необходимыми для снятия стерического напряжения, налагаемого соседними трет -бутильными заместителями; несмотря на эти различия, данные показывают, что замещенный циклопентадиенил также является η 5 -координированным. [45]
Стабильность металлоценов меняется при замене кольца. Сравнение потенциалов восстановления катионов кобальтоцения и декаметилкобальтоцения показывает, что декаметильная разновидность составляет ок. на 600 мВ более восстанавливающий, чем исходный металлоцен [19] , такая же ситуация наблюдается в системах ферроцена [48] и родоцена. [49] Следующие данные представлены относительно окислительно-восстановительной пары ферроцений/ферроцен : [50]
Различия в потенциалах восстановления в системе кобальтоцения объясняются индуктивным действием алкильных групп, [19] дополнительно стабилизирующими 18-валентные электроны. Аналогичный эффект наблюдается в данных по родоцению, показанных выше, что снова согласуется с индуктивными эффектами. [45] В замещенной системе иридоцения исследования циклической вольтамперометрии показывают необратимые сокращения при температурах до -60 ° C; [51] для сравнения, восстановление соответствующих родоценов квазиобратимо при комнатной температуре и полностью обратимо при -35 °C. [49] Необратимость восстановления замещенного иридоцения объясняется чрезвычайно быстрой димеризацией образующихся частиц с 19 валентными электронами, что дополнительно иллюстрирует, что иридоцены менее стабильны, чем соответствующие им родоцены. [51]
Объем знаний о соединениях с пентазамещенными циклопентадиенильными лигандами обширен, при этом хорошо известны металлоорганические комплексы пентаметилциклопентадиенильных и пентафенилциклопентадиенильных лигандов . [52] Замены в циклопентадиенильных кольцах родоценов и солей родоцения производят соединения с более высокой стабильностью, поскольку они обеспечивают повышенную делокализацию положительного заряда или электронной плотности , а также обеспечивают стерические препятствия для других частиц, приближающихся к металлическому центру. [37] Известны различные моно- и дизамещенные виды родоцения, но существенная стабилизация не достигается без больших замен. [37] Известные сильнозамещенные соли родоцения включают гексафторфосфат декаметилродоцения [(η 5 -C 5 Me 5 ) 2 Rh]PF 6 , [53] гексафторфосфат декаизопропилродоцения [(η 5 -C 5 i Pr 5 ) 2 Rh]PF 6 , [ 54] и гексафторфосфат октафенилродоцения [(η 5 -C 5 Ph 4 H) 2 Rh]PF 6 . [18] [Примечание 5] Тетрафторборат декаметилродоцения может быть синтезирован из трис(ацетона) комплекса [(η 5 -C 5 Me 5 )Rh(Me 2 CO) 3 ](BF 4 ) 2 реакцией с пентаметилциклопентадиеном , и аналогичный Известен также синтез иридия. [55] Гексафторфосфат декаизопропилродикния был синтезирован в 1,2-диметоксиэтане ( растворитель ) в необычном однореакторном синтезе , который включает образование 20 углерод-углеродных связей : [54]
По аналогичной реакции гексафторфосфат пентаизопропилродоцения [(η 5 -C 5 i Pr 5 )Rh(η 5 -C 5 H 5 )]PF 6 может быть синтезирован из гексафторфосфата пентаметилродоцения [(η 5 -C 5 Me 5 )Rh(η 5 -C 5 H 5 )]PF 6 с выходом 80%. [54] Эти реакции показывают, что кислотность метиловых атомов водорода в пентаметилциклопентадиенильном комплексе может быть значительно увеличена за счет присутствия металлического центра. Механически реакция протекает так, что гидроксид калия депротонирует метильную группу, и образующийся карбанион подвергается нуклеофильному замещению йодидом метила с образованием новой связи углерод-углерод. [54]
Соединения тетрафторборат пентафенилродоцена [(η 5 -C 5 Ph 5 )Rh(η 5 -C 5 H 5 )]BF 4 , и тетрафторборат пентаметилпентафенилродоцена [(η 5 -C 5 Ph 5 )Rh(η 5 -C 5 Me 5 ) )]BF 4 также сообщалось. Они демонстрируют, что сэндвич-соединения родия можно получить из полусэндвич-предшественников. Например, в подходе, во многом аналогичном трис(ацетоновому) синтезу тетрафторбората декаметилродоцения, [55] тетрафторборат пентафенилродоцения был синтезирован из соли трис( ацетонитрила ) [(η 5 -C 5 Ph 5 )Rh(CH 3 CN) 3 ](BF 4 ) 2 по реакции с циклопентадиенидом натрия : [17]

Октафенилродоцен, [(η 5 -C 5 Ph 4 H) 2 Rh], является первым производным родоцена, выделенным при комнатной температуре. Его оливково-зеленые кристаллы быстро разлагаются в растворе и в течение нескольких минут на воздухе, демонстрируя значительно большую чувствительность к воздуху, чем аналогичный комплекс кобальта , хотя он значительно более стабилен, чем сам родоцен. Это различие объясняется относительно меньшей стабильностью состояния родия(II) по сравнению с состоянием кобальта(II). [18] [38] Восстановительный потенциал катиона [(η 5 -C 5 Ph 4 H) 2 Rh] + (измеренный в диметилформамиде относительно пары ферроцений/ферроцен) составляет -1,44 В, что соответствует большей термодинамической стабилизации родоцен по лиганду C 5 HPh 4 по сравнению с лигандами C 5 H 5 или C 5 Me 5 . [18] Кобальтоцен является полезным одноэлектронным восстановителем в исследовательских лабораториях, поскольку он растворим в неполярных органических растворителях, [19] и его окислительно-восстановительная пара достаточно хорошо ведет себя, поэтому его можно использовать в качестве внутреннего стандарта в циклической вольтамперометрии . . [56] Ни один из полученных ранее замещенных родоценов не продемонстрировал достаточную стабильность для использования аналогичным образом.
Синтез октафенилродоцена протекает в три стадии: кипячение диглима с обратным холодильником с последующей обработкой гексафторфосфорной кислотой , а затем восстановлением амальгамы натрия в тетрагидрофуране : [18]
Кристаллическая структура октафенилродоцена имеет шахматную конформацию [18] (аналогичную структуре ферроцена и в отличие от затменной конформации рутеноцена ). [13] Расстояние родий-центроид составляет 1,904 Å, а длина связи родий-углерод в среднем составляет 2,26 Å; длина связи углерод-углерод в среднем составляет 1,44 Å. [18] Все эти расстояния аналогичны тем, которые обнаружены в катионе 1,2,3-три- трет -бутилродоцения, описанном выше, с той лишь разницей, что эффективный размер родиевого центра кажется больше, что согласуется с расширенным ионным радиус родия(II) по сравнению с родием(III). [45]
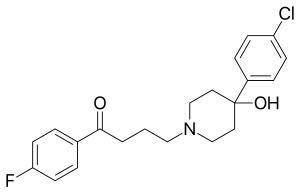
Были проведены обширные исследования металлофармацевтики , [ 57] [58] , включая обсуждение соединений родия в медицине. [20] Значительный объем исследований изучал использование металлоценовых производных рутения [59] и железа [60] в качестве металлофармацевтических препаратов. В одной из областей таких исследований металлоцены использовались вместо фторфенильной группы в галоперидоле [21] , который является фармацевтическим препаратом , классифицируемым как типичный антипсихотик . Исследованное соединение ферроценилгалоперидола имеет строение (C 5 H 5 )Fe(C 5 H 4 )–C(=O)–(CH 2 ) 3 –N(CH 2 CH 2 ) 2 C(OH)–C 6 H. 4 Cl и может быть преобразован в аналог рутения посредством реакции трансметаллирования. С помощью радиоактивного изотопа 103 Ru получен радиофармпрепарат рутеноценил-галоперидол с высоким сродством к тканям легких , но не к тканям головного мозга у мышей и крыс . [21] Бета-распад 103 Ru приводит к образованию метастабильного изотопа 103 m Rh в соединении родоценил-галоперидола. Это соединение, как и другие производные родоцена, имеет нестабильную конфигурацию 19-валентного электрона и быстро окисляется до ожидаемых катионных разновидностей родоцения-галоперидола. [21] Было изучено разделение видов рутеноценил-галоперидола и родоцения-галоперидола, а также распределение каждого из них среди органов тела. [22] 103 м Rh имеет период полураспада 56 минут и испускает гамма-лучи с энергией 39,8 кэВ , поэтому гамма-распад изотопа родия должен последовать вскоре после бета-распада изотопа рутения. Бета- и гамма-излучающие радионуклиды , используемые в медицине, включают 131 I , 59 Fe и 47 Ca , а 103 м Rh было предложено использовать в лучевой терапии небольших опухолей. [20]
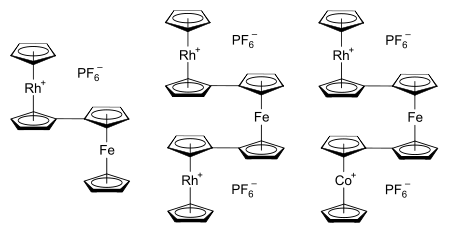
Первоначальной мотивацией для научных исследований родоценовой системы было понимание природы соединений металлоценового класса и связей внутри них. В последнее время интерес возродился из-за желания исследовать и применять взаимодействия металл-металл, которые происходят при соединении металлоценовых систем. [23] Потенциальные применения таких систем включают молекулярную электронику , [24] полупроводниковые (и, возможно, ферромагнитные ) металлоценовые полимеры (пример молекулярной проволоки ), [23] и исследование порога между гетерогенным и гомогенным катализом . [24] Примеры известных биметаллоценов и терметаллоценов, которые обладают родоценильной частью, включают гексафторфосфатные соли родоценилферроцена, 1,1'-диродоценилферроцена и 1-кобальтоценил-1'-родоценилферроцена, [61] каждая из которых показана справа. Связанные металлоцены также могут быть образованы путем введения нескольких металлоценильных заместителей к одному циклопентадиенильному лиганду. [24]
Структурные исследования терметаллоценовых систем показали, что они обычно имеют геометрию «коленчатого вала» в виде «затменного двойного трансоида». [62] Если взять в качестве примера катион 1-кобальтоценил-1'-родоценилферроцена, показанный выше, это означает, что кобальтоценильный и родоценильный фрагменты затмеваются, и, таким образом, атомы углерода 1 и 1' на центральном ферроценовом ядре расположены максимально близко к вертикальному выравниванию. это возможно, учитывая шахматную конформацию циклопентадиенильных колец внутри каждого металлоценового звена. Если смотреть сбоку, это означает, что терметаллоцены напоминают рисунок коленчатого вала вниз-вверх- вниз . [62] Синтез этого терметаллоцена включает объединение растворов родоцения и кобальтоцена с 1,1'-дилитиоферроценом . В результате образуется незаряженное промежуточное соединение со связанными циклопентадиенил-циклопентадиеновыми лигандами, связь которых напоминает связь, обнаруженную в димере родоцена. Эти лиганды затем реагируют с трифенилметилкарбокатионом с образованием терметаллоценовой соли [(η 5 -C 5 H 5 )Rh(μ-η 5 :η 5 -C 5 H 4 –C 5 H 4 )Fe(μ-η 5 :η 5 -C 5 H 4 –C 5 H 4 )Co(η 5 -C 5 H 5 )](PF 6 ) 2 . Этот синтетический путь проиллюстрирован ниже: [61] [62]
Первые родоценийсодержащие полимеры с боковой цепью были получены с помощью методов контролируемой полимеризации, таких как обратимая полимеризация с переносом цепи присоединения-фрагментации (RAFT) и метатезисная полимеризация с раскрытием цикла (ROMP). [63]
Промышленное применение металлоорганической химии переходных металлов появилось еще в 1880-х годах, когда Людвиг Монд показал, что никель можно очистить, используя CO для улавливания никеля в виде газообразного Ni(CO) 4 , который легко отделяется от твердых примесей и позже подвергается термическому разложению с образованием чистого никеля.... Недавние работы показали существование растущего класса металлоферментов, имеющих окружение из металлоорганических лигандов, которое рассматривается как химия ионов металлов, имеющих C-донорные лиганды, такие как CO или метильная группа.
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )Оба металла демонстрируют обширный химический состав, в основном в степени окисления +3, причем +1 также важен, а также существует значительный химический состав иридия +4. В состоянии +2 известно немного соединений, в отличие от ситуации с кобальтом, их более легким гомологом (ответственные факторы включают повышенную стабильность состояния +3 вследствие большей стабилизации низкого спина d 6 при увеличении 10 Dq). (с. 78)