Структуры Льюиса – также называемые формулами точек Льюиса , структурами точек Льюиса , структурами электронных точек или структурами электронных точек Льюиса ( СИД ) – представляют собой диаграммы, которые показывают связи между атомами молекулы , а также неподеленные пары электронов , которые могут существовать в молекула. [1] [2] [3] Структуру Льюиса можно нарисовать для любой ковалентно связанной молекулы, а также для координационных соединений . Структура Льюиса была названа в честь Гилберта Н. Льюиса , который представил ее в своей статье 1916 года «Атом и молекула». [4] Структуры Льюиса расширяют концепцию электронной точечной диаграммы , добавляя линии между атомами для обозначения общих пар в химической связи.
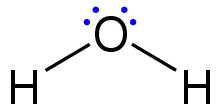
Структуры Льюиса показывают каждый атом и его положение в структуре молекулы с использованием его химического символа. Линии рисуются между атомами, связанными друг с другом (вместо линий можно использовать пары точек). Лишние электроны, образующие неподеленные пары, представлены парами точек и расположены рядом с атомами.
Хотя элементы основной группы второго периода и последующих периодов обычно реагируют путем приобретения, потери или обмена электронами до тех пор, пока они не достигнут электронной конфигурации валентной оболочки с полным октетом (8) электронов, водород (H) может образовывать только связи, которые имеют только два электрона.
Общее количество электронов, представленных в структуре Льюиса, равно сумме чисел валентных электронов на каждом отдельном атоме. Невалентные электроны не представлены в структурах Льюиса.
После того, как общее количество валентных электронов определено, они помещаются в структуру в соответствии со следующими этапами:
Структуры Льюиса для многоатомных ионов можно нарисовать тем же методом. При подсчете электронов отрицательные ионы должны иметь дополнительные электроны, помещенные в их структуры Льюиса; положительные ионы должны иметь меньше электронов, чем незаряженная молекула. При записи льюисовской структуры иона вся структура помещается в скобки, а заряд записывается в виде верхнего индекса справа вверху, вне скобок.
Был предложен более простой метод построения структур Льюиса, исключающий необходимость подсчета электронов: атомы рисуются с указанием валентных электронов; связи затем образуются путем спаривания валентных электронов атомов, участвующих в процессе образования связи, а анионы и катионы образуются путем добавления или удаления электронов к/от соответствующих атомов. [5]
Хитрость заключается в том, чтобы подсчитать валентные электроны, затем подсчитать количество электронов, необходимое для выполнения правила октетов (или, в случае водорода, всего 2 электрона), а затем взять разницу этих двух чисел. Ответ заключается в количестве электронов, образующих связи. Остальные электроны просто заполнят октеты всех остальных атомов.
Была предложена еще одна простая и общая процедура записи структур Льюиса и резонансных форм. [6]
Что касается структур Льюиса, формальный заряд используется при описании, сравнении и оценке вероятных топологических и резонансных структур [7] путем определения кажущегося электронного заряда каждого атома внутри него на основе его электронной точечной структуры, предполагая исключительную ковалентность или отсутствие -полярная связь. Он используется для определения возможной реконфигурации электрона, когда речь идет о механизмах реакций , и часто, за исключениями, приводит к тому же знаку, что и частичный заряд атома. В общем случае формальный заряд атома можно рассчитать по следующей формуле, предполагая нестандартные определения используемой разметки:
где:
Формальный заряд атома рассчитывается как разница между количеством валентных электронов, которые имел бы нейтральный атом, и количеством электронов, принадлежащих ему в структуре Льюиса. Электроны в ковалентной связи делятся поровну между атомами, участвующими в связи. Сумма формальных зарядов иона должна быть равна заряду иона, а сумма формальных зарядов нейтральной молекулы должна быть равна нулю.
Для некоторых молекул и ионов трудно определить, какие неподеленные пары следует переместить для образования двойных или тройных связей, и для одной и той же молекулы или иона могут быть записаны две или более разные резонансные структуры. В таких случаях обычно все они пишутся с двусторонними стрелками между ними . Иногда это происходит, когда несколько атомов одного типа окружают центральный атом, и это особенно характерно для многоатомных ионов.
Когда возникает такая ситуация, структура Льюиса молекулы называется резонансной структурой , и молекула существует как резонансный гибрид. Каждая из различных возможностей накладывается на другие, и считается, что молекула имеет структуру Льюиса, эквивалентную некоторой комбинации этих состояний.
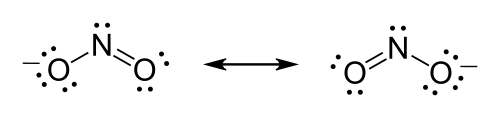
Нитрат-ион ( NO−3), например, должен образовывать двойную связь между азотом и одним из атомов кислорода, чтобы удовлетворить правилу октетов для азота. Однако, поскольку молекула симметрична, не имеет значения, какой из атомов кислорода образует двойную связь. В этом случае возможны три резонансные структуры. Выразить резонанс при рисовании структур Льюиса можно либо нарисовав каждую из возможных форм резонанса и поместив между ними двунаправленные стрелки, либо используя пунктирные линии для обозначения частичных связей (хотя последнее является хорошим представлением резонансного гибрида, который формально говоря, это не структура Льюиса).
При сравнении резонансных структур одной и той же молекулы обычно те, у которых наименьшее количество формальных зарядов, вносят больший вклад в общий резонансный гибрид. Когда необходимы формальные заряды, предпочтение отдается резонансным структурам, которые имеют отрицательные заряды на более электроотрицательных элементах и положительные заряды на менее электроотрицательных элементах.
Одиночные связи также можно перемещать таким же образом, чтобы создать резонансные структуры для гипервалентных молекул , таких как гексафторид серы , что является правильным описанием в соответствии с квантово-химическими расчетами вместо обычной модели расширенного октета.
Резонансную структуру следует интерпретировать не как указание на то, что молекула переключается между формами, а как на то, что молекула действует как среднее из нескольких форм.
Формула нитрит -иона NO.−2.

Химические структуры можно записать в более компактной форме, особенно при изображении органических молекул . В сокращенных структурных формулах многие или даже все ковалентные связи могут быть опущены, при этом нижние индексы указывают количество идентичных групп, присоединенных к конкретному атому. Еще одна сокращенная структурная диаграмма — это скелетная формула (также известная как формула линии связи или диаграмма углеродного скелета). В скелетной формуле атомы углерода обозначаются не символом C, а вершинами линий . Атомы водорода, связанные с углеродом, не показаны — их можно определить, подсчитав количество связей с конкретным атомом углерода — предполагается, что каждый углерод имеет в общей сложности четыре связи, поэтому любые не показанные связи косвенно относятся к атомам водорода.
Другие диаграммы могут быть более сложными, чем структуры Льюиса, показывая связи в 3D с использованием различных форм, таких как диаграммы заполнения пространства .
Несмотря на свою простоту и развитие в начале двадцатого века, когда понимание химической связи было еще зачаточным, структуры Льюиса отражают многие ключевые особенности электронной структуры ряда молекулярных систем, в том числе те, которые имеют отношение к химической реакционной способности. Таким образом, они продолжают широко использоваться химиками и преподавателями химии. Это особенно верно в области органической химии , где все еще доминирует традиционная модель связи валентной связи, а механизмы часто понимаются в терминах обозначений в виде кривых стрелок , наложенных на скелетные формулы , которые являются сокращенными версиями структур Льюиса. Из-за большего разнообразия схем связывания, встречающихся в неорганической и металлоорганической химии , многие из встречающихся молекул требуют использования полностью делокализованных молекулярных орбиталей для адекватного описания их связей, что делает структуры Льюиса сравнительно менее важными (хотя они все еще распространены).
Важно отметить, что существуют простые и архетипические молекулярные системы, для которых описание Льюиса, по крайней мере в неизмененной форме, вводит в заблуждение или неточно. Примечательно, что наивное рисование структур Льюиса для молекул, о которых экспериментально известно, что они содержат неспаренные электроны (например, O 2 , NO и ClO 2 ), приводит к неверным выводам о порядках связей, длинах связей и/или магнитных свойствах. Простая модель Льюиса также не объясняет явление ароматичности . Например, структуры Льюиса не дают объяснения, почему циклический C 6 H 6 (бензол) испытывает особую стабилизацию, выходящую за рамки обычных эффектов делокализации, тогда как C 4 H 4 (циклобутадиен) фактически испытывает особую дестабилизацию . [ нужна цитата ] Теория молекулярных орбиталей дает наиболее простое объяснение этим явлениям. [ оригинальное исследование? ]