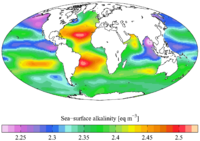
Щелочность (от арабского : القلوية , латинизированного : al-qaly , букв. «пепел солянки » ) [1] — это способность воды противостоять подкислению . [2] Не следует путать его с основностью , которая является абсолютным показателем по шкале pH . Щелочность — это сила буферного раствора , состоящего из слабых кислот и сопряженных с ними оснований . Его измеряют путем титрования раствора кислотой, такой как HCl , до тех пор, пока его pH резко не изменится или не достигнет известной конечной точки, при которой это происходит. Щелочность выражается в единицах концентрации, таких как мэкв/л ( миллиэквиваленты на литр ), мкэкв/кг (микроэквиваленты на килограмм) или мг/л CaCO 3 (миллиграммы на литр карбоната кальция ). [3] Каждое из этих измерений соответствует количеству кислоты, добавленной в качестве титранта .
В пресной воде , особенно на неизвестняковой местности , щелочность низкая и содержит много ионов. В океане, с другой стороны, в щелочности полностью преобладают карбонаты и бикарбонаты плюс небольшой вклад бората . [4]
Хотя щелочность — это в первую очередь термин, используемый лимнологами [5] и океанографами , [3] он также используется гидрологами для описания временной жесткости . Более того, измерение щелочности важно для определения способности ручья нейтрализовать кислотные загрязнения из осадков или сточных вод . Это один из лучших показателей чувствительности потока к кислотным воздействиям. [6] Могут наблюдаться долгосрочные изменения щелочности ручьев и рек в ответ на антропогенные воздействия, такие как кислотные дожди, вызванные выбросами SO x и NO x . [7]
В 1884 году профессор Вильгельм (Уильям) Диттмар из Андерсон-колледжа, ныне Университета Стратклайда , проанализировал 77 образцов нетронутой морской воды со всего мира, привезенных экспедицией «Челленджер» . Он обнаружил, что в морской воде основные ионы находятся в фиксированном соотношении, подтверждая гипотезу Йохана Георга Форххаммера , которая теперь известна как принцип постоянных пропорций. Однако было одно исключение. Диттмар обнаружил, что в глубинах океана концентрация кальция несколько выше, и назвал это увеличение щелочностью. [ нужна цитата ]
Также в 1884 году Сванте Аррениус защитил докторскую диссертацию, в которой он отстаивал существование ионов в растворе и определял кислоты как доноры ионов гидроксония , а основания - как доноры гидроксид- ионов. За эту работу он получил Нобелевскую премию по химии в 1903 году . См . также Сванте Аррениус#Ионная диссоциация .
Щелочность примерно означает молярное количество оснований в растворе, которое можно превратить в незаряженные соединения под действием сильной кислоты. Например, 1 моль HCO−
3в растворе представляет собой 1 мольный эквивалент, а 1 моль CO2−
3составляет 2 молярных эквивалента, поскольку для уравновешивания заряда потребуется вдвое больше ионов H + . Полный заряд раствора всегда равен нулю. [8] Это приводит к параллельному определению щелочности, которое основано на балансе зарядов ионов в растворе.
Некоторые ионы, включая Na + , K + , Ca 2+ , Mg 2+ , Cl − , SO2−
4, и нет−
3являются « консервативными », так что на них не влияют изменения температуры, давления или pH. [8] Другие, такие как HCO−
3на них влияют изменения pH, температуры и давления. Изолируя консервативные ионы на одной стороне этого уравнения баланса заряда, неконсервативные ионы, которые принимают или отдают протоны и, таким образом, определяют щелочность, группируются на другой стороне уравнения.
Этот комбинированный баланс зарядов и баланс протонов называется общей щелочностью . [9] На общую щелочность (не сильно) влияют температура, давление или pH, и, таким образом, она сама по себе является консервативным показателем, что увеличивает ее полезность в водных системах. Все анионы, кроме HCO−
3и CO2−
3имеют низкие концентрации в поверхностных водах Земли (ручьях, реках и озерах). При этом карбонатная щелочность , равная [ HCO−
3] + 2[ СО2−
3] также примерно равна общей щелочности поверхностных вод. [8]
Щелочность измеряет способность раствора нейтрализовать кислоты до точки эквивалентности карбоната или бикарбоната, определяемой как pH 4,5 для многих океанографических/лимнологических исследований. [10] Щелочность равна стехиометрической сумме оснований в растворе. В большинстве поверхностных вод Земли карбонатная щелочность имеет тенденцию составлять большую часть общей щелочности из-за обычного возникновения и растворения карбонатных пород и других геологических процессов выветривания , которые производят карбонатные анионы. Другие распространенные природные компоненты, которые могут способствовать повышению щелочности, включают борат , гидроксид , фосфат , силикат , растворенный аммиак и сопряженные основания органических кислот (например, ацетат ). Растворы, производимые в лаборатории, могут содержать практически неограниченное количество веществ, способствующих щелочности. Щелочность часто выражается в молярном эквиваленте на литр раствора или на килограмм растворителя. В коммерческих целях (например, в сфере плавательных бассейнов) и нормативных актах щелочность также может указываться в частях на миллион эквивалента карбоната кальция (ppm CaCO 3 ) [ нужна ссылка ] . Щелочность иногда неправильно используется как синоним основности . Например, добавление CO 2 снижает pH раствора, тем самым снижая основность, в то время как щелочность остается неизменной (см. пример ниже).
Для различных методов измерения щелочности указаны различные титранты , конечные точки и индикаторы . Соляная и серная кислоты являются обычными титрантами кислоты, а фенолпталеин , метиловый красный и бромкрезоловый зеленый являются обычными индикаторами. [11]
В типичных грунтовых или морских водах измеренная общая щелочность принимается равной:
(Нижний индекс T указывает измеренную общую концентрацию соединений в растворе. Это противоположно свободной концентрации, которая учитывает значительное количество взаимодействий ионных пар , которые происходят в морской воде.)
Щелочность можно измерить путем титрования образца сильной кислотой до тех пор, пока не будет израсходована вся буферная емкость вышеупомянутых ионов выше pH бикарбоната или карбоната. Эта точка функционально установлена на уровне pH 4,5. На данный момент все интересующие основания протонированы до нулевого уровня, следовательно, они больше не вызывают щелочность. В карбонатной системе ионы бикарбоната [ HCO−
3] и карбонат-ионы [ CO2−
3] превратились в угольную кислоту [H 2 CO 3 ] при этом pH. Этот pH также называется точкой эквивалентности CO 2 , где основным компонентом воды является растворенный CO 2 , который в водном растворе превращается в H 2 CO 3 . В этой точке нет сильных кислот и оснований. Поэтому щелочность моделируется и количественно оценивается относительно точки эквивалентности CO 2 . Поскольку щелочность измеряется относительно точки эквивалентности CO 2 , растворение CO 2 , хотя и добавляет кислоту и растворенный неорганический углерод, не меняет щелочность. В природных условиях растворение основных пород и добавление аммиака [NH 3 ] или органических аминов приводит к добавлению основания в природные воды в точке эквивалентности CO 2 . Растворенное в воде основание повышает pH и титрует эквивалентное количество CO 2 до бикарбонат-иона и карбонат-иона. В равновесном состоянии вода содержит определенное количество щелочности, обусловленной концентрацией анионов слабых кислот. И наоборот, добавление кислоты превращает анионы слабой кислоты в CO 2 , а постоянное добавление сильных кислот может привести к тому, что щелочность станет меньше нуля. [12] Например, при добавлении кислоты к обычному раствору морской воды происходят следующие реакции:
Из приведенных выше реакций протонирования видно, что большинство оснований потребляют один протон (H + ), чтобы стать нейтральной разновидностью, тем самым увеличивая щелочность на один на эквивалент. СО2−
3однако он поглотит два протона, прежде чем станет видом с нулевым уровнем (CO 2 ), таким образом, он увеличивает щелочность на два протона на моль CO .2−
3. [H + ] и [ HSO−
4] уменьшают щелочность, так как выступают источниками протонов. Их часто обозначают вместе как [H + ] T .
Щелочность обычно указывается в мг/л в пересчете на CaCO 3 . (В данном случае уместно использовать союз «как», поскольку щелочность возникает в результате смеси ионов, но сообщается «как будто» все это происходит из-за CaCO 3 .) Это можно преобразовать в миллиэквиваленты на литр (мэкв/л). путем деления на 50 (приблизительная молекулярная масса CaCO 3 деленная на 2).
Добавление (или удаление) CO 2 к раствору не меняет его щелочность, поскольку в результате суммарной реакции образуется то же количество эквивалентов положительно вносящих вклад частиц (H + ), что и отрицательно вносящих вклад частиц ( HCO−
3и/или CO2−
3). Добавление CO 2 в раствор снижает его pH, но не влияет на щелочность.
При всех значениях pH:
Только при высоких (основных) значениях pH:
Добавление CO 2 к раствору, контактирующему с твердым веществом, может (с течением времени) влиять на щелочность, особенно для карбонатных минералов, контактирующих с грунтовыми или морскими водами. Растворение (или осаждение) карбонатных пород оказывает сильное влияние на щелочность. Это связано с тем, что карбонатная порода состоит из CaCO 3 , и ее диссоциация приведет к добавлению Ca 2+ и CO.2−
3в раствор. Ca 2+ не влияет на щелочность, а CO2−
3увеличит щелочность на 2 единицы. Повышенное растворение карбонатных пород в результате подкисления кислотных дождей и добычи полезных ископаемых способствовало повышению концентрации щелочности в некоторых крупных реках на востоке США. [7] Следующая реакция показывает, как кислотные дожди, содержащие серную кислоту, могут привести к увеличению щелочности рек за счет увеличение количества бикарбонат-иона:
Другой способ записи:
Чем ниже pH, тем выше будет концентрация бикарбоната. Это показывает, как более низкий pH может привести к более высокой щелочности, если количество образующегося бикарбоната превышает количество H + , оставшегося после реакции. Это так, поскольку количество кислоты в дождевой воде невелико. Если эти щелочные грунтовые воды позже вступят в контакт с атмосферой, они могут потерять CO 2 , осадить карбонаты и тем самым снова стать менее щелочными. Когда карбонатные минералы, вода и атмосфера находятся в равновесии, происходит обратимая реакция.
показывает, что pH будет зависеть от концентрации ионов кальция, причем более низкий pH соответствует более высокой концентрации ионов кальция. В этом случае, чем выше pH, тем больше будет бикарбоната и карбонат-иона, в отличие от описанной выше парадоксальной ситуации, когда равновесия с атмосферой нет.
В океане в щелочности полностью преобладают карбонаты и бикарбонаты плюс небольшой вклад боратов . [4]
Таким образом, химическое уравнение щелочности морской воды выглядит так:
Существует множество методов повышения щелочности океана . Пожалуй, наиболее известным является растворение карбоната кальция с образованием Ca 2+ и CO.2−
3(карбонат). Карбонат-ион может поглотить два иона водорода. Следовательно, это вызывает чистое увеличение щелочности океана. Растворение карбоната кальция происходит в районах океана, недонасыщенных карбонатом кальция.
Увеличение уровня углекислого газа в атмосфере из-за выбросов углекислого газа приводит к увеличению поглощения CO 2 из атмосферы в океаны. [13] Это не влияет на щелочность океана [14] : 2252 , но приводит к снижению значения pH (так называемое подкисление океана ). [15] Повышение щелочности океана было предложено как один из вариантов повышения щелочности океана и, следовательно, защиты от изменений pH. [16] : 181
Биологические процессы оказывают гораздо большее влияние на щелочность океана в коротких (от минут до столетий) временных масштабах. [17] Аэробное дыхание органических веществ может снизить щелочность за счет высвобождения протонов. [17] Денитрификация и восстановление сульфатов происходят в средах с ограниченным содержанием кислорода. Оба этих процесса потребляют ионы водорода (что увеличивает щелочность) и выделяют газы (N 2 или H 2 S), которые в конечном итоге уходят в атмосферу. Нитрификация и окисление сульфидов уменьшают щелочность за счет высвобождения протонов в качестве побочного продукта реакций окисления. [18]
Щелочность океана меняется со временем, особенно в геологических временных масштабах (тысячелетия). Изменения в балансе между земным выветриванием и осаждением карбонатных минералов (например, в зависимости от закисления океана) являются основными долгосрочными факторами щелочности океана. [19] В человеческом масштабе средняя щелочность океана относительно стабильна. [20] Сезонная и годовая изменчивость средней щелочности океана очень низкая. [21]
Щелочность варьируется в зависимости от местоположения в зависимости от испарения/осадков, адвекции воды, биологических и геохимических процессов. [4]
Смешивание с преобладанием реки также происходит вблизи берега; он наиболее силен вблизи устья большой реки. Здесь реки могут выступать как источником, так и стоком щелочности. AT следует за стоком реки и имеет линейную зависимость от солености. [21]
Щелочность океана также следует общим тенденциям, зависящим от широты и глубины. Было показано, что AT часто обратно пропорционален температуре поверхности моря (SST). Поэтому она обычно увеличивается с увеличением широты и глубины. В результате области апвеллинга (где вода из глубин океана выталкивается на поверхность) также имеют более высокие значения щелочности. [22]
Существует множество программ по измерению, регистрации и изучению щелочности океана, а также многих других характеристик морской воды, таких как температура и соленость. К ним относятся: GEOSECS (Геохимическое исследование разрезов океана), [23] TTO/NAS (Исследование временных индикаторов в океане/Северной Атлантике), JGOFS (Совместное исследование глобальных потоков океана), [24] WOCE (Эксперимент по циркуляции мирового океана), [ 25] КАРИНА (Углекислый газ в Атлантическом океане). [26]
{{citation}}: CS1 maint: DOI неактивен по состоянию на январь 2024 г. ( ссылка )Следующие пакеты рассчитывают состояние карбонатной системы морской воды (включая pH):