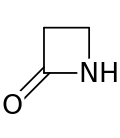
Бета -лактамное ( β-лактамное ) кольцо представляет собой четырехчленный лактам . [1] Лактам представляет собой циклический амид , а бета -лактамы названы так потому, что атом азота присоединен к атому β-углерода по отношению к карбонилу. Самый простой возможный β-лактам — это 2-азетидинон. β-лактамы являются важными структурными единицами лекарственных средств, что проявляется во многих β-лактамных антибиотиках . [2] До 1970 года большинство исследований β-лактамов было связано с группами пенициллинов и цефалоспоринов , но с тех пор было описано большое разнообразие структур. [3] [4]
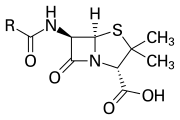
β-лактамное кольцо является частью базовой структуры нескольких семейств антибиотиков , основными из которых являются пенициллины , цефалоспорины , карбапенемы и монобактамы , которые поэтому также называются β-лактамными антибиотиками . Почти все эти антибиотики действуют путем ингибирования биосинтеза клеточной стенки бактерий . Это оказывает летальное воздействие на бактерии , хотя любая популяция бактерий обычно содержит подгруппу, устойчивую к β-лактамным антибиотикам. Устойчивость бактерий возникает в результате экспрессии одного из многих генов, отвечающих за выработку β-лактамаз , класса ферментов, которые разрывают β-лактамное кольцо. У различных видов бактерий зарегистрировано более 1800 различных ферментов β-лактамаз. [5] Эти ферменты широко различаются по своей химической структуре и каталитической эффективности. [6] Когда бактериальные популяции имеют эти устойчивые подгруппы, лечение β-лактамами может привести к тому, что устойчивый штамм станет более распространенным и, следовательно, более вирулентным. Антибиотики, производные β-лактамов, можно считать одним из наиболее важных классов антибиотиков, но они склонны к клинической резистентности. β-лактам проявляет свои антибиотические свойства, имитируя природный субстрат d-Ala-d-Ala для группы ферментов, известных как пенициллин-связывающие белки (PBP), функция которых заключается в сшивании пептидогликановой части клеточной стенки. бактерии. [7]
β-лактамное кольцо также содержится в некоторых других лекарствах, таких как препарат , ингибитор абсорбции холестерина эзетимиб .
Первый синтетический β-лактам был получен Германом Штаудингером в 1907 году реакцией Шиффова основания анилина и бензальдегида с дифенилкетеном [8] [9] в результате [2+2] -циклоприсоединения (Ph указывает на фенильную функциональную группу):
Разработано множество методов синтеза β-лактамов. [10] [11] [12]
Синтез β-лактамов по Брекпоту [13] позволяет получить замещенные β-лактамы путем циклизации эфиров бета-аминокислот с использованием реактива Гриньяра . [14] Реактив Мукаямы также используется в модифицированном синтезе Брекпота. [13]
Из-за деформации кольца β-лактамы гидролизуются легче, чем линейные амиды или более крупные лактамы. Этот штамм дополнительно увеличивается за счет слияния со вторым кольцом, как это обнаружено у большинства β-лактамных антибиотиков. Эта тенденция обусловлена снижением амидного характера β-лактама из-за апланарности системы. Атом азота идеального амида sp 2 -гибридизирован вследствие резонанса , а sp 2 -гибридизированные атомы имеют тригональную плоскую геометрию связей . Поскольку геометрия пирамидальной связи навязывается атому азота напряжением кольца, резонанс амидной связи уменьшается, и карбонил становится более кетоподобным . Нобелевский лауреат Роберт Бернс Вудворд описал параметр h как меру высоты тригональной пирамиды, определяемой азотом (как вершиной ) и тремя соседними с ним атомами. h соответствует прочности связи β-лактама с меньшими числами (более плоскими; больше похожими на идеальные амиды), которые являются более сильными и менее реакционноспособными. [15] Монобактамы имеют значения h от 0,05 до 0,10 ангстрем (Å). Цефемы имеют значения h в пределах 0,20–0,25 Å. Пенамы имеют значения в диапазоне 0,40–0,50 Å, тогда как карбапенемы и клавамы имеют значения 0,50–0,60 Å, будучи наиболее реакционноспособными из β-лактамов в отношении гидролиза. [16]