Биобанк — это тип биорепозитория , в котором хранятся биологические образцы (обычно человеческие) для использования в исследованиях. Биобанки стали важным ресурсом в медицинских исследованиях, поддерживая многие типы современных исследований, такие как геномика и персонализированная медицина .
Биобанки могут предоставить исследователям доступ к данным, представляющим большое количество людей. Образцы в биобанках и данные, полученные из этих образцов, часто могут использоваться несколькими исследователями для межцелевых исследований. Например, многие заболевания связаны с однонуклеотидными полиморфизмами . Исследования ассоциаций по всему геному с использованием данных десятков или сотен тысяч людей могут идентифицировать эти генетические ассоциации как потенциальные биомаркеры заболеваний . Многие исследователи боролись за получение достаточного количества образцов до появления биобанков.
Биобанки вызвали вопросы о конфиденциальности, исследовательской этике и медицинской этике . Мнения о том, что составляет надлежащую этику биобанков, расходятся. Однако был достигнут консенсус, что работа биобанков без установления тщательно продуманных руководящих принципов и политик может быть пагубной для сообществ, которые участвуют в программах биобанков.
Термин «биобанк» впервые появился в конце 1990-х годов и является широким термином, который развивался в последние годы. [1] [2] Одно из определений — «организованная коллекция человеческого биологического материала и связанной с ним информации, хранящаяся для одной или нескольких исследовательских целей». [3] [4] Коллекции растительных, животных, микробных и других нечеловеческих материалов также могут быть описаны как биобанки, но в некоторых обсуждениях этот термин зарезервирован для человеческих образцов. [3]
Биобанки обычно включают криогенные хранилища для образцов. [5] Они могут варьироваться по размеру от отдельных холодильников до складов и обслуживаются такими учреждениями, как больницы, университеты, некоммерческие организации и фармацевтические компании. [5]
Биобанки можно классифицировать по назначению или конструкции. Биобанки, ориентированные на болезни, обычно имеют больничную принадлежность, через которую они собирают образцы, представляющие различные заболевания, возможно, для поиска биомаркеров, связанных с болезнью. [6] [7] Биобанки, ориентированные на население, не нуждаются в особой больничной принадлежности, поскольку они берут образцы у большого количества людей всех типов, возможно, для поиска биомаркеров восприимчивости к болезням в общей популяции. [8]
В 2008 году исследователи США хранили 270 миллионов образцов в биобанках, а скорость сбора новых образцов составляла 20 миллионов в год. [11] Эти цифры представляют собой фундаментальное мировое изменение характера исследований с того времени, когда такое количество образцов не могло быть использовано, и до того времени, когда исследователи начали требовать их. [11] В совокупности исследователи начали выходить за рамки одноцентровых исследовательских центров и переходить к качественно иной исследовательской инфраструктуре следующего поколения. [12] Некоторые из проблем, возникших в связи с появлением биобанков, — это этические, правовые и социальные вопросы, связанные с их существованием, включая справедливость сбора пожертвований от уязвимых групп населения, предоставление информированного согласия донорам, логистику раскрытия данных участникам, право собственности на интеллектуальную собственность, а также конфиденциальность и безопасность доноров, которые участвуют. [11] Из-за этих новых проблем исследователи и политики стали требовать новые системы управления исследованиями. [12]
Многие исследователи определили биобанкинг как ключевую область для развития инфраструктуры в целях содействия открытию и разработке лекарственных препаратов . [3]
К концу 1990-х годов ученые поняли, что хотя многие заболевания вызваны, по крайней мере, частично генетическим компонентом, лишь немногие заболевания возникают из-за одного дефектного гена ; большинство генетических заболеваний вызваны несколькими генетическими факторами на нескольких генах. [13] Поскольку стратегия изучения только отдельных генов была неэффективна для поиска генетических компонентов многих заболеваний, и поскольку новые технологии сделали стоимость исследования одного гена по сравнению со сканированием всего генома примерно одинаковой, ученые начали собирать гораздо большие объемы генетической информации, когда вообще что-либо нужно было собирать. [13] В то же время технологические достижения также сделали возможным широкий обмен информацией, поэтому, когда данные были собраны, многие ученые, занимающиеся генетикой, обнаружили, что доступ к данным из сканирования всего генома, собранным по какой-либо одной причине, на самом деле будет полезен во многих других типах генетических исследований. [13] В то время как раньше данные обычно хранились в одной лаборатории, теперь ученые начали хранить большие объемы генетических данных в отдельных местах для использования и обмена сообществом. [13]
Непосредственным результатом проведения полногеномного сканирования и обмена данными стало открытие множества однонуклеотидных полиморфизмов , причем ранний успех был улучшением по сравнению с идентификацией около 10 000 из них с помощью сканирования одного гена и до биобанков по сравнению с 500 000 к 2007 году после того, как практика полногеномного сканирования существовала в течение нескольких лет. [13] Проблема оставалась; эта меняющаяся практика позволяла собирать данные о генотипе , но она не сопровождалась системой сбора связанных данных о фенотипе . [13] В то время как данные о генотипе поступают из биологического образца, такого как образец крови, данные о фенотипе должны поступать из обследования донора образца с помощью интервью, физической оценки, обзора истории болезни или какого-либо другого процесса, который может быть трудно организовать. [13] Даже когда эти данные были доступны, существовали этические неопределенности относительно степени и способов, которыми права пациента могли быть сохранены путем их связывания с генотипическими данными. [13] Институт биобанка начал развиваться для хранения генотипических данных, связывания их с фенотипическими данными и обеспечения их более широкого доступа для исследователей, которым они были нужны. [13]
Биобанки, включающие образцы для генетического тестирования , исторически состояли в основном из образцов, полученных от лиц европейского происхождения. [14] Необходимо диверсифицировать образцы биобанков, и исследователи должны учитывать факторы, влияющие на недостаточно представленные популяции. [15] [16]
В ноябре 2020 года ученые начали собирать живые фрагменты, образцы тканей и ДНК находящихся под угрозой исчезновения кораллов Большого Барьерного рифа для предупредительного биобанка для возможных будущих восстановительных и реабилитационных мероприятий. [17] Несколькими месяцами ранее другая австралийская группа исследователей сообщила, что они эволюционировали и сделали такие кораллы более устойчивыми к нагреванию. [18]
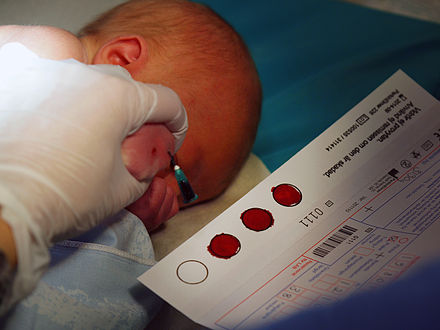
Образцы , хранящиеся в биобанке и предоставляемые исследователям, берутся путем отбора проб . Типы образцов включают кровь , мочу , клетки кожи, ткани органов и другие материалы. Все чаще методы отбора образцов тканей становятся более целенаправленными, иногда с использованием МРТ для определения того, какие конкретные области ткани следует отобрать. [19] [20] Биобанк хранит эти образцы в хорошем состоянии до тех пор, пока они не понадобятся исследователю для проведения теста, эксперимента или анализа. [ необходима цитата ]
Биобанки, как и другие базы данных ДНК, должны тщательно хранить и документировать доступ к образцам и информации о донорах. [21] Образцы должны надежно храниться с минимальным ухудшением с течением времени, и они должны быть защищены от физических повреждений, как случайных, так и преднамеренных. Регистрация каждого образца, входящего и выходящего из системы, хранится централизованно, как правило, в компьютерной системе, которая может часто резервироваться. [21] Отмечается физическое местоположение каждого образца, чтобы обеспечить быстрое местоположение образцов. Архивные системы деидентифицируют образцы, чтобы уважать конфиденциальность доноров и позволять исследователям скрывать анализ. [21] База данных, включая клинические данные, хранится отдельно с помощью безопасного метода для связывания клинической информации с образцами тканей. [21] Иногда используется хранение образцов при комнатной температуре, и оно было разработано в ответ на предполагаемые недостатки низкотемпературного хранения, такие как затраты и вероятность отказа морозильника. [21] Современные системы небольшие и способны хранить около 40 000 образцов примерно в одной десятой пространства, необходимого для морозильника с температурой −80 °C (−112 °F). Повторные или разделенные образцы часто хранятся в отдельных местах в целях безопасности. [21]
Одним из спорных вопросов, связанных с большими базами данных генетического материала, является вопрос о праве собственности на образцы. По состоянию на 2007 год в Исландии действовало три разных закона о праве собственности на физические образцы и информацию, которую они содержат. [22] Исландское законодательство гласит, что правительство Исландии имеет право опеки над самими физическими образцами, в то время как доноры сохраняют права собственности. [22] Напротив, Тонга и Эстония передают право собственности на образцы биобанка правительству, но их законы включают в себя надежную защиту прав доноров. [22]
Ключевое событие, которое возникает в биобанкинге, происходит, когда исследователь хочет собрать человеческий образец для исследования. Когда это происходит, возникают некоторые вопросы, в том числе: право на конфиденциальность для участников исследования , право собственности на образец и полученные из него данные, степень, в которой донор может участвовать в возврате результатов исследования , и степень, в которой донор может дать согласие на участие в исследовании. [23]
Что касается согласия, то основная проблема заключается в том, что биобанки обычно собирают образцы и данные для многочисленных будущих исследовательских целей, и невозможно получить конкретное согласие для всех возможных будущих исследований. Обсуждалось, что одноразовое согласие или широкое согласие для различных исследовательских целей может быть недостаточным для этических и правовых требований. [24] [25] Динамическое согласие — это подход к согласию, который может лучше подходить для биобанкинга, поскольку он обеспечивает постоянное взаимодействие и коммуникацию между исследователями и донорами образцов/данных с течением времени.
Не существует международно признанного набора руководящих принципов управления, разработанных для работы с биобанками. Биобанки обычно пытаются адаптироваться к более широким рекомендациям, которые приняты на международном уровне для исследований с участием людей, и изменяют руководящие принципы по мере их обновления. Для многих типов исследований, и особенно медицинских исследований, надзор осуществляется на местном уровне институциональным наблюдательным советом . Институциональные наблюдательные советы обычно обеспечивают соблюдение стандартов, установленных правительством своей страны. В разной степени закон, используемый разными странами, часто смоделирован на основе рекомендаций по управлению биобанками, которые были предложены на международном уровне.
Вот несколько примеров организаций, которые участвовали в создании письменных руководств по биобанкингу: [2] Всемирная медицинская ассоциация , Совет международных организаций медицинских наук , Совет Европы , Организация по геному человека , Всемирная организация здравоохранения и ЮНЕСКО . Международное общество биологических и экологических репозиториев (ISBER) — это глобальная организация биобанкинга, которая создает возможности для сетевого взаимодействия, образования и инноваций, а также гармонизирует подходы к решению возникающих проблем в биологических и экологических репозиториях. ISBER объединяет репозитории по всему миру с помощью передового опыта. Четвертое издание «Передовых практик ISBER» было выпущено 31 января 2018 года вместе с дополнением LN2, выпущенным в начале мая 2019 года. [26]
В 1998 году исландский парламент принял Закон о базе данных сектора здравоохранения . Этот закон позволил создать национальный биобанк в этой стране. В 1999 году Национальная консультативная комиссия по биоэтике США опубликовала отчет, содержащий рекомендации по политике обращения с биологическими образцами человека. [11] В 2005 году Национальный институт рака США основал Управление биохранилищ и исследований биологических образцов , чтобы иметь подразделение для создания общей базы данных и стандартных операционных процедур для своих партнерских организаций с коллекциями биологических образцов. [11] В 2006 году Совет Европейского союза принял политику в отношении биологических образцов человека, которая была новаторской для обсуждения вопросов, уникальных для биобанков. [11]
Исследователи призвали к более критическому изучению экономических аспектов биобанков, особенно тех, которые поддерживаются государством. [27] Национальные биобанки часто финансируются государственно-частными партнерствами, при этом финансирование предоставляется любой комбинацией национальных исследовательских советов, медицинских благотворительных организаций, инвестиций фармацевтических компаний и биотехнологического венчурного капитала. [28] Таким образом, национальные биобанки обеспечивают экономические отношения, опосредованные между государствами, национальным населением и коммерческими организациями. Было показано, что в основе систематического сбора тканевого материала лежит сильный коммерческий стимул. Это можно увидеть, в частности, в области геномных исследований, где исследование на уровне популяции легче поддается диагностическим технологиям, чем базовым этиологическим исследованиям. [29] Учитывая потенциал существенной прибыли, исследователи Митчелл и Уолдби [27] утверждают, что, поскольку биобанки регистрируют большое количество национального населения в качестве продуктивных участников, которые позволяют своим телам и перспективным историям болезни создавать ресурс с коммерческим потенциалом, их вклад следует рассматривать как форму «клинического труда», и поэтому участники также должны получать экономическую выгоду.
Были случаи, когда право собственности на хранящиеся человеческие образцы оспаривалось и передавалось в суд. Некоторые случаи включают: