Карбораны (или карббораны) представляют собой электронно-делокализованные (неклассически связанные) кластеры, состоящие из атомов бора , углерода и водорода . [1] Как и многие родственные гидриды бора , эти кластеры представляют собой полиэдры или фрагменты полиэдров. Карбораны представляют собой один класс гетероборанов . [2]
С точки зрения области применения, карбораны могут иметь от 5 до 14 атомов в каркасе клетки. Большинство имеют два атома углерода в клетке. Соответствующие C - алкильные и B - алкильные аналоги также известны в нескольких случаях.
Карбораны и бораны принимают 3-мерную геометрию клетки ( кластера ), резко контрастирующую с типичными органическими соединениями. Клетки совместимы с сигма-делокализованной связью, тогда как углеводороды обычно представляют собой цепи или кольца.
Как и для других электронно-делокализованных полиэдрических кластеров, электронная структура этих кластерных соединений может быть описана правилами Уэйда-Мингоса . Как и родственные гидриды бора , эти кластеры являются полиэдрами или фрагментами полиэдров и аналогично классифицируются как клозо- , нидо- , арахно- , гифо- , гиперклозо- , изо- , кладо- , конъюнкто- и мегало- , в зависимости от того, представляют ли они полный ( клозо- ) полиэдр или полиэдр, в котором отсутствует одна ( нидо- ), две ( арахно- ), три ( гифо- ) или более вершин. Карбораны являются ярким примером гетероборанов . [2] [3] Суть этих правил заключается в том, что они подчеркивают делокализованную, многоцентровую связь для взаимодействий BB, CC и BC.
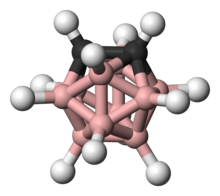
Структурно их можно считать родственными икосаэдрическому ( I h ) [ B 12 H 12 ] 2− посредством формальной замены двух его фрагментов BH − на CH.
Геометрические изомеры карборанов могут существовать на основе различных положений углерода в клетке. Изомеры требуют использования числовых префиксов в названии соединения. Клозо -дикарбадекаборан может существовать в трех изомерах: 1,2-, 1,7- и 1,12- C 2 B 10 H 12 .
Карбораны были получены многими способами, наиболее распространенным из которых является добавление алкинильных реагентов к кластерам гидрида бора с образованием диуглеродных карборанов. По этой причине подавляющее большинство карборанов имеют две углеродные вершины.
Монокарбораны представляют собой кластеры с клетками B n C. Производная с 12 вершинами изучена лучше всего, но известно несколько.
Обычно их готовят добавлением одноуглеродных реагентов к кластерам гидрида бора. Одноуглеродные реагенты включают цианид , изоцианиды и формальдегид . Например, монокарбадодекаборат ( [CB 11 H 12 ] − ) получают из декаборана и формальдегида с последующим добавлением диметилсульфида борана . [4] [5] Монокарбораны являются предшественниками слабо координирующих анионов . [6]
Дикарбобораны могут быть получены из гидридов бора с использованием алкинов в качестве источника двух углеродных центров. В дополнение к упомянутой выше серии клозо - C 2 B n H n +2 известны несколько видов диуглерода с открытой клеткой, включая нидо - C 2 B 3 H 7 (изоструктурный и изоэлектронный с B 5 H 9 ) и арахно - C 2 B 7 H 13 .
Синтезы производных икосаэдрического клозо -дикарбододекаборана ( R 2 C 2 B 10 H 10 ) используют алкины в качестве источника R 2 C 2 и декаборан ( B 10 H 14 ) для получения звена B 10 .
Следующая классификация адаптирована из книги Граймса о карборанах. [1]
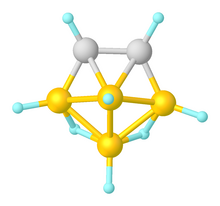
Это семейство кластеров включает нидо-клетки CB 5 H 9 , C 2 B 4 H 8 , C 3 B 3 H 7 , C 4 B 2 H 6 и C 2 B 3 H 7 . Этим соединениям посвящено сравнительно мало работ. Пентаборан[9] реагирует с ацетиленом, давая нидо -1,2- C 2 B 4 H 8 . При обработке гидридом натрия последний образует соль [1,2- C 2 B 4 H 7 ] − Na + .
Это семейство кластеров включает клозо-клетки C 2 B 3 H 5 , C 2 B 4 H 6 , C 2 B 5 H 7 и CB 5 H 7 . Это семейство кластеров также мало изучено из-за синтетических трудностей. Также отражая синтетические трудности, многие из этих соединений наиболее известны как их алкильные производные. 1,5- C 2 B 3 H 5 является единственным известным изомером пятивершинной клетки. Он получается из реакции пентаборана (9) с ацетиленом в две операции, начиная с конденсации с ацетиленом с последующим пиролизом (крекингом) продукта:

Это семейство кластеров включает клозо-клетки C 2 B 6 H 8 , C 2 B 7 H 9 , C 2 B 8 H 10 и C 2 B 9 H 11 и их производные. Изомерия хорошо известна в этом семействе:
Карбораны промежуточной ядерности наиболее эффективно генерируются путем деградации из более крупных кластеров. Напротив, меньшие карбораны обычно получаются путем построения маршрутов, например, из пентаборана + алкина и т. д. Например, орто-карборан может быть деградирован с получением [C 2 B 9 H 12 ] − , [9] который можно манипулировать с помощью окислителей, протонирования и термолиза.
Окисление хроматом 11-вершинных кластеров приводит к деборированию, давая C 2 B 7 H 13 . Из этого вида другие кластеры получаются путем пиролиза, иногда в присутствии диборана : C 2 B 6 H 8 , C 2 B 8 H 10 и C 2 B 7 H 9 . [1]
В общем, изомеры, имеющие несмежные атомы углерода в клетке, более термически стабильны, чем те, у которых атомы углерода соседние. Таким образом, нагревание имеет тенденцию вызывать взаимное разделение атомов углерода в каркасе.
Икосаэдрические нейтральные по заряду клозо -карбораны, 1,2-, 1,7- и 1,12- C 2 B 10 H 12 (неофициально орто- , мета- и пара -карбораны) особенно стабильны и коммерчески доступны. [10] [11] Орто -карборан образуется первым при реакции декаборана и ацетилена. Он количественно превращается в мета-карборан при нагревании в инертной атмосфере. Получение мета-карборана из орто-карборана требует 700 °C, выход составляет около 25%. [1]
[CB 11 H 12 ] − также хорошо известен.
Металлирование карборанов иллюстрируется реакциями клозо - C 2 B 3 H 5 с источниками карбонила железа. Получаются два клозо Fe- и Fe 2 -содержащих продукта, согласно этим идеализированным уравнениям:
Вызванная основанием деградация карборанов дает анионные нидопроизводные , которые также могут быть использованы в качестве лигандов для переходных металлов, генерируя металлакарбораны , которые являются карборанами , содержащими один или несколько атомов переходного металла или металла основной группы в каркасе клетки. Наиболее известными являются дикарболлиды , комплексы с формулой M2 + [ C2B9H11 ] 2− , где M обозначает металл . [12]
Комплексы дикарболлида исследовались в течение многих лет, но коммерческое применение встречается редко. Бис(дикарболлид) [Co(C 2 B 9 H 11 ) 2 ] − использовался в качестве осадителя для удаления 137 Cs + из радиоактивных отходов . [13]
Были изучены медицинские применения карборанов. [14] [15] C - функционализированные карбораны представляют собой источник бора для бор-нейтронной захватной терапии . [16]
Соединение H(CHB 11 Cl 11 ) является суперкислотой , образующей изолируемую соль с протонированным катионом бензола , [C 6 H 7 ] + (катион бензола). [17] Формула этой соли - [C 6 H 7 ] + [CHB 11 Cl 11 ] − . Суперкислота протонирует фуллерен , C 60 . [18]