Спиновые состояния при описании координационных комплексов переходных металлов относятся к потенциальным спиновым конфигурациям d-электронов центрального металла. Для нескольких степеней окисления металлы могут принимать высокоспиновые и низкоспиновые конфигурации. Эта двусмысленность применима только к металлам первого ряда, поскольку металлы второго и третьего ряда неизменно низкоспиновые. Эти конфигурации можно понять с помощью двух основных моделей, используемых для описания координационных комплексов; теория кристаллического поля и теория поля лигандов (более продвинутая версия, основанная на теории молекулярных орбиталей ). [1]

Δ -расщепление d- орбиталей играет важную роль в электронном спиновом состоянии координационного комплекса. На Δ влияют три фактора: период (строка в периодической таблице) иона металла, заряд иона металла и напряженность поля лигандов комплекса, описываемых спектрохимическим рядом . Только октаэдрические комплексы переходных металлов первого ряда принимают высокоспиновые состояния.
Чтобы произошло низкоспиновое расщепление, энергетические затраты на размещение электрона на уже одиночно занятой орбитали должны быть меньше, чем стоимость размещения дополнительного электрона на, например, g- орбитали с энергетической стоимостью Δ. Если энергия, необходимая для спаривания двух электронов, превышает энергетические затраты на размещение электрона, например , Δ, происходит сильное спиновое расщепление.
Если расстояние между орбиталями велико, то нижние энергетические орбитали полностью заполняются до заселения высших орбиталей в соответствии с принципом Ауфбау . Такие комплексы называются «низкоспиновыми», поскольку заполнение орбитали соответствует электронам и уменьшает общий спин электронов. Если расстояние между орбиталями достаточно мало, то легче поместить электроны на орбитали с более высокой энергией, чем поместить два электрона на одну и ту же орбиталь с низкой энергией, из-за отталкивания, возникающего в результате совпадения двух электронов на одной и той же орбитали. Таким образом, в соответствии с правилом Хунда по одному электрону помещается на каждую из пяти d- орбиталей, прежде чем произойдет какое-либо спаривание , в результате чего образуется так называемый «высокоспиновый» комплекс. Такие комплексы называются «высокоспиновыми», поскольку заселение верхней орбитали позволяет избежать совпадений между электронами с противоположным спином.

Заряд металлоцентра играет роль в лигандном поле и Δ-расщеплении. Чем выше степень окисления металла, тем сильнее создается поле лигандов. В случае, если есть два металла с одинаковой d-электронной конфигурацией, тот, у которого более высокая степень окисления, скорее всего, будет низкоспиновым, чем тот, у которого более низкая степень окисления; например, Fe 2+ и Co 3+ оба представляют собой d 6 ; однако более высокий заряд Co 3+ создает более сильное поле лиганда, чем Fe 2+ . При прочих равных условиях Fe 2+ скорее будет высокоспиновым, чем Co 3+ .
Лиганды также влияют на величину Δ-расщепления d - орбиталей в зависимости от напряженности их поля, как это описывается спектрохимическим рядом . Лиганды сильного поля, такие как CN - и CO, увеличивают Δ-расщепление и с большей вероятностью будут низкоспиновыми. Лиганды слабого поля, такие как I - и Br -, вызывают меньшее Δ-расщепление и с большей вероятностью будут высокоспиновыми.
Некоторые октаэдрические комплексы демонстрируют спиновый кроссовер , где существуют состояния с высоким и низким спином, что является динамическим равновесием.

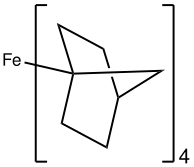
Энергия расщепления Δ для тетраэдрических металлокомплексов (четыре лиганда), Δtet, меньше , чем для октаэдрического комплекса. Следовательно, тетраэдрические комплексы почти всегда являются высокоспиновыми [3] . Примеры низкоспиновых тетраэдрических комплексов включают Fe(2-норборнил) 4 , [4] [Co(4-норборнил) 4 ] + и нитрозильный комплекс Cr(NO)( (Н(тмс) 2 ) 3 .
Многие d 8 -комплексы металлов первого ряда существуют в тетраэдрической или плоско-квадратной геометрии. В некоторых случаях эти геометрии существуют в измеримых состояниях равновесия. Например, дихлорбис(трифенилфосфин)никель(II) кристаллизовался как в тетраэдрической, так и в плоско-квадратной геометрии. [5]
Что касается расщепления d-орбиталей, теория поля лигандов (LFT) и теория кристаллического поля (CFT) дают аналогичные результаты. CFT — более старая и простая модель, в которой лиганды рассматриваются как точечные заряды. LFT более химичен, подчеркивает ковалентную связь и явно учитывает пи-связь.
В случае октаэдрических комплексов вопрос о высоком спине или низком спине сначала возникает для d 4 , поскольку он имеет более трех электронов для заполнения несвязывающих d-орбиталей согласно теории поля лигандов или стабилизированных d-орбиталей согласно кристаллической теории. разделение полей.
Все комплексы металлов второго и третьего рядов низкоспиновые.
Спиновое состояние комплекса влияет на ионный радиус атома . При данном количестве d-электронов высокоспиновые комплексы больше. [7]
Как правило, скорости диссоциации лигандов из низкоспиновых комплексов ниже, чем скорости диссоциации из высокоспиновых комплексов. В случае октаэдрических комплексов электроны на eg- уровнях являются разрыхляющими по отношению к связям металл-лиганд. Известные «обменные инертные» комплексы представляют собой октаэдрические комплексы d 3 и низкоспиновых ионов металлов d 6 , проиллюстрированные соответственно Cr 3+ и Co 3+ . [8]