Генотоксичность – это свойство химических агентов, которые повреждают генетическую информацию внутри клетки, вызывая мутации , которые могут привести к раку . Хотя генотоксичность часто путают с мутагенностью , все мутагены генотоксичны, но некоторые генотоксичные вещества не являются мутагенными. Изменение может иметь прямое или косвенное воздействие на ДНК: индукция мутаций, несвоевременная активация событий и прямое повреждение ДНК, приводящее к мутациям. Постоянные наследственные изменения могут затрагивать как соматические клетки организма, так и половые клетки и передаваться будущим поколениям. [1] Клетки предотвращают проявление генотоксической мутации либо путем восстановления ДНК , либо путем апоптоза ; однако повреждение не всегда может быть устранено, что приводит к мутагенезу .
Чтобы определить генотоксичные молекулы, исследователи исследуют повреждение ДНК в клетках, подвергшихся воздействию токсичных субстратов. Это повреждение ДНК может проявляться в форме одно- и двухцепочечных разрывов, потери эксцизионной репарации, перекрестных связей, щелочелабильных участков, точечных мутаций, а также структурных и числовых хромосомных аберраций. [2] Известно, что нарушение целостности генетического материала может вызывать рак. Как следствие, было разработано множество сложных методов, включая анализ Эймса, токсикологические тесты in vitro и in vivo , а также анализ комет, для оценки способности химических веществ вызывать повреждение ДНК, которое может привести к раку.
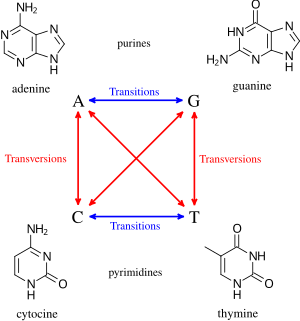
Генотоксичные вещества вызывают повреждение генетического материала в клетках посредством взаимодействия с последовательностью и структурой ДНК. Например, переходный металл хром взаимодействует с ДНК в высоковалентной степени окисления, вызывая повреждения ДНК, которые приводят к канцерогенезу . Метастабильная степень окисления Cr(V) достигается за счет восстановительной активации. Исследователи провели эксперимент по изучению взаимодействия ДНК с канцерогенным хромом, используя комплекс Cr(V)-Сален в определенной степени окисления. [3] Взаимодействие было специфичным для гуанинового нуклеотида в генетической последовательности. Чтобы сузить взаимодействие комплекса Cr(V)-сален с основанием гуанина, исследователи модифицировали основания до 8-оксо-G, чтобы обеспечить сайт-специфическое окисление. Реакция между двумя молекулами вызвала повреждение ДНК; два повреждения, наблюдаемые в модифицированном базовом участке, представляли собой гуанидиногидантоин и спироиминодигидантоин. При дальнейшем анализе места повреждения было замечено, что полимераза остановилась на этом месте, и аденин был неправильно включен в последовательность ДНК, противоположную основанию 8-оксо-G. Следовательно, эти поражения преимущественно содержат трансверсии G-->T . Считается, что высоковалентный хром действует как канцероген, поскольку исследователи обнаружили, что «механизм повреждения и продукты окисления оснований для взаимодействия между высоковалентным хромом и ДНК... имеют отношение к образованию повреждений ДНК in vivo , приводящих к раку у людей». человеческие популяции, подвергшиеся воздействию хромата». [3] Следовательно, это показывает, как высоковалентный хром может действовать как канцероген, образуя ксенобиотики 8-оксо-G . [3]
Другим примером генотоксичного вещества, вызывающего повреждение ДНК, являются пирролизидиновые алкалоиды (ПА). Эти вещества встречаются главным образом в растениях и ядовиты для животных, в том числе для человека; около половины из них были идентифицированы как генотоксичные, а многие — как канцерогенные. В результате тестирования исследователи пришли к выводу, что при метаболической активации «PA производят аддукты ДНК, сшивку ДНК, разрывы ДНК, обмен сестринских хроматид, микроядра, хромосомные аберрации, генные и хромосомные мутации in vivo и in vitro ». [4] Наиболее распространенными мутациями внутри генов являются трансверсии G:C --> T:A и тандемная замена оснований. Пирролизидиновые алкалоиды обладают мутагенным действием in vivo и in vitro и, следовательно, ответственны за канцерогенез, главным образом в печени. [4] Окопник является примером вида растений, который содержит четырнадцать различных ПА. Активные метаболиты взаимодействуют с ДНК, вызывая повреждение ДНК, индукцию мутаций и развитие рака в эндотелиальных клетках печени и гепатоцитах . В конце концов исследователи обнаружили, что «окопник оказывает мутагенное действие на печень, а ПА, содержащийся в окопнике, по-видимому, ответственен за токсичность, вызванную окопником, и индукцию опухолей». [5]
Целью испытаний на генотоксичность является определение того, будет ли субстрат влиять на генетический материал или может ли вызвать рак. Их можно проводить в клетках бактерий, дрожжей и млекопитающих. [2] Благодаря знаниям, полученным в результате испытаний, можно контролировать раннее развитие уязвимых организмов к генотоксичным веществам. [1]
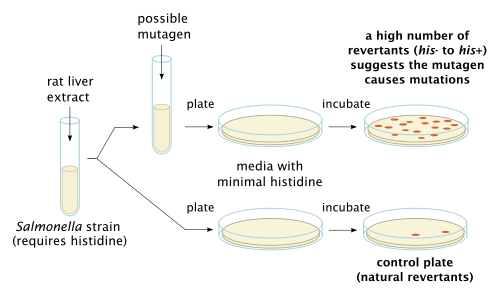
Анализ обратной мутации бактерий, также известный как анализ Эймса , используется в лабораториях для проверки мутаций генов. В этом методе используется множество различных бактериальных штаммов для сравнения различных изменений в генетическом материале. Результат теста обнаруживает большинство генотоксичных канцерогенов и генетических изменений; Типами обнаруженных мутаций являются сдвиги рамки и замены оснований. [6]
Целью тестирования in vitro является определение того, вызывают ли субстрат, продукт или фактор окружающей среды генетические повреждения. Один метод предполагает цитогенетические анализы с использованием различных клеток млекопитающих. [6] Типами аберраций , обнаруживаемых в клетках, подвергшихся воздействию генотоксичного вещества, являются разрывы хроматид и хромосом, разрывы хромосом, делеции хроматид, фрагментация, транслокация, сложные перестройки и многие другие. Кластогенные или аевгенные эффекты генотоксического повреждения вызовут увеличение частоты структурных или числовых аберраций генетического материала . [6] Это похоже на микроядерный тест и анализ хромосомных аберраций, которые выявляют структурные и численные хромосомные аберрации в клетках млекопитающих. [1]
В конкретной ткани млекопитающего можно провести анализ TK+/- лимфомы мыши , чтобы проверить изменения в генетическом материале. [6] Генные мутации обычно представляют собой точечные мутации, изменяющие только одно основание в генетической последовательности с целью изменения последующего транскрипта и аминокислотной последовательности; эти точечные мутации включают замены оснований, делеции, сдвиги рамки и перестановки. Кроме того, целостность хромосом может быть изменена за счет потери хромосом и кластогенных поражений , вызывающих множественные делеции генов и мультилокусов. Конкретный тип повреждения определяется размером колоний, различая генетические мутации (мутагены) и хромосомные аберрации (кластогены). [6]
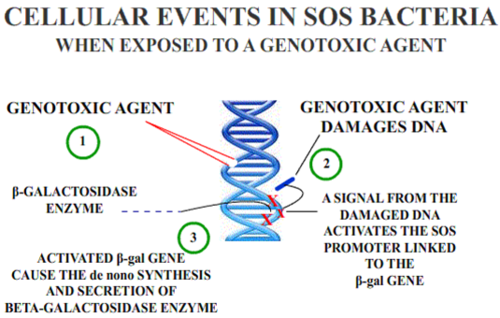
Тест SOS/umu оценивает способность вещества вызывать повреждение ДНК; он основан на изменениях индукции SOS-ответа из-за повреждения ДНК. Преимущества этого метода заключаются в том, что это быстрый и простой метод, удобный для многих веществ. Эти методы выполняются на воде и сточных водах окружающей среды. [7]
Целью тестирования in vivo является определение возможности повреждения ДНК, которое может повлиять на структуру хромосом или нарушить митотический аппарат , изменяющий число хромосом; Факторами, которые могут влиять на генотоксичность, являются ADME и репарация ДНК. Он также может обнаруживать генотоксические агенты, пропущенные в тестах in vitro . Положительным результатом индуцированного хромосомного повреждения является увеличение частоты микроядерных PCE. [6] Микроядро — это небольшая структура, отдельная от ядра, содержащая ядерную ДНК, возникшую из фрагментов ДНК или целых хромосом, которые не были включены в дочернюю клетку во время митоза . Причинами такой структуры являются митотическая потеря ацентрических хромосомных фрагментов (кластогенность), механические проблемы, связанные с разрушением и обменом хромосом, митотическая потеря хромосом (анегенность) и апоптоз. Микроядерный тест in vivo аналогичен тесту in vitro , поскольку он проверяет структурные и числовые хромосомные аберрации в клетках млекопитающих, особенно в клетках крови крыс. [6]
Анализы комет являются одним из наиболее распространенных тестов на генотоксичность. Этот метод включает лизис клеток с использованием детергентов и солей. ДНК, высвобождаемая из лизированной клетки, подвергается электрофорезу в агарозном геле в условиях нейтрального pH. Клетки, содержащие ДНК с повышенным количеством двухцепочечных разрывов, будут быстрее мигрировать к аноду. Преимущество этого метода заключается в том, что он обнаруживает низкие уровни повреждений ДНК, требует лишь очень небольшого количества клеток, дешевле, чем многие методы, прост в исполнении и быстро отображает результаты. Однако он не определяет механизм, лежащий в основе генотоксического эффекта, или точный химический или химический компонент, вызывающий нарушения. [8]
Генотоксические эффекты, такие как делеции, разрывы и/или перестройки, могут привести к раку, если повреждение не приводит немедленно к гибели клеток. Области, чувствительные к поломке, называемые хрупкими участками , могут быть результатом воздействия генотоксичных агентов (таких как пестициды). Некоторые химические вещества обладают способностью индуцировать хрупкие участки в участках хромосомы, где присутствуют онкогены , что может привести к канцерогенным эффектам. В соответствии с этим выводом, профессиональное воздействие некоторых смесей пестицидов положительно коррелирует с увеличением генотоксического ущерба у подвергшихся воздействию людей. Повреждения ДНК неодинаковы по степени тяжести в разных популяциях, поскольку люди различаются по своей способности активировать или детоксицировать генотоксические вещества, что приводит к вариабельности заболеваемости раком среди людей. Разница в способности детоксикации определенных соединений обусловлена унаследованным полиморфизмом генов, участвующих в метаболизме химического вещества. Различия также можно объяснить индивидуальными различиями в эффективности механизмов репарации ДНК [9].
Метаболизм некоторых химических веществ приводит к образованию активных форм кислорода ( АФК), что является возможным механизмом генотоксичности. Это видно по метаболизму мышьяка , который производит гидроксильные радикалы , которые, как известно, вызывают генотоксические эффекты. [10] Аналогично, АФК вовлечены в генотоксичность, вызванную частицами и волокнами. Генотоксичность неволокнистых и волокнистых частиц характеризуется высокой продукцией АФК воспалительными клетками . [11]
Выявлены основные генотоксические агенты, ответственные за четыре наиболее распространенных рака во всем мире (легких, молочной железы, толстой кишки и желудка).
Рак легких является наиболее частым раком в мире как по числу ежегодных случаев (1,61 миллиона случаев; 12,7% всех случаев рака), так и по смертности (1,38 миллиона смертей; 18,2% всех смертей от рака). [12] Табачный дым является основной причиной рака легких. Оценки риска рака легких показывают, что табачный дым является причиной 90% случаев рака легких в Соединенных Штатах. Табачный дым содержит более 5300 идентифицированных химических веществ. Наиболее значимые канцерогены в табачном дыме были определены с помощью подхода «Граница воздействия». [13] Согласно этому подходу, канцерогенными соединениями в табачном дыме были в порядке значимости акролеин , формальдегид , акрилонитрил , 1,3-бутадиен , кадмий , ацетальдегид , оксид этилена и изопрен . В целом эти соединения генотоксичны и вызывают повреждение ДНК. В качестве примеров сообщалось о повреждающем ДНК воздействии акролеина, [14] формальдегида, [15] и акрилонитрила. [16]
Рак молочной железы является вторым по распространенности раком в мире в годовом исчислении [(1,38 миллиона случаев, 10,9% всех случаев рака) и занимает 5-е место по причине смертности (458 000, 6,1% всех случаев смерти от рака)]. [12] Риск рака молочной железы связан с постоянно высоким уровнем эстрогена в крови . [17] Эстроген, вероятно, способствует канцерогенезу молочной железы посредством следующих трех процессов; (1) метаболическое преобразование эстрогена в генотоксичные, мутагенные канцерогены, (2) стимуляция роста тканей и (3) репрессия ферментов детоксикации фазы II , которые метаболизируют генотоксичные активные формы кислорода , что приводит к увеличению окислительного повреждения ДНК. [18] [19] [20] Основной человеческий эстроген, эстрадиол , может метаболизироваться до хиноновых производных, которые образуют аддукты ДНК . [21] Эти производные могут вызывать удаление оснований из фосфодиэфирного остова ДНК (например, депуринирование ). За этим удалением может последовать неточное восстановление или репликация апуринового сайта, что приводит к мутации и, в конечном итоге, к раку.
Колоректальный рак является третьим по распространенности видом рака в мире [1,23 миллиона случаев (9,7% всех случаев рака), 608 000 смертей (8,0% всех случаев смерти от рака)]. [12] В Соединенных Штатах табачный дым может быть причиной до 20% случаев колоректального рака. [22] Кроме того, согласно убедительным доказательствам, желчные кислоты являются важным генотоксическим фактором при раке толстой кишки. [23] В частности, желчная кислота дезоксихолевая кислота вызывает выработку повреждающих ДНК активных форм кислорода в эпителиальных клетках толстой кишки человека и грызунов. [23]
Рак желудка является четвертым по распространенности видом рака в мире [990 000 случаев (7,8% всех случаев рака), 738 000 смертей (9,7% всех случаев смерти от рака)]. [12] Инфекция Helicobacter pylori является основным причинным фактором рака желудка. Хроническое воспаление, вызванное H. pylori , если его не лечить, часто бывает длительным. Инфекция H. pylori эпителиальных клеток желудка вызывает повышенное производство генотоксичных активных форм кислорода (АФК). [24] [25] АФК вызывают окислительное повреждение ДНК, которое включает изменение основного основания 8-оксо-2'-дезоксигуанозина . В недавнем ретроспективном исследовании было обнаружено, что использование секвестрантов желчных кислот было связано со значительным снижением риска рака желудка, что позволяет предположить, что желчные кислоты могут быть фактором, способствующим развитию рака желудка. [26]
Генотоксическая химиотерапия – это лечение рака с использованием одного или нескольких генотоксичных препаратов. Лечение традиционно является частью стандартизированного режима . Используя разрушительные свойства генотоксинов, лечение направлено на повреждение ДНК раковых клеток. Любой ущерб, нанесенный раку, передается потомкам раковых клеток по мере продолжения пролиферации . Если это повреждение достаточно серьезное, оно заставит клетки подвергнуться апоптозу . [27]
Недостатком лечения является то, что многие генотоксичные препараты одинаково эффективны как на раковые, так и на нормальные клетки. Избирательность действия того или иного препарата основана на чувствительности самих клеток. Таким образом, хотя быстро делящиеся раковые клетки особенно чувствительны ко многим медикаментозным препаратам, часто поражаются нормально функционирующие клетки. [27]
Другой риск лечения заключается в том, что многие лекарства не только генотоксичны, но и обладают мутагенными и цитотоксичными свойствами . Таким образом, действие этих препаратов не ограничивается только повреждением ДНК. Кроме того, некоторые из этих препаратов, предназначенных для лечения рака, сами по себе являются канцерогенами , что повышает риск возникновения вторичного рака, такого как лейкемия . [27]
В этой таблице показаны различные методы лечения рака, основанные на генотоксичности, а также примеры. [27]
Генотоксическое повреждение ДНК в почках связано как с острым, так и с хроническим повреждением почек , а также с почечно-клеточным раком . [28] Исследования людей с генетическими нарушениями путей восстановления ДНК показали, что их почки особенно уязвимы к повреждениям ДНК, таким как перекрестные связи ДНК, разрывы ДНК и повреждения, блокирующие транскрипцию. [28]