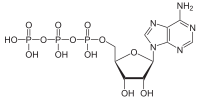
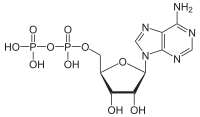

Гидролиз АТФ — это процесс катаболической реакции, при котором химическая энергия , запасенная в высокоэнергетических фосфоангидридных связях в аденозинтрифосфате (АТФ), высвобождается после расщепления этих связей, например, в мышцах , производя работу в форме механической энергии . Продукт представляет собой аденозиндифосфат (ADP) и неорганический фосфат (P i ). АДФ может подвергаться дальнейшему гидролизу с получением энергии, аденозинмонофосфата (АМФ) и другого неорганического фосфата (P i ). [1] Гидролиз АТФ является последним связующим звеном между энергией, полученной из пищи или солнечного света, и полезной работой, такой как сокращение мышц , создание электрохимических градиентов через мембраны и биосинтетические процессы, необходимые для поддержания жизни.
Ангидридные связи часто называют « высокоэнергетическими связями» . Связи PO на самом деле довольно прочны (на ~ 30 кДж/моль прочнее, чем связи CN) [2] [3] , и их не так-то легко разорвать. Как отмечено ниже, энергия выделяется при гидролизе АТФ. Однако когда связи ПО разрываются, требуется затрата энергии. Именно образование новых связей и более низкоэнергетического неорганического фосфата с выделением большего количества энергии снижает общую энергию системы и делает ее более устойчивой. [1]
Гидролиз фосфатных групп в АТФ является особенно экзергоническим , поскольку образующийся неорганический молекулярный ион фосфата в значительной степени стабилизируется множеством резонансных структур , в результате чего продукты (АДФ и Pi ) имеют более низкую энергию, чем реагент (АТФ). Высокая плотность отрицательного заряда, связанная с тремя соседними фосфатными единицами АТФ, также дестабилизирует молекулу, увеличивая ее энергию. Гидролиз снимает некоторые из этих электростатических отталкиваний, высвобождая полезную энергию в процессе, вызывая конформационные изменения в структуре фермента.
У людей примерно 60 процентов энергии, выделяемой при гидролизе АТФ, производит метаболическое тепло, а не питает текущие реакции. [4] Благодаря кислотно-основным свойствам АТФ, АДФ и неорганического фосфата гидролиз АТФ приводит к снижению pH реакционной среды. При определенных условиях высокий уровень гидролиза АТФ может способствовать лактоацидозу .
Гидролиз концевой фосфоангидридной связи представляет собой высокоэкзергонический процесс. Количество выделяемой энергии зависит от условий в конкретной клетке. В частности, высвобождаемая энергия зависит от концентрации АТФ, АДФ и Pi . По мере отклонения концентраций этих молекул от равновесных значений величина изменения свободной энергии Гиббса (ΔG ) будет все больше отличаться. В стандартных условиях (концентрации АТФ, АДФ и P i равны 1 М, концентрация воды равна 55 М) значение Δ G находится в пределах от -28 до -34 кДж/моль. [5] [6]
Диапазон значений ΔG существует потому, что эта реакция зависит от концентрации катионов Mg2 + , которые стабилизируют молекулу АТФ. Клеточная среда также способствует различиям в величине ΔG, поскольку гидролиз АТФ зависит не только от исследуемой клетки, но и от окружающей ткани и даже от компартмента внутри клетки. Поэтому следует ожидать изменчивости значений Δ G. [6]
Показательна связь между стандартным изменением свободной энергии Гиббса Δ r G o и химическим равновесием. Эта связь определяется уравнением Δr G o = - RT ln( K ), где K – константа равновесия , равная коэффициенту реакции Q в равновесии. Стандартное значение ΔG для этой реакции, как уже упоминалось, находится между -28 и -34 кДж/моль; однако экспериментально определенные концентрации участвующих молекул показывают, что реакция не находится в равновесии. [6] Учитывая этот факт, сравнение константы равновесия K и коэффициента реакции Q дает понимание. К учитывает реакции, протекающие в стандартных условиях, но в клеточной среде концентрации участвующих молекул (а именно АТФ, АДФ и Р i ) далеки от стандартного 1 М. На самом деле концентрации правильнее измерять в мм, что на три порядка меньше М. [6] При использовании этих нестандартных концентраций расчетное значение Q оказывается намного меньше единицы. Связывая Q с Δ G с помощью уравнения Δ G = Δ r G o + RT ln( Q ), где Δ r G o - стандартное изменение свободной энергии Гиббса для гидролиза АТФ, обнаруживают, что величина Δ G намного превышает стандартное значение. Нестандартные условия клетки на самом деле приводят к более благоприятной реакции. [7]
В одном конкретном исследовании для определения ΔG in vivo у людей концентрацию АТФ, АДФ и Pi измеряли с помощью ядерного магнитного резонанса. [6] Было обнаружено, что в мышечных клетках человека в состоянии покоя концентрация АТФ составляет около 4 мкМ, а концентрация АДФ — около 9 мкМ. Ввод этих значений в приведенные выше уравнения дает Δ G = -64 кДж/моль. После ишемии , когда мышца восстанавливается после тренировки, концентрация АТФ составляет всего 1 мкМ, а концентрация АДФ — около 7 мкМ. Следовательно, абсолютная ΔG будет достигать -69 кДж/моль. [8]
Сравнивая стандартное значение ΔG и экспериментальное значение ΔG , можно увидеть, что энергия, выделяющаяся при гидролизе АТФ, измеренная у человека, почти в два раза больше энергии, вырабатываемой в стандартных условиях. [6] [7]
{{cite book}}: CS1 maint: другие ( ссылка )