Ток кардиостимулятора ( I f , или I K f , также называемый забавным током ) представляет собой электрический ток в сердце , который протекает через канал HCN или канал кардиостимулятора. Такие каналы являются важными частями электропроводящей системы сердца и образуют компонент естественного кардиостимулятора .
Впервые описанный в конце 1970-х годов в волокнах Пуркинье и синоатриальных миоцитах , ток кардиостимулятора «funny» (I f ) был подробно охарактеризован, и его роль в кардиостимуляции была исследована. [1] [2] [3] Среди необычных особенностей, которые оправдали название «funny», - смешанная проницаемость для Na + и K + , активация при гиперполяризации и очень медленная кинетика. [1]
Funny current высоко выражен в спонтанно активных областях сердца, таких как синоатриальный узел (SAN, область естественного водителя ритма), атриовентрикулярный узел (AVN) и волокна Пуркинье проводящей ткани. Funny current представляет собой смешанный натрий-калиевый ток, который активируется при гиперполяризации при напряжениях в диастолическом диапазоне (обычно от -60/-70 мВ до -40 мВ). Когда в конце синоатриального потенциала действия мембрана реполяризуется ниже порога I f (около -40/-50 мВ), funny current активируется и подает входящий ток, который отвечает за начало фазы диастолической деполяризации (DD); с помощью этого механизма funny current контролирует скорость спонтанной активности синоатриальных миоцитов и, таким образом, частоту сердечных сокращений. Потенциал реверсии funny current лежит между -20 и -10 мВ. [4]
Другой необычной особенностью I f является его двойная активация напряжением и циклическими нуклеотидами. Молекулы циклического аденозинмонофосфата (цАМФ) напрямую связываются с f-каналами и увеличивают вероятность их открытия. [5] Зависимость от цАМФ является особенно важным физиологическим свойством, поскольку она лежит в основе I f -зависимой автономной регуляции сердечного ритма. Симпатическая стимуляция повышает уровень молекул цАМФ, которые связываются с f-каналами и сдвигают диапазон активации I f в сторону более положительных напряжений; этот механизм приводит к увеличению тока при диастолических напряжениях и, следовательно, к увеличению крутизны DD и ускорению сердечного ритма.
Парасимпатическая стимуляция (которая увеличивает вероятность открытия калиевых каналов, но уменьшает вероятность открытия кальциевых каналов) снижает частоту сердечных сокращений противоположным действием, то есть сдвигая кривую активации I f в сторону более отрицательных напряжений. Когда вагально-высвобождаемый ацетилхолин (ACh) связывается с мускариновыми рецепторами M2 , это способствует диссоциации комплексов субъединиц βγ, что приводит к прямому открытию управляемого G-белком внутреннего выпрямляющего канала K+ (Girk/Kir) IKACh. [6]
Похожий ток, называемый Ih ( активируемый гиперполяризацией), также был описан в различных типах нейронов, где он имеет различные функции, включая участие в контроле ритмической активности, регуляции нейронной возбудимости, сенсорной трансдукции, синаптической пластичности и т. д. [7]
Молекулярные детерминанты тока водителя ритма принадлежат каналу HCN ( гиперполяризационно -активируемый циклический нуклеотид -управляемый канал), из которых известны 4 изоформы (HCN1 до HCN4). На основании их последовательности каналы HCN классифицируются как члены суперсемейства потенциалзависимых каналов K + (Kv) и CNG. [3] [8]
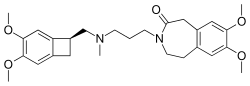
Из-за их значимости для генерации активности водителя ритма и модуляции спонтанной частоты, f-каналы являются естественными мишенями для препаратов, направленных на фармакологический контроль частоты сердечных сокращений. Несколько агентов, называемых «средствами, снижающими частоту сердечных сокращений», действуют путем специфического ингибирования функции f-каналов. [3] Ивабрадин является наиболее специфическим и селективным ингибитором I f и единственным членом этого семейства, который в настоящее время продается для фармакологического лечения хронической стабильной стенокардии у пациентов с нормальным синусовым ритмом, имеющих противопоказания или непереносимость бета-блокаторов. Недавние исследования также показали, что ингибирование забавных каналов может использоваться для снижения частоты исходов ишемической болезни сердца в подгруппе пациентов с частотой сердечных сокращений ≥70 уд/мин. [9]
Сердечно-сосудистые заболевания являются одной из основных причин смертности во всем мире, и значимость генетического компонента в этих заболеваниях в последнее время стала более очевидной. Генетические изменения каналов HCN4 (молекулярный коррелят синоатриальных f-каналов), связанные с нарушениями ритма, были зарегистрированы у людей. Например, наследственная мутация высококонсервативного остатка в CNBD белка HCN4 (S672R) связана с наследственной синусовой брадикардией . [10] Исследования in vitro показывают, что мутация S672R вызывает гиперполяризационный сдвиг кривой вероятности открытия канала HCN4 примерно на 5 мВ при гетерозиготности, эффект, аналогичный гиперполяризационному сдвигу, вызванному парасимпатической стимуляцией, и способный объяснить снижение входящего тока во время диастолы и, как следствие, более медленную спонтанную скорость. [ необходима цитата ]
Биологические кардиостимуляторы, обычно предназначенные как клеточные субстраты, способные вызывать спонтанную активность в молчащей ткани, представляют собой потенциальный инструмент для преодоления ограничений электронных кардиостимуляторов . Одна из стратегий, используемых для создания биологических кардиостимуляторов, включает использование клеток, изначально экспрессирующих или сконструированных для экспрессии забавных каналов. Для этой цели могут использоваться различные типы стволовых клеток. [8]