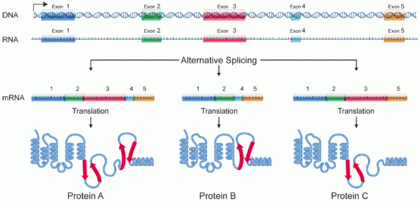
Изоформа белка , или « вариант белка », [1] является членом набора очень похожих белков , которые происходят из одного гена или семейства генов и являются результатом генетических различий. [2] Хотя многие изоформы выполняют одинаковые или схожие биологические роли, некоторые изоформы обладают уникальными функциями. Набор изоформ белка может быть образован путем альтернативного сплайсинга , использования вариабельного промотора или других посттранскрипционных модификаций одного гена; посттрансляционные модификации обычно не учитываются. (Об этом см. Протеоформы .) Благодаря механизмам сплайсинга РНК мРНК обладает способностью выбирать разные сегменты, кодирующие белок ( экзоны ) гена, или даже разные части экзонов РНК для формирования разных последовательностей мРНК. Каждая уникальная последовательность производит определенную форму белка.
Открытие изоформ могло бы объяснить несоответствие между небольшим количеством белково-кодирующих областей генов, выявленных в ходе проекта генома человека, и большим разнообразием белков, наблюдаемых в организме: разные белки, кодируемые одним и тем же геном, могут увеличить разнообразие протеома . Изоформы на уровне РНК легко охарактеризовать с помощью исследований транскриптов кДНК . Многие человеческие гены обладают подтвержденными альтернативными изоформами сплайсинга . Было подсчитано, что у людей можно идентифицировать около 100 000 меток экспрессируемых последовательностей ( EST ). [1] Изоформы на уровне белка могут проявляться в делеции целых доменов или более коротких петель, обычно расположенных на поверхности белка. [3]
Один-единственный ген способен производить множество белков, различающихся как по структуре, так и по составу; [4] [5] этот процесс регулируется альтернативным сплайсингом мРНК, однако неясно, в какой степени такой процесс влияет на разнообразие протеома человека, поскольку обилие изоформ транскриптов мРНК не обязательно коррелирует с обилием изоформ белка. [6] Трехмерное сравнение структуры белков можно использовать, чтобы определить, какие изоформы (если таковые имеются) представляют собой функциональные белковые продукты, а структура большинства изоформ в протеоме человека была предсказана AlphaFold и публично опубликована на isoform.io. [7] Специфичность транслируемых изоформ зависит от структуры/функции белка, а также от типа клеток и стадии развития, на которой они производятся. [4] [5] Определение специфичности становится более сложным, если белок имеет несколько субъединиц и каждая субъединица имеет несколько изоформ.
Например, 5'-AMP-активируемая протеинкиназа (AMPK), фермент, выполняющий различные роли в клетках человека, имеет 3 субъединицы: [8]
В скелетных мышцах человека предпочтительной формой является α2β2γ1. [8] Но в печени человека наиболее распространенной формой является α1β2γ1. [8]

Основными механизмами производства изоформ белка являются альтернативный сплайсинг и использование вариабельных промоторов, хотя модификации, вызванные генетическими изменениями, такими как мутации и полиморфизмы , иногда также считаются отдельными изоформами. [9]
Альтернативный сплайсинг — это основной процесс посттранскрипционной модификации , в результате которого образуются изоформы транскриптов мРНК, и основной молекулярный механизм, который может способствовать разнообразию белков. [5] Сплайсосома , большой рибонуклеопротеин , представляет собой молекулярную машину внутри ядра, ответственную за расщепление и лигирование РНК , удаляя некодирующие белки сегменты ( интроны ). [10]
Поскольку сплайсинг — это процесс, который происходит между транскрипцией и трансляцией , его основные эффекты в основном изучались с помощью методов геномики — например, анализ микрочипов и секвенирование РНК использовались для идентификации альтернативно сплайсированных транскриптов и измерения их численности. [9] Обилие транскриптов часто используется в качестве показателя обилия изоформ белка, хотя протеомные эксперименты с использованием гель-электрофореза и масс-спектрометрии показали, что корреляция между количеством транскриптов и белков часто низкая и что одна изоформа белка обычно является доминантной. [11] В одном исследовании 2015 года говорится, что причина этого несоответствия, вероятно, возникает после перевода, хотя механизм практически неизвестен. [12] Следовательно, хотя альтернативный сплайсинг считается важной связью между изменчивостью и заболеванием, нет убедительных доказательств того, что он действует в первую очередь путем производства новых изоформ белка. [11]
Альтернативный сплайсинг обычно описывает строго регулируемый процесс, в котором альтернативные транскрипты намеренно генерируются с помощью механизма сплайсинга. Однако такие транскрипты также производятся в результате ошибок сплайсинга в процессе, называемом «шумным сплайсингом», и также потенциально транслируются в изоформы белка. Хотя считается, что около 95% мультиэкзонных генов подвергаются альтернативному сплайсингу, одно исследование шумного сплайсинга показало, что большинство различных транскриптов с низким содержанием являются шумовыми, и предсказывает, что большинство альтернативных транскриптов и изоформ белков, присутствующих в клетке, функционально не являются соответствующий. [13]
Другие этапы транскрипционной и посттранскрипционной регуляции также могут производить различные изоформы белка. [14] Использование вариабельного промотора происходит, когда транскрипционный аппарат клетки ( РНК-полимераза , факторы транскрипции и другие ферменты ) начинает транскрипцию на разных промоторах — участке ДНК рядом с геном, который служит начальным сайтом связывания, — что приводит к слегка модифицированному транскрипты и изоформы белков.
Обычно одна изоформа белка помечается как каноническая последовательность на основании таких критериев, как ее распространенность и сходство с ортологичными или функционально аналогичными последовательностями у других видов. [15] Предполагается, что изоформы обладают сходными функциональными свойствами, поскольку большинство из них имеют схожие последовательности и имеют некоторые общие экзоны с канонической последовательностью. Однако некоторые изоформы демонстрируют гораздо большую дивергенцию (например, за счет транс-сплайсинга ) и могут иметь мало общих экзонов или вообще не иметь их с канонической последовательностью. Кроме того, они могут иметь разные биологические эффекты (например, в крайнем случае функция одной изоформы может способствовать выживанию клеток, а другой — гибели клеток) или могут иметь сходные основные функции, но различаться внутриклеточной локализацией. [16] Однако исследование 2016 года функционально охарактеризовало все изоформы 1492 генов и определило, что большинство изоформ ведут себя как «функциональные аллоформы». Авторы пришли к выводу, что изоформы ведут себя как отдельные белки, после того, как заметили, что функциональные возможности большинства изоформ не перекрываются. [17] Поскольку исследование проводилось на клетках in vitro , неизвестно, имеют ли изоформы в экспрессированном протеоме человека эти характеристики. Кроме того, поскольку функцию каждой изоформы обычно необходимо определять отдельно, большинство идентифицированных и предсказанных изоформ все еще имеют неизвестные функции.
Гликоформа — это изоформа белка, которая отличается только количеством или типом присоединенного гликана . Гликопротеины часто состоят из ряда различных гликоформ с изменениями в присоединенном сахариде или олигосахариде . Эти модификации могут быть результатом различий в биосинтезе в процессе гликозилирования или вследствие действия гликозидаз или гликозилтрансфераз . Гликоформы можно обнаружить посредством детального химического анализа разделенных гликоформ, но удобнее обнаруживать их посредством дифференциальной реакции с лектинами , как, например, с помощью лектиновой аффинной хроматографии и лектинового аффинного электрофореза . Типичными примерами гликопротеинов, состоящих из гликоформ, являются белки крови оросомукоид , антитрипсин и гаптоглобин . Необычная вариация гликоформ наблюдается в молекуле адгезии нейрональных клеток, NCAM, включающей полисиаловые кислоты, PSA .
Моноаминоксидаза , семейство ферментов, катализирующих окисление моноаминов, существует в двух изоформах: МАО-А и МАО-В.