В химии гидрон , неофициально называемый протоном , [2] представляет собой катионную форму атомарного водорода , обозначаемую символом H.+
. Общий термин «гидрон», одобренный ИЮПАК , охватывает катионы водорода независимо от их изотопного состава: таким образом, он в совокупности относится к протонам ( 1 H + ) для изотопа протия, дейтронам ( 2 H + или D + ) для дейтерия. изотоп и тритоны ( 3 H + или T + ) для изотопа трития .
В отличие от большинства других ионов, гидрон состоит только из атомного ядра . Отрицательно заряженным аналогом гидрона является гидрид- анион H.−
.
При прочих равных условиях соединения, которые легко отдают гидроны (кислоты Бренстеда, см. ниже), обычно являются полярными гидрофильными растворенными веществами и часто растворимы в растворителях с высокой относительной статической диэлектрической проницаемостью (диэлектрической проницаемостью). Примеры включают органические кислоты, такие как уксусная кислота (CH 3 COOH) или метансульфоновая кислота (CH 3 SO 3 H). Однако большие неполярные части молекулы могут ослабить эти свойства. Таким образом, из-за наличия алкильной цепи октановая кислота (C 7 H 15 COOH) значительно менее гидрофильна по сравнению с уксусной кислотой.
Несольватированный гидрон (полностью свободное или «голое» ядро атома водорода) не существует в конденсированной (жидкой или твердой) фазе. Хотя иногда говорят, что суперкислоты обязаны своей необычайной способностью донора гидронов присутствию «свободных гидронов», такое утверждение вводит в заблуждение: даже для такого источника «свободных гидронов», как H
2Ф+
, один из сверхкислотных катионов, присутствующих в сверхкислотной фторсурьмяной кислоте (HF:SbF 5 ), отщепление свободного H+
по-прежнему приводит к огромным энергетическим потерям, порядка нескольких сотен ккал/моль. Это эффективно исключает возможность присутствия свободного гидрона в растворе, даже в качестве мимолетного промежуточного продукта. По этой причине считается, что в жидких сильных кислотах гидроны диффундируют путем последовательного переноса от одной молекулы к другой по сети водородных связей посредством так называемого механизма Гроттуса . [3]
Ион гидрона может включить в молекулу электронную пару основания Льюиса путем аддукции:
Из-за захвата основания Льюиса (L) ион гидрона имеет кислотный характер Льюиса. С точки зрения теории жесткого/мягкого кислотного основания (HSAB) , голый гидрон представляет собой бесконечно жесткую кислоту Льюиса.
Гидрон играет центральную роль в кислотно-основной теории Бренстеда-Лоури : разновидность, которая ведет себя как донор гидрона в реакции, известна как кислота Бренстеда, а разновидность, принимающая гидрон, известна как основание Бренстеда. В общей кислотно-основной реакции, показанной ниже, HA является кислотой, а B (показан неподеленной парой) — основанием:
Гидратированная форма катиона водорода, ион гидроксония (гидроксония) H
3О+
(aq) является ключевым объектом определения кислоты Аррениусом . Другие гидратированные формы, катион Цунделя H
5О+
2, который образуется из протона и двух молекул воды, и собственного катиона H
9О+
4, который образуется из иона гидроксония и трех молекул воды, теоретически играет важную роль в диффузии протонов через водный раствор в соответствии с механизмом Гроттуса. Хотя ион H
3О+
(aq) часто указывается во вводных учебниках, чтобы подчеркнуть, что гидрон никогда не присутствует в водном растворе в несольватированном виде. Это несколько вводит в заблуждение, поскольку слишком упрощает печально известную сложную структуру сольватированного протона в воде; обозначение H+
(водный) часто предпочтительнее, поскольку он обеспечивает водную сольватацию, оставаясь при этом неопределенным в отношении количества участвующих молекул воды.
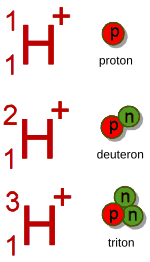
Другие изотопы водорода слишком нестабильны, чтобы их можно было использовать в химии.
ИЮПАК рекомендует использовать термин «гидрон» вместо «протон», если не проводится различие между изотопами протон, дейтрон и тритон, которые все встречаются в природных недифференцированных смесях изотопов . Название «протон» относится к изотопно чистому 1 H + . [4] С другой стороны, называть гидрон просто ионом водорода не рекомендуется, поскольку анионы водорода также существуют. [5]
Термин «гидрон» был определен ИЮПАК в 1988 году. [6] [7]
Традиционно термин «протон» был [2] и [ необходима ссылка ] используется вместо слова «гидрон». Последний термин обычно используется только в том контексте, где важно сравнение между различными изотопами водорода (например, при кинетическом изотопном эффекте или мечении изотопов водорода ). В противном случае называть гидроны протонами по-прежнему считается приемлемым, например, в таких терминах, как протонирование , депротонирование , протонный насос или протонный канал . Трансфер Х.+
в кислотно-основной реакции обычно называют переносом протона . Кислоты и основания называются донорами и акцепторами протонов соответственно.
99,9844% природных гидронов (ядер водорода) — это протоны, а остальная часть (около 156 на миллион в морской воде) — дейтроны (см. Дейтерий ), за исключением некоторых очень редких природных тритонов (см. Тритий ).
[T] Слово
протон
используется не только для иона
1
H
+
, но обычно и неправильно для H
+
в естественном изобилии. Во многих контекстах это не создает двусмысленности, и вполне вероятно, что такое использование будет продолжаться.