Биогеохимический цикл , или, в более общем смысле, круговорот материи , [1] — это движение и преобразование химических элементов и соединений между живыми организмами, атмосферой и земной корой. Основные биогеохимические циклы включают круговорот углерода , круговорот азота и круговорот воды . В каждом цикле химический элемент или молекула трансформируется и циркулирует в живых организмах, а также в различных геологических формах и резервуарах, включая атмосферу, почву и океаны. Его можно рассматривать как путь, по которому химическое вещество циркулирует (переворачивается или проходит) в биотическом отсеке и абиотических отсеках Земли . Биотическая часть — это биосфера , а абиотическая часть — это атмосфера , литосфера и гидросфера .
Например, в углеродном цикле углекислый газ из атмосферы поглощается растениями посредством фотосинтеза , который превращает его в органические соединения , которые используются организмами для получения энергии и роста. Затем углерод выбрасывается обратно в атмосферу в результате дыхания и разложения . Кроме того, углерод хранится в ископаемом топливе и выбрасывается в атмосферу в результате деятельности человека, такой как сжигание ископаемого топлива . В круговороте азота атмосферный азот преобразуется растениями в полезные формы, такие как аммиак и нитраты, посредством процесса фиксации азота . Эти соединения могут использоваться другими организмами, а азот возвращается в атмосферу посредством денитрификации и других процессов. В круговороте воды универсальный растворитель вода испаряется с суши и океанов, образуя облака в атмосфере, а затем выпадает обратно в разные части планеты. Осадки могут просачиваться в землю и становиться частью систем грунтовых вод, используемых растениями и другими организмами, или могут стекать с поверхности , образуя озера и реки. Подземные воды могут затем просачиваться в океан вместе с речными стоками , богатыми растворенными и твердыми органическими веществами и другими питательными веществами.
Существуют биогеохимические циклы для многих других элементов, таких как кислород , водород , фосфор , кальций , железо , сера , ртуть и селен . Существуют также циклы для молекул, таких как вода и кремнезем . Кроме того, существуют макроскопические циклы, такие как цикл горных пород , и антропогенные циклы синтетических соединений, таких как полихлорированные дифенилы (ПХД). В некоторых циклах существуют геологические резервуары, в которых вещества могут оставаться или изолироваться в течение длительных периодов времени.
Биогеохимические циклы представляют собой взаимодействие биологических, геологических и химических процессов. Биологические процессы включают влияние микроорганизмов , которые являются важнейшими движущими силами биогеохимического круговорота. Микроорганизмы обладают способностью осуществлять широкий спектр метаболических процессов , необходимых для круговорота питательных веществ и химических веществ в глобальных экосистемах. Без микроорганизмов многие из этих процессов не происходили бы, оказывая существенное влияние на функционирование экосистем суши и океана, а также биогеохимические циклы планеты в целом. Изменения в циклах могут повлиять на здоровье человека. Циклы взаимосвязаны и играют важную роль в регулировании климата, поддержке роста растений , фитопланктона и других организмов, а также поддержании здоровья экосистем в целом. Человеческая деятельность, такая как сжигание ископаемого топлива и использование большого количества удобрений, может нарушить циклы, способствуя изменению климата, загрязнению окружающей среды и другим экологическим проблемам.


Энергия течет направленно через экосистемы, входя в нее в виде солнечного света (или неорганических молекул для хемоавтотрофов ) и покидая ее в виде тепла во время многочисленных переходов между трофическими уровнями . Однако вещество, из которого состоят живые организмы, сохраняется и перерабатывается. Шесть наиболее распространенных элементов, связанных с органическими молекулами, — углерод, азот, водород, кислород, фосфор и сера — принимают различные химические формы и могут существовать в течение длительного времени в атмосфере, на суше, в воде или под поверхностью Земли. . Геологические процессы, такие как выветривание , эрозия , дренаж воды и субдукция континентальных плит , играют роль в переработке материалов. Поскольку геология и химия играют важную роль в изучении этого процесса, переработка неорганического вещества между живыми организмами и окружающей их средой называется биогеохимическим циклом. [3]
Шесть вышеупомянутых элементов используются организмами по-разному. Водород и кислород содержатся в воде и органических молекулах , оба из которых необходимы для жизни. Углерод содержится во всех органических молекулах, тогда как азот является важным компонентом нуклеиновых кислот и белков . Фосфор используется для производства нуклеиновых кислот и фосфолипидов , составляющих биологические мембраны . Сера имеет решающее значение для трехмерной формы белков. Круговорот этих элементов взаимосвязан. Например, движение воды имеет решающее значение для выщелачивания серы и фосфора в реки, которые затем могут течь в океаны. Минералы циркулируют в биосфере между биотическими и абиотическими компонентами и от одного организма к другому. [4]
Экологические системы ( экосистемы ) имеют множество биогеохимических циклов, действующих в составе системы, например круговорот воды, круговорот углерода, круговорот азота и др. Все химические элементы, встречающиеся в организмах, входят в состав биогеохимических циклов. Помимо того, что эти химические элементы являются частью живых организмов, они также проходят через абиотические факторы экосистем, таких как вода ( гидросфера ), земля ( литосфера ) и/или воздух ( атмосфера ). [5]
Живые факторы планеты можно назвать биосферой . Все питательные вещества, такие как углерод , азот , кислород , фосфор и сера , используемые в экосистемах живыми организмами, являются частью замкнутой системы ; следовательно, эти химикаты перерабатываются, а не теряются и постоянно пополняются, как, например, в открытой системе. [5]
Основные части биосферы связаны потоками химических элементов и соединений в биогеохимических круговоротах. Во многих из этих циклов важную роль играет биота . Вещество из недр Земли выбрасывается вулканами. Атмосфера быстро обменивается некоторыми соединениями и элементами с биотой и океанами. По сравнению с этим обмен веществами между горными породами, почвами и океанами обычно происходит медленнее. [2]
Поток энергии в экосистеме представляет собой открытую систему ; Солнце постоянно дает планете энергию в виде света, в то время как она в конечном итоге используется и теряется в виде тепла на всех трофических уровнях пищевой сети. Углерод используется для производства углеводов, жиров и белков — основных источников пищевой энергии . Эти соединения окисляются с выделением углекислого газа, который растения могут улавливать для образования органических соединений. Химическая реакция осуществляется за счет световой энергии солнечного света.
Солнечный свет необходим для объединения углерода с водородом и кислородом в источник энергии, но глубоководные экосистемы , куда солнечный свет не может проникнуть, получают энергию из серы. Сероводород вблизи гидротермальных источников может использоваться такими организмами, как гигантский трубчатый червь . В цикле серы сера может быть переработана навсегда в качестве источника энергии. Энергия может быть высвобождена за счет окисления и восстановления соединений серы (например, окисления элементарной серы до сульфита , а затем до сульфата ).
Хотя Земля постоянно получает энергию от Солнца, ее химический состав по существу фиксирован, поскольку метеориты лишь изредка добавляют дополнительное вещество. Поскольку этот химический состав не пополняется, как энергия, все процессы, которые зависят от этих химикатов, должны быть переработаны. Эти циклы включают как живую биосферу, так и неживую литосферу , атмосферу и гидросферу .
Биогеохимические циклы можно противопоставить геохимическим циклам . Последний касается только коровых и подкоровых резервуаров, хотя некоторые процессы в обоих случаях перекрываются.


Мировой океан покрывает более 70% поверхности Земли и чрезвычайно неоднороден. Морские продуктивные районы и прибрежные экосистемы составляют незначительную часть океана по площади поверхности, но оказывают огромное влияние на глобальные биогеохимические циклы, осуществляемые микробными сообществами , которые составляют 90% биомассы океана. [8] Работа в последние годы в основном сосредоточена на круговороте углерода и макроэлементов, таких как азот, фосфор и силикат: другие важные элементы, такие как сера или микроэлементы, изучены меньше, что отражает связанные с этим технические и логистические проблемы. [9] Эти морские районы и таксоны, образующие их экосистемы, все чаще подвергаются значительному антропогенному давлению, влияющему на морскую жизнь и переработку энергии и питательных веществ. [10] [11] [12] Ключевым примером является культурная эвтрофикация , когда сельскохозяйственные стоки приводят к обогащению прибрежных экосистем азотом и фосфором, что значительно увеличивает продуктивность, что приводит к цветению водорослей , деоксигенации водной толщи и морского дна, а также к увеличению выбросов парниковых газов. газовые выбросы, [13] с прямым местным и глобальным воздействием на циклы азота и углерода . Однако сток органических веществ с материка в прибрежные экосистемы — это лишь одна из ряда серьезных угроз, которые подвергают микробные сообщества стрессу из-за глобальных изменений. Изменение климата также привело к изменениям в криосфере : таяние ледников и вечной мерзлоты привело к усилению морской стратификации , в то время как сдвиги окислительно -восстановительного состояния в различных биомах быстро меняют микробные сообщества с беспрецедентной скоростью. [14] [15] [16] [17] [9]
Таким образом, глобальные изменения влияют на ключевые процессы, включая первичную продуктивность , фиксацию CO 2 и N 2 , дыхание/ реминерализацию органических веществ , а также погружение и захоронение фиксированного CO 2 . [17] В дополнение к этому, океаны переживают процесс подкисления с изменением pH на ~0,1 единицы между доиндустриальным периодом и сегодняшним днем, что влияет на химию карбонатного / бикарбонатного буфера . В свою очередь, сообщается, что подкисление оказывает воздействие на планктонные сообщества, главным образом за счет воздействия на кальцифицирующие таксоны. [18] Имеются также данные об изменениях в производстве ключевых промежуточных летучих продуктов, некоторые из которых имеют заметный парниковый эффект (например, N 2 O и CH 4 , рассмотренные Брейтбургом в 2018 году, [15] из-за увеличения глобального температура, стратификация океана и деоксигенация, приводящие к потере от 25 до 50% азота из океана в атмосферу в так называемых зонах минимума кислорода [19] или бескислородных морских зонах [20] , вызванных микробными процессами. , которые обычно токсичны для морского нектона , включая виды с пониженным содержанием серы, такие как H 2 S, оказывают негативное воздействие на морские ресурсы, такие как рыболовство и прибрежная аквакультура. морских экосистем, и особенно фундаментальную роль микробов как движущей силы функционирования экосистемы. [16] [9]
Микроорганизмы управляют большей частью биогеохимического круговорота в земной системе. [21] [22]
Химические вещества иногда хранятся в одном месте в течение длительного времени. Это место называется резервуаром , который, например, включает в себя такие объекты, как залежи угля , хранящие углерод в течение длительного периода времени. [23] Когда химические вещества хранятся лишь в течение коротких периодов времени, они хранятся в обменных пулах . Примеры обменных пулов включают растения и животных. [23]
Растения и животные используют углерод для производства углеводов, жиров и белков, которые затем можно использовать для построения их внутренних структур или для получения энергии. Растения и животные временно используют углерод в своих системах, а затем выделяют его обратно в воздух или окружающую среду. Как правило, резервуары являются абиотическими факторами, тогда как обменные пулы являются биотическими факторами. Углерод удерживается в растениях и животных в течение относительно короткого времени по сравнению с угольными месторождениями. Время, в течение которого химическое вещество удерживается в одном месте, называется временем его пребывания или временем оборота (также называемым временем обновления или сроком выхода). [23]
Боксовые модели широко используются для моделирования биогеохимических систем. [24] [25] Коробочные модели представляют собой упрощенные версии сложных систем, сводящие их к ящикам (или резервуарам для хранения) химических материалов, связанных материальными потоками (потоками). Простые модели коробок содержат небольшое количество коробок, свойства которых, например объем, не меняются со временем. Предполагается, что ящики ведут себя так, как если бы они были перемешаны однородно. [25] Эти модели часто используются для вывода аналитических формул, описывающих динамику и устойчивое содержание участвующих химических веществ.
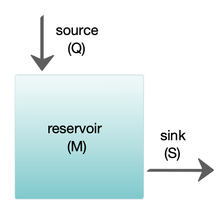
На диаграмме справа показана базовая одноблочная модель. Резервуар содержит количество рассматриваемого материала М , определенное по химическим, физическим или биологическим свойствам. Источник Q — это поток материала в резервуар, а сток S — поток материала из резервуара. Бюджет – это контроль и баланс источников и стоков, влияющих на круговорот веществ в водоеме. Резервуар находится в устойчивом состоянии , если Q = S , то есть если источники уравновешивают стоки и нет никаких изменений с течением времени. [25]
Время пребывания или оборота – это среднее время, в течение которого материал находится в резервуаре. Если резервуар находится в устойчивом состоянии, это время равно времени, необходимому для заполнения или опорожнения резервуара. Таким образом, если τ — время оборота, то τ = M / S . [25] Уравнение, описывающее скорость изменения содержания в резервуаре:
Когда два или более резервуаров соединены, материал можно рассматривать как циркулирующий между резервуарами, и циклический поток может иметь предсказуемые закономерности. [25] Более сложные мультибоксовые модели обычно решаются с использованием численных методов.

Глобальные биогеохимические бокс-модели обычно измеряют:
- масса резервуара в петаграммах (Пг)
- потоки стока в петаграммах в год (Пг/ год )
На диаграмме слева показан упрощенный бюджет потоков углерода в океане. Он состоит из трех простых взаимосвязанных коробчатых моделей: одна для эвфотической зоны , одна для внутренней части океана или темного океана и одна для океанских отложений . В эвфотической зоне чистая продукция фитопланктона составляет около 50 Пг С в год. Около 10 Пг экспортируется в глубь океана, а остальные 40 Пг выдыхаются. Разложение органического углерода происходит, когда частицы ( морской снег ) оседают в глубине океана. Только 2 Pg в конечном итоге достигают морского дна, а остальные 8 Pg вдыхаются в темном океане. В отложениях временной масштаб, доступный для разложения, увеличивается на порядки, в результате чего 90% поступившего органического углерода разлагается, и только 0,2 Пг С/год в конечном итоге захоранивается и переносится из биосферы в геосферу. [26]

На диаграмме справа показана более сложная модель со множеством взаимодействующих блоков. Массы резервуаров здесь представляют собой запасы углерода , измеряемые в Пг С. Потоки обмена углерода, измеряемые в Пг С/год , происходят между атмосферой и двумя ее основными поглотителями, сушей и океаном. Черные цифры и стрелки указывают массу резервуара и обменные потоки, рассчитанные на 1750 год, незадолго до промышленной революции . Красные стрелки (и соответствующие цифры) указывают годовые изменения потоков из-за антропогенной деятельности, усредненные за период 2000–2009 гг. Они показывают, как изменился углеродный цикл с 1750 года. Красные цифры в водоемах представляют собой совокупные изменения антропогенного углерода с начала индустриального периода, 1750–2011 годов. [28] [29] [27]

Различают быстрые и медленные биогеохимические циклы. Быстрый цикл действует в биосфере , а медленный — в горных породах . Быстрые или биологические циклы могут завершиться в течение нескольких лет, перемещая вещества из атмосферы в биосферу, а затем обратно в атмосферу. Медленные или геологические циклы могут занять миллионы лет, перемещая вещества через земную кору между горными породами, почвой, океаном и атмосферой. [31]
В качестве примера быстрый углеродный цикл показан на диаграмме ниже слева. Этот цикл включает относительно кратковременные биогеохимические процессы между окружающей средой и живыми организмами биосферы. Он включает перемещение углерода между атмосферой, наземными и морскими экосистемами, а также почвами и отложениями морского дна . Быстрый цикл включает годовые циклы, включающие фотосинтез, и десятилетние циклы, включающие вегетативный рост и разложение. Реакция быстрого углеродного цикла на деятельность человека будет определять многие из наиболее непосредственных последствий изменения климата. [32] [33] [34] [35]
Медленный цикл показан на диаграмме выше справа. Он включает в себя средне- и долгосрочные геохимические процессы, относящиеся к циклу горных пород . Обмен между океаном и атмосферой может занять столетия, а выветривание горных пород — миллионы лет. Углерод в океане осаждается на дно океана, где может образовывать осадочные породы и погружаться в мантию Земли . Процессы горообразования приводят к возвращению этого геологического углерода на поверхность Земли. Там породы выветриваются, а углерод путем дегазации возвращается в атмосферу и реками в океан. Другой геологический углерод возвращается в океан посредством гидротермальной эмиссии ионов кальция. За год по этому медленному циклу перемещается от 10 до 100 миллионов тонн углерода. Сюда входят вулканы, возвращающие геологический углерод непосредственно в атмосферу в виде углекислого газа. Однако это менее одного процента углекислого газа, выбрасываемого в атмосферу при сжигании ископаемого топлива. [31] [32]
Земные недра являются крупнейшим резервуаром углерода на Земле, содержащим 14–135 Пг углерода [36] и 2–19% всей биомассы. [37] Микроорганизмы управляют трансформацией органических и неорганических соединений в этой среде и тем самым контролируют биогеохимические циклы. Современные знания о микробной экологии недр в первую очередь основаны на последовательностях генов 16S рибосомальной РНК (рРНК). Недавние оценки показывают, что <8% последовательностей 16S рРНК в общедоступных базах данных происходят от подповерхностных организмов [38] и лишь небольшая часть из них представлена геномами или изолятами. Таким образом, достоверной информации о микробном метаболизме в недрах крайне мало. Кроме того, мало что известно о том, как организмы в подземных экосистемах метаболически взаимосвязаны. Некоторые исследования синтрофных консорциумов , основанные на культивировании [39] [40] [41] и мелкомасштабный метагеномный анализ природных сообществ [42] [43] [44] предполагают, что организмы связаны посредством метаболических передач: переноса продуктов окислительно-восстановительных реакций. одного организма в другой. Однако ни одна сложная среда не была изучена достаточно полно, чтобы выявить сети метаболических взаимодействий, лежащие в их основе. Это ограничивает способность биогеохимических моделей отражать ключевые аспекты циклов углерода и других питательных веществ. [45] Новые подходы, такие как метагеномика с разрешением генома, подход, который может дать полный набор черновых и даже полных геномов организмов без необходимости лабораторной изоляции [42] [46] [47], потенциально могут обеспечить эту важную уровень понимания биогеохимических процессов. [48]
Некоторые из наиболее известных биогеохимических циклов показаны ниже:
Многие биогеохимические циклы в настоящее время изучаются впервые. Изменение климата и антропогенное воздействие радикально меняют скорость, интенсивность и баланс этих относительно неизвестных циклов, которые включают в себя:
Биогеохимические циклы всегда включают состояния активного равновесия: баланс в круговороте элемента между компартментами. Однако общий баланс может включать в себя сегменты, распределенные в глобальном масштабе.
Поскольку биогеохимические циклы описывают движение веществ по всему земному шару, их изучение по своей сути является междисциплинарным. Углеродный цикл может быть связан с исследованиями в области экологии и наук об атмосфере . [53] Биохимическая динамика также может быть связана с областями геологии и почвоведения . [54]
{{cite book}}: CS1 maint: numeric names: authors list (link)