К-казеин , или каппа-казеин , представляет собой белок молока млекопитающих , участвующий в нескольких важных физиологических процессах. Химозин (содержащийся в сычужном ферменте ) расщепляет К-казеин на нерастворимый пептид (паракаппа-казеин) и водорастворимый гликомакропептид (ГМП). GMP отвечает за повышение эффективности пищеварения, предотвращение гиперчувствительности новорожденных к потребляемым белкам и ингибирование желудочных патогенов. [1] Человеческий ген κ-казеина — CSN3 .

Казеины представляют собой семейство фосфопротеинов ( αS1 , αS2, β , κ), которые составляют почти 80% белков коровьего молока [3] и образуют растворимые агрегаты, известные как «казеиновые мицеллы», в которых молекулы κ-казеина стабилизируют структуру. Существует несколько моделей, объясняющих пространственную конформацию казеина в мицеллах. [4] Одна из них предполагает, что мицеллярное ядро образовано несколькими субмицеллами, периферия состоит из микроворсинок κ-казеина [5] [6] Другая модель предполагает, что ядро образовано фибриллами, связанными между собой казеином. [7] Наконец, самая последняя модель [8] предполагает двойную связь между казеинами, обеспечивающую гелеобразование. Все три модели рассматривают мицеллы как коллоидные частицы, образованные агрегатами казеина, обернутыми растворимыми молекулами κ-казеина. Протеазы, свертывающие молоко, действуют на растворимую часть, κ-казеин, создавая нестабильное мицеллярное состояние, которое приводит к образованию сгустков. [9]

Химозин (EC 3.4.23.4) представляет собой аспарагиновую протеазу , которая специфически гидролизует пептидную связь в Phe105-Met106 κ-казеина и считается наиболее эффективной протеазой для сыродельной промышленности. [10] Однако существуют протеазы, свертывающие молоко, способные расщеплять другие пептидные связи в цепи κ-казеина, такие как эндотиапепсин, продуцируемый Endothia parasitica . [11] Существует также несколько молокосвертывающих протеаз, которые, будучи способны расщеплять связь Phe105-Met106 в молекуле κ-казеина, также расщепляют и другие пептидные связи в других казеинах, например, продуцируемых Cynara cardunculus [6] [12] ] [13] или даже бычий химозин. [14] Это позволяет производить различные сыры с различными реологическими и органолептическими свойствами.
Процесс свертывания молока состоит из трех основных фаз: [15]
Каждый этап следует разной кинетической схеме, причем ограничивающим этапом свертывания молока является скорость разложения κ-казеина. На кинетическую картину второй стадии процесса свертывания молока влияет кооперативный характер мицеллярной флокуляции [16, 13] , тогда как реологические свойства образующегося геля зависят от типа действия протеаз, типа молоко и закономерности протеолиза казеина. [13] На общий процесс влияют несколько различных факторов, таких как pH или температура. [12] [9]
Традиционный способ количественного определения данного молокосвертывающего фермента [17] использует молоко в качестве субстрата и определяет время, прошедшее до появления молочных сгустков. Однако свертывание молока может происходить и без участия ферментов из-за изменений физико-химических факторов, таких как низкий уровень pH или высокая температура. [6] [3] [9] Следовательно, это может привести к запутанным и невоспроизводимым результатам, особенно когда ферменты имеют низкую активность. В то же время классический метод недостаточно специфичен с точки зрения установления точного начала гелеобразования молока, поэтому определение участвующих ферментных единиц становится затруднительным и неясным. Более того, хотя сообщалось, что гидролиз κ-казеина следует типичной кинетике Михаэлиса-Ментена [15] , его трудно определить с помощью классического анализа свертывания молока.
Чтобы преодолеть эту проблему, было предложено несколько альтернативных методов, таких как определение диаметра гало в агар-желированном молоке, [17] колориметрическое измерение [18] или определение скорости разложения казеина, ранее меченного радиоактивным индикатором [17 ]. 19] или соединение флуорохрома . [20] Все эти методы используют казеин в качестве субстрата для количественной оценки протеолитической или молокосвертывающей активности.
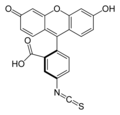
Κ-казеин, меченный изотиоцианатом флуоресцеина ( FITC ), с получением производного тиокарбамоила флуоресцеина ( FTC ). Этот субстрат используется для определения активности протеаз по свертыванию молока. [21]
Метод FTC-κ-казеина позволяет точно и точно определить κ-казеинолитическую деградацию, первый этап процесса свертывания молока. Этот метод является результатом модификации метода, описанного SS Twining (1984). Основная модификация заключалась в замене ранее использовавшегося субстрата ( казеина ) на κ-казеин, меченный изотиоцианатом флуоресцеина флуорохрома (FITC), с получением производного тиокарбамоила флуоресцеина (FTC). Этот вариант позволяет более точно и специфично определить количество разложившихся молекул κ-казеина, обнаруживая только те ферменты, которые способны расщеплять такие молекулы. Однако метод, описанный Твинингом (1984), был разработан для обнаружения протеолитической активности значительно большего числа ферментов. FTC-κ-казеин позволяет обнаруживать различные типы протеаз на уровнях, когда свертывание молока еще не очевидно, демонстрируя его более высокую чувствительность по сравнению с используемыми в настоящее время методами анализа. Таким образом, метод может найти применение в качестве индикатора при очистке или характеристике новых молокосвертывающих ферментов.