Мембранные липиды представляют собой группу соединений (структурно подобных жирам и маслам), которые образуют липидный бислой клеточной мембраны . Тремя основными классами мембранных липидов являются фосфолипиды , гликолипиды и холестерин . Липиды амфифильны : у них есть один конец, растворимый в воде («полярный»), и конец, растворимый в жире («неполярный»). Образуя двойной слой с полярными концами, направленными наружу, и неполярными концами, направленными внутрь, мембранные липиды могут образовывать «липидный бислой», который удерживает водную внутреннюю часть клетки отдельно от водянистой внешней части клетки. Расположение липидов и различных белков, действующих как рецепторы и поры каналов в мембране, контролирует вход и выход других молекул и ионов в рамках клеточного метаболизма. Чтобы выполнять физиологические функции, мембранные белки могут вращаться и диффундировать в латеральном направлении в двумерном пространстве липидного бислоя благодаря наличию липидной оболочки, тесно прикрепленной к поверхности белка, называемой кольцевой липидной оболочкой .
Бислой, образованный мембранными липидами, служит удерживающей единицей живой клетки. Мембранные липиды также образуют матрицу, в которой находятся мембранные белки . Исторически считалось, что липиды выполняют лишь структурную роль. Функциональные роли липидов на самом деле многочисленны: они служат регуляторными агентами роста и адгезии клеток . Они участвуют в биосинтезе других биомолекул . Они могут служить для повышения ферментативной активности ферментов . [1]
Липид, не образующий бислой, такой как моногалактозилдиглицерид (МГДГ), преобладает среди липидов в тилакоидных мембранах, которые при гидратации в одиночку образуют обращенную гексагональную цилиндрическую фазу. Однако в сочетании с другими липидами и каротиноидами / хлорофиллами тилакоидных мембран они тоже образуют липидные бислои. [2]
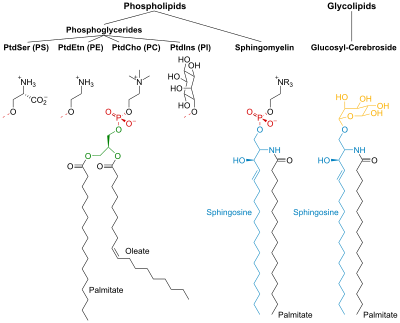
Фосфолипиды и гликолипиды состоят из двух длинных неполярных ( гидрофобных ) углеводородных цепей , связанных с гидрофильной головной группой.
Головки фосфолипидов фосфорилированы и состоят из:
Тетраэфир диалкилглицерина (GDGT) помогает изучать древние факторы окружающей среды . [3]
Головки гликолипидов (глико-сахар) содержат сфингозин с присоединенными к нему одной или несколькими сахарными единицами . Гидрофобные цепи принадлежат либо:
Галактолипиды - моногалактозилдиглицерид (МГДГ) и дигалактозилдиглицерид (ДГДГ) образуют преобладающие липиды в мембранах тилакоидов хлоропластов высших растений; липосомальные структуры, образованные общим липидным экстрактом тилакоидных мембран, оказались чувствительными к сахарозе, поскольку она превращает бислои в мицеллярные структуры. [4]
Жирные кислоты в фосфо- и гликолипидах обычно содержат четное число атомов углерода , обычно от 14 до 24 , причем наиболее распространенными являются 16- и 18-углеродные атомы. ЖК могут быть насыщенными и ненасыщенными, причем конфигурация двойных связей почти всегда цис . Длина и степень ненасыщенности цепей ЖК оказывают глубокое влияние на текучесть мембран . Мембраны тилакоидов растений сохраняют высокую текучесть даже при относительно низких температурах окружающей среды благодаря обилию 18-углеродных жирных ацильных цепей с тремя двойными связями - линоленовой кислоты , как было выявлено методами ЯМР 13-С. [5]
В фосфоглицеридах гидроксильные группы при С-1 и С-2 глицерина этерифицированы карбоксильными группами жирных кислот. Гидроксильная группа С-3 этерифицирована до фосфорной кислоты. Полученное соединение, называемое фосфатидатом , представляет собой простейший фосфоглицерат . В мембранах присутствуют лишь небольшие количества фосфатидата. Однако он является ключевым промежуточным продуктом в биосинтезе других фосфоглицеридов.
Сфингозин — аминоспирт , содержащий длинную ненасыщенную углеводородную цепь. В сфингомиелине и гликолипидах аминогруппа сфингозина связана с ЖК амидной связью. В сфингомиелине первичная гидроксильная группа сфингозина этерифицирована до фосфорилхолина .

В гликолипидах к этой группе присоединяется сахарный компонент. Простейший гликолипид — цереброзид , в котором имеется только один сахарный остаток — Glc или Gal . Более сложные гликолипиды, такие как ганглиозиды , содержат разветвленную цепь, состоящую до семи остатков сахаров.
Самый известный стерол — холестерин , который содержится в организме человека. Холестерин также содержится в мембранах других клеток эукариот . Стеролы имеют гидрофобную четырехчленную жесткую структуру слитого кольца и небольшую полярную головную группу.
Холестерин биосинтезируется из мевалоната посредством скваленовой циклизации терпеноидов . Клеточные мембраны требуют высокого уровня холестерина – обычно в среднем 20% холестерина во всей мембране, локально увеличиваясь в участках плота до 50% холестерина (-% — молекулярное соотношение). [6] Он преимущественно связывается со сфинголипидами (см. Диаграмму) в богатых холестерином липидных рафтах участков мембран эукариотических клеток. [7] Формирование липидных рафтов способствует агрегации периферических и трансмембранных белков , включая стыковку белков SNARE и VAMP . [8] Фитостерины , такие как ситостерин и стигмастерин, и гопаноиды выполняют аналогичную функцию у растений и прокариот .