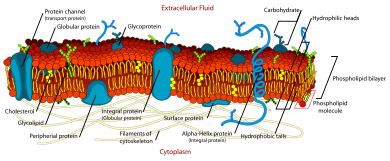
Модель жидкостной мозаики объясняет различные характеристики структуры функциональных клеточных мембран . Согласно этой биологической модели , существует липидный бислой (слой толщиной в две молекулы, состоящий в основном из амфипатических фосфолипидов), в который встроены белковые молекулы . Бислой фосфолипидов придает мембране текучесть и эластичность . Небольшое количество углеводов также содержится в клеточной мембране. Биологическая модель, разработанная Сеймуром Джонатаном Сингером и Гартом Л. Николсоном в 1972 году [1] , описывает клеточную мембрану как двумерную жидкость , ограничивающую латеральную диффузию компонентов мембраны. Такие домены определяются наличием внутри мембраны участков со специальным липидным и белковым коконом, которые способствуют образованию липидных рафтов или белково- гликопротеиновых комплексов. Другим способом определения мембранных доменов является ассоциация липидной мембраны с нитями цитоскелета и внеклеточным матриксом через мембранные белки. [2] Текущая модель описывает важные особенности, относящиеся ко многим клеточным процессам, в том числе: передача сигналов между клетками , апоптоз , деление клеток , почкование мембран и слияние клеток. Модель жидкостной мозаики является наиболее приемлемой моделью плазматической мембраны. В этом определении клеточной мембраны ее основная функция — выступать в качестве барьера между содержимым внутри клетки и внеклеточной средой.
Жидкостные свойства функциональных биологических мембран были определены с помощью экспериментов по маркировке , рентгеновской дифракции и калориметрии. Эти исследования показали, что интегральные мембранные белки диффундируют со скоростью, зависящей от вязкости липидного бислоя, в который они встроены, и продемонстрировали, что молекулы внутри клеточной мембраны являются скорее динамическими, чем статичными. [1]
Предыдущие модели биологических мембран включали модель мембраны Робертсона и трехслойную модель Дэвсона-Даниелли . [2] В этих моделях белки присутствовали в виде листов, соседних с липидным слоем, а не были включены в фосфолипидный бислой. Другие модели описывали повторяющиеся регулярные единицы белка и липида. Эти модели не были хорошо подтверждены микроскопическими и термодинамическими данными и не учитывали доказательства динамических свойств мембран. [2]

Важный эксперимент, который предоставил доказательства в пользу жидкостной и динамической биологии, был проведен Фраем и Эдидином. Они использовали вирус Сендай , чтобы заставить клетки человека и мыши сливаться и образовывать гетерокарион . Используя окрашивание антителами , они смогли показать, что мышиные и человеческие белки оставались разделенными, образуя отдельные половины гетерокариона, спустя короткое время после слияния клеток. Однако со временем белки диффундировали, и со временем граница между двумя половинками утрачивалась. Снижение температуры замедляло скорость этой диффузии, заставляя мембранные фосфолипиды переходить из жидкой фазы в гелевую. [3] Сингер и Николсон рационализировали результаты этих экспериментов, используя свою модель жидкостной мозаики. [1]
Модель жидкостной мозаики объясняет изменения в структуре и поведении клеточных мембран при различных температурах, а также ассоциацию мембранных белков с мембранами. Хотя Сингер и Николсон располагали существенными доказательствами, полученными из различных областей, в поддержку своей модели, недавние достижения в области флуоресцентной микроскопии и структурной биологии подтвердили жидкостно-мозаичную природу клеточных мембран.
Кроме того, два листка биологических мембран асимметричны и разделены на субдомены, состоящие из специфических белков или липидов, что позволяет пространственно разделить биологические процессы, связанные с мембранами. Белки, взаимодействующие с холестерином и холестерином, могут концентрироваться в липидных плотах и ограничивать процессы передачи сигналов в клетках только этими плотами. [4] Другая форма асимметрии была показана в работе Моуритсена и Блума в 1984 году, где они предложили « матрасную модель » липид-белковых взаимодействий для рассмотрения биофизических данных о том, что мембрана может различаться по толщине и гидрофобности белков. [5]
Существование недвуслойных липидных образований с важными биологическими функциями было подтверждено после публикации модели жидкостной мозаики. Эти мембранные структуры могут быть полезны, когда клетке необходимо размножать недвухслойную форму, что происходит во время деления клетки и образования щелевого соединения . [6]
Бислой мембраны не всегда плоский. Локальная кривизна мембраны может быть вызвана асимметрией и недвуслойной организацией липидов, как обсуждалось выше. Более драматическая и функциональная кривизна достигается за счет доменов BAR , которые связываются с фосфатидилинозитолом на поверхности мембраны, способствуя образованию везикул , образованию органелл и делению клеток. [7] Развитие кривизны постоянно меняется и способствует динамическому характеру биологических мембран. [8]
В 1970-х годах было признано, что отдельные молекулы липидов подвергаются свободной латеральной диффузии внутри каждого из слоев липидной мембраны. [9] Диффузия происходит с высокой скоростью: средняя молекула липида диффундирует примерно на 2 мкм, что примерно соответствует длине большой бактериальной клетки, примерно за 1 секунду. [9] Также было замечено, что отдельные молекулы липидов быстро вращаются вокруг своей оси. [9] Более того, молекулы фосфолипидов могут, хотя и редко, мигрировать с одной стороны липидного бислоя на другую (процесс, известный как триггер). Однако движение флип-флоп усиливается ферментами флиппазами. [10] Описанные выше процессы влияют на неупорядоченную природу липидных молекул и взаимодействующих белков в липидных мембранах, что оказывает влияние на текучесть мембран, передачу сигналов, транспортировку и функцию.
Существуют ограничения на латеральную подвижность липидных и белковых компонентов в жидкой мембране, налагаемые образованием субдоменов внутри липидного бислоя. Эти субдомены возникают в результате нескольких процессов, например, связывания компонентов мембраны с внеклеточным матриксом, нанометрических участков мембраны с определенным биохимическим составом, которые способствуют образованию липидных рафтов и белковых комплексов, опосредованных белок-белковыми взаимодействиями. [2] Кроме того, белково-цитоскелетные ассоциации опосредуют образование «цитоскелетных заборов», загонов, в которых липидные и мембранные белки могут свободно диффундировать, но редко покидать их. [2] Ограничение скорости латеральной диффузии мембранных компонентов очень важно, поскольку оно позволяет функциональную специализацию определенных областей внутри клеточных мембран.
Липидные рафты представляют собой мембранные нанометрические платформы с определенным липидным и белковым составом, которые диффундируют латерально, перемещаясь по жидкому билипидному слою. Сфинголипиды и холестерин являются важными строительными блоками липидных рафтов. [11]
Белки и гликопротеины клеточной мембраны не существуют как отдельные элементы липидной мембраны, как впервые предположили Сингер и Николсон в 1972 году. Скорее, они возникают в виде диффузионных комплексов внутри мембраны. [2] Сборка отдельных молекул в эти макромолекулярные комплексы имеет важные функциональные последствия для клетки; такие как транспорт ионов и метаболитов , передача сигналов, клеточная адгезия и миграция . [2]
Некоторые белки, встроенные в билипидный слой, взаимодействуют с внеклеточным матриксом вне клетки, нитями цитоскелета внутри клетки и кольцеобразными структурами септина. Эти взаимодействия оказывают сильное влияние на форму и структуру, а также на компартментализацию . Более того, они накладывают физические ограничения, которые ограничивают свободную латеральную диффузию белков и, по крайней мере, некоторых липидов внутри билипидного слоя. [2]
Когда интегральные белки липидного бислоя привязаны к внеклеточному матриксу, они не могут свободно диффундировать. Белки с длинным внутриклеточным доменом могут сталкиваться с ограждением, образованным нитями цитоскелета. [12] Оба процесса ограничивают диффузию непосредственно вовлеченных белков и липидов, а также других взаимодействующих компонентов клеточных мембран.

Септины представляют собой семейство GTP-связывающих белков, высококонсервативных среди эукариот. У прокариотов есть похожие белки, называемые парасептинами. Они образуют компартментализирующие кольцевые структуры, прочно связанные с клеточными мембранами. Септины участвуют в формировании таких структур, как реснички и жгутики, дендритные шипики и дрожжевые почки. [13]