Известно несколько аллотропов кислорода . Наиболее знакомым является молекулярный кислород ( O 2 ), присутствующий в значительных количествах в атмосфере Земли и также известный как дикислород или триплетный кислород . Другой — высокореактивный озон ( O 3 ). Другие:
Атомарный кислород, обозначаемый O или O 1 , очень реакционноспособен, поскольку отдельные атомы кислорода имеют тенденцию быстро связываться с близлежащими молекулами. Его электронное состояние с самой низкой энергией представляет собой триплет спинов , обозначаемый терминальным символом 3 P. На поверхности Земли он существует естественным образом в течение очень короткого времени. В космическом пространстве наличие обильного ультрафиолетового излучения приводит к образованию атмосферы на низкой околоземной орбите , в которой 96% кислорода присутствует в атомарной форме. [1]
Атомарный кислород был обнаружен на Марсе «Маринером» , « Викингом» и обсерваторией СОФИЯ . [2]
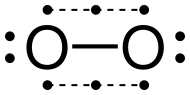
Общий аллотроп элементарного кислорода на Земле, O 2 , обычно известен как кислород, но его можно называть дикислородом , двухатомным кислородом , молекулярным кислородом , диоксидом или газообразным кислородом , чтобы отличить его от самого элемента и от трехатомного аллотропного озона O 3 . . Элементарный кислород , являющийся основным компонентом (около 21% по объему) земной атмосферы , чаще всего встречается в двухатомной форме. Аэробные организмы используют атмосферный диоксид кислорода в качестве конечного окислителя в клеточном дыхании для получения химической энергии . Основное состояние дикислорода известно как триплетный кислород 3 [ O 2 ] , поскольку он имеет два неспаренных электрона. Первое возбужденное состояние, синглетный кислород , 1 [O2 ] , не имеет неспаренных электронов и является метастабильным . Дублетное состояние требует нечетного числа электронов и поэтому не может возникнуть в диоксиде без присоединения или потери электронов, например, в супероксид - ионе ( O −2) или диоксигенильный ион ( O+2).
Основное состояние O 2 имеет длину связи 121 пм и энергию связи 498 кДж/моль. [3] Это бесцветный газ с температурой кипения -183 ° C (90 K; -297 ° F). [4] Его можно конденсировать из воздуха путем охлаждения жидким азотом, температура кипения которого составляет -196 ° C (77 K; -321 ° F). Жидкий кислород имеет бледно-голубой цвет и явно парамагнитен из-за неспаренных электронов; жидкий кислород, содержащийся в колбе, подвешенной на веревке, притягивается к магниту.
Синглетный кислород — общее название, используемое для двух метастабильных состояний молекулярного кислорода ( O 2 ) с более высокой энергией, чем основное состояние триплетного кислорода . Из-за различий в электронных оболочках синглетный кислород имеет другие химические и физические свойства, чем триплетный кислород, включая поглощение и излучение света на разных длинах волн. Он может генерироваться в фотосенсибилизированном процессе путем передачи энергии от молекул красителей, таких как бенгальский розовый , метиленовый синий или порфирины , или в результате химических процессов, таких как спонтанное разложение триоксида водорода в воде или реакция перекиси водорода с гипохлоритом .
Трехатомный кислород (озон, O 3 ) — очень реакционноспособный аллотроп кислорода, который при стандартных температуре и давлении представляет собой бледно-голубой газ . Жидкий и твердый O 3 имеют более глубокий синий цвет, чем обычный O 2 , они нестабильны и взрывоопасны. [5] [6] В газовой фазе озон разрушает такие материалы, как резина и ткань , и повреждает легочную ткань. [7] Его следы можно обнаружить по резкому хлороподобному запаху, [4] исходящему от электродвигателей , лазерных принтеров и копировальных аппаратов , поскольку он образуется всякий раз, когда воздух подвергается электрическому разряду. Он был назван «озоном» в 1840 году Кристианом Фридрихом Шёнбейном , [8] от древнегреческого ὄζειν (озеин: «пахнуть») плюс суффикс -on , обычно используемый в то время для обозначения производного соединения и переведенный на английский язык как -one . [9]
Озон термодинамически нестабилен и имеет тенденцию реагировать с образованием более распространенной формы дикислорода. Он образуется в результате реакции неповрежденного O 2 с атомарным кислородом, образующимся при расщеплении O 2 УФ-излучением в верхних слоях атмосферы . [5] Озон сильно поглощает ультрафиолет, а в стратосфере действует как щит для биосферы от мутагенных и других разрушительных эффектов солнечного УФ-излучения (см. Озоновый слой ). [5] Тропосферный озон образуется вблизи поверхности Земли в результате фотохимического распада диоксида азота в выхлопных газах автомобилей . [10] Приземный озон является загрязнителем воздуха , который особенно вреден для пожилых людей, детей и людей с заболеваниями сердца и легких, такими как эмфизема , бронхит и астма . [11] Иммунная система вырабатывает озон как противомикробное средство (см. ниже). [12]
Циклический озон представляет собой теоретически предсказанную молекулу O 3 , в которой три атома кислорода связаны в равносторонний треугольник, а не в открытый угол.
Предполагалось, что тетракислород существует с начала 1900-х годов, когда он был известен как оксозон. Он был обнаружен в 2001 году командой под руководством Фульвио Какаче из Римского университета. [13] Считалось, что молекула O 4 находится в одной из фаз твердого кислорода , позже идентифицированного как O 8 . Команда Какаче предположила, что O 4 , вероятно, состоит из двух гантелеобразных молекул O 2 , слабо удерживаемых вместе индуцированными дипольными дисперсионными силами.
Известно шесть различных фаз твердого кислорода. Один из них — темно-красное скопление О 8 . Когда кислород подвергается давлению 96 ГПа, он становится металлическим , подобно водороду [14] и становится более похожим на более тяжелые халькогены , такие как селен (демонстрирующий розово-красный цвет в своем элементарном состоянии), теллур и полоний , оба из которых имеют значительный металлический характер. При очень низких температурах эта фаза также становится сверхпроводящей .