
В химии неподеленная пара относится к паре валентных электронов , которые не являются общими с другим атомом в ковалентной связи [1] , и иногда ее называют неподеленной парой или несвязывающей парой . Неподеленные пары находятся на внешней электронной оболочке атомов. Их можно идентифицировать, используя структуру Льюиса . Поэтому электронные пары считаются неподеленными парами, если два электрона спарены, но не участвуют в химической связи . Таким образом, количество электронов в неподеленных парах плюс количество электронов в связях равняется числу валентных электронов вокруг атома.
Неподеленная пара — это концепция, используемая в теории отталкивания электронных пар валентной оболочки (теория VSEPR), которая объясняет формы молекул . Они также упоминаются в химии кислот и оснований Льюиса . Однако не все несвязывающие пары электронов химики считают неподеленными парами. Примерами являются переходные металлы, несвязывающие пары которых не влияют на геометрию молекулы и считаются стереохимически неактивными. В теории молекулярных орбиталей (полностью делокализованные канонические орбитали или локализованные в той или иной форме) концепция неподеленной пары менее ясна, поскольку соответствие между орбиталью и компонентами структуры Льюиса часто не является простым. Тем не менее, занятые несвязывающие орбитали (или орбитали преимущественно несвязывающего характера) часто идентифицируются как неподеленные пары.
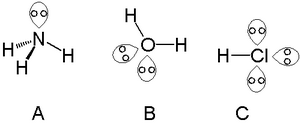
Единственную неподеленную пару можно найти с атомами в группе азота , например, с азотом в аммиаке . Две неподеленные пары можно найти с атомами халькогенной группы , например, с кислородом в воде. Галогены могут нести три неподеленные пары, например, в хлористом водороде .
В теории VSEPR пары электронов на атоме кислорода в воде образуют вершины тетраэдра с неподеленными парами в двух из четырех вершин. Валентный угол H–O–H составляет 104,5°, что меньше 109°, предсказанных для тетраэдрического угла , и это можно объяснить отталкивающим взаимодействием между неподеленными парами. [2] [3] [4]
Были предложены различные вычислительные критерии наличия неподеленных пар. Хотя сама плотность электронов ρ( r ), как правило, не дает полезных указаний в этом отношении, показательной является лапласиан электронной плотности, и одним из критериев местоположения неподеленной пары является то, что L ( r ) = – ∇ 2 ρ( r ) является локальным максимумом. Минимум электростатического потенциала V ( r ) является еще одним предлагаемым критерием. Еще один рассматривает функцию локализации электрона (ELF). [5]

Пары часто обладают отрицательной полярностью , обладают высокой плотностью заряда и в среднем расположены ближе к атомному ядру , чем связывающая пара электронов. Наличие неподеленной пары уменьшает валентный угол между связывающей парой электронов из-за их высокого электрического заряда, что вызывает сильное отталкивание между электронами. Они также участвуют в образовании дативной связи . Например, образование иона гидроксония (H 3 O + ) происходит при растворении кислот в воде и происходит из-за того, что атом кислорода отдает неподеленную пару иону водорода .
Это можно увидеть более ясно, если посмотреть на две более распространенные молекулы . Например, в углекислом газе (CO 2 ), не имеющем неподеленной пары, атомы кислорода находятся на противоположных сторонах атома углерода ( линейная молекулярная геометрия ), тогда как в воде (H 2 O), имеющей две неподеленные пары, угол между атомами водорода составляет 104,5° ( изогнутая геометрия молекулы ). Это вызвано силой отталкивания двух неподеленных пар атомов кислорода, которые отталкивают атомы водорода дальше друг от друга, пока силы всех электронов на атоме водорода не придут в равновесие . Это иллюстрация теории VSEPR .
Неподеленные пары могут вносить вклад в дипольный момент молекулы . NH 3 имеет дипольный момент 1,42 Д. Поскольку электроотрицательность азота (3,04) больше, чем электроотрицательность водорода (2,2), в результате связи NH являются полярными с суммарным отрицательным зарядом на атоме азота и меньшим суммарным положительным зарядом. заряд на атомах водорода. Существует также диполь, связанный с неподеленной парой, и это усиливает вклад полярных ковалентных связей NH в дипольный момент аммиака . В отличие от NH 3 , NF 3 имеет гораздо меньший дипольный момент, равный 0,234 Д. Фтор более электроотрицательен, чем азот, и полярность связей NF противоположна полярности связей NH в аммиаке, так что диполь за счет одинокого пара противостоит диполям связи NF, что приводит к низкому молекулярному дипольному моменту. [6]
Неподеленная пара может способствовать существованию хиральности в молекуле, тогда как все три другие группы, присоединенные к атому, различаются. Эффект наблюдается в некоторых аминах , фосфинах , [7] ионах сульфония и оксония , сульфоксидах и даже карбанионах .
Разделение энантиомеров, в которых стереогенным центром является амин, обычно невозможно, поскольку энергетический барьер для инверсии азота в стереоцентре низок, что позволяет двум стереоизомерам быстро взаимопревращаться при комнатной температуре. В результате такие хиральные амины невозможно разделить, если аминные группы не ограничены циклической структурой (например, в основании Трегера ).
Стереохимически активная неподеленная пара также ожидается для двухвалентных ионов свинца и олова из-за их формальной электронной конфигурации ns 2 . В твердом состоянии это приводит к искаженной координации металлов, наблюдаемой в тетрагональной структуре глета , принятой как PbO, так и SnO. Недавно было показано , что образование этих неподеленных ns 2 пар тяжелых металлов , которое ранее приписывалось внутриатомной гибридизации s- и p-состояний металла [8], имеет сильную анионную зависимость. [9] Эта зависимость от электронных состояний аниона может объяснить, почему некоторые двухвалентные материалы из свинца и олова, такие как PbS и SnTe, не демонстрируют стереохимических признаков неподеленной пары и принимают симметричную кристаллическую структуру каменной соли. [10] [11]
В молекулярных системах неподеленная пара также может приводить к нарушению координации лигандов вокруг иона металла. Эффект неподеленной пары свинца можно наблюдать в супрамолекулярных комплексах нитрата свинца (II) , а в 2007 году исследование связало неподеленную пару с отравлением свинцом . [12] Ионы свинца могут заменять нативные ионы металлов в нескольких ключевых ферментах, таких как катионы цинка в ферменте ALAD , который также известен как порфобилиногенсинтаза и играет важную роль в синтезе гема , ключевого компонента переносящего кислород молекула гемоглобина . Это ингибирование синтеза гема, по-видимому, является молекулярной основой отравления свинцом (также называемого «сатурнизмом» или «плюмбизмом»). [13] [14] [15]
Вычислительные эксперименты показывают, что, хотя координационное число не меняется при замене в кальций-связывающих белках, введение свинца искажает способ организации лигандов для размещения такой возникающей неподеленной пары: следовательно, эти белки нарушаются. Этот эффект неподеленной пары становится драматичным для цинк-связывающих белков, таких как вышеупомянутая порфобилиногенсинтаза, поскольку природный субстрат больше не может связываться – в этих случаях белок ингибируется .
В элементах группы 14 ( углеродная группа ) неподеленные пары могут проявляться путем укорочения или удлинения длин одинарных связей ( порядок связи 1), [16] , а также в эффективном порядке тройных связей . [17] [18] Знакомые алкины имеют тройную связь углерод-углерод ( 3-й порядок связи ) и линейную геометрию валентных углов 180° (рисунок A в ссылке [19] ). Однако ниже в группе ( кремний , германий и олово ) формальные тройные связи имеют эффективный порядок связи 2 с одной неподеленной парой (рисунок B [19] ) и транс -изогнутую геометрию. В свинце эффективный порядок связей еще больше сводится к одинарной связи с двумя неподеленными парами для каждого атома свинца (рисунок C [19] ). В германийорганическом соединении ( схема 1 в ссылке) эффективный порядок связи также равен 1, с комплексообразованием кислых изонитрильных ( или изоцианидных ) групп CN, основанным на взаимодействии с пустой 4p-орбиталью германия. [19] [20]

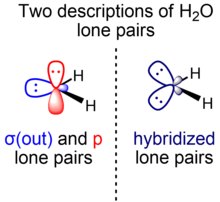
В курсах элементарной химии неподеленные пары воды описываются как «кроличьи уши»: две эквивалентные электронные пары, находящиеся примерно в гибридизации sp 3 , а валентный угол HOH составляет 104,5°, что немного меньше идеального тетраэдрического угла arccos(–1/). 3) ≈ 109,47°. Меньший валентный угол рационализируется теорией VSEPR , приписывая большее пространство для двух идентичных неподеленных пар по сравнению с двумя связывающими парами. В более продвинутых курсах альтернативное объяснение этого явления рассматривает большую стабильность орбиталей с избыточным характером s с использованием теории изовалентной гибридизации , в которой связи и неподеленные пары могут быть построены с помощью гибридов sp x , где допускаются нецелые значения x , поэтому до тех пор, пока общее количество символов s и p сохраняется (одна s и три p-орбитали в случае элементов p-блока второй строки).
Чтобы определить гибридизацию кислородных орбиталей, используемых для образования связывающих пар и неподеленных пар воды на этом рисунке, мы используем формулу 1 + x cos θ = 0, которая связывает валентный угол θ с индексом гибридизации x . Согласно этой формуле связи O–H считаются построенными из O-связывающих орбиталей гибридизации ~sp 4.0 (~80% p-характер, ~20% s-характер), что оставляет после себя неподеленные пары O-орбиталей гибридизации ~sp 2.3 . (~70% символа p, ~30% символа s). Эти отклонения от идеализированной sp 3- гибридизации (75% символа p, 25% символа s) для тетраэдрической геометрии согласуются с правилом Бента : неподеленные пары локализуют большую электронную плотность ближе к центральному атому по сравнению со связывающими парами; следовательно, использование орбиталей с избыточным s-характером для образования неподеленных пар (и, следовательно, с избыточным p-характером для образования связывающих пар) энергетически выгодно.
Однако теоретики часто предпочитают альтернативное описание воды, разделяющее неподеленные пары воды по симметрии относительно молекулярной плоскости. В этой модели существуют две энергетически и геометрически различные неподеленные пары воды, обладающие разной симметрией: одна (σ) плоскостная и симметричная относительно плоскости молекулы, а другая (π) перпендикулярная и антисимметричная относительно молекулярной плоскости. самолет. Неподеленная пара σ-симметрии (σ(out)) образуется из гибридной орбитали, которая смешивает символы 2s и 2p, в то время как неподеленная пара π-симметрии (p) имеет исключительное происхождение от 2p-орбитали. Орбиталь неподеленной пары O σ(out), богатая s-символами (также обозначаемая n O (σ) ), представляет собой гибрид ~ sp 0,7 (~ 40% символов p, 60% символов s), в то время как орбиталь неподеленной пары p (также обозначаемая n O (π) ) состоит из 100% символа p.
Обе модели имеют ценность и представляют одну и ту же полную электронную плотность с орбиталями, связанными унитарным преобразованием . В этом случае мы можем построить две эквивалентные неподеленные гибридные орбитали h и h ', взяв линейные комбинации h = c 1 σ(out) + c 2 p и h ' = c 1 σ(out) – c 2 p для соответствующий выбор коэффициентов c 1 и c 2 . Для химических и физических свойств воды, которые зависят от общего распределения электронов в молекуле, использование h и h ' так же справедливо, как и использование σ(out) и p. В некоторых случаях такое представление интуитивно полезно. Например, стереоэлектронные требования для аномерного эффекта могут быть рационализированы с использованием эквивалентных неподеленных пар, поскольку имеет значение общий вклад электронной плотности в разрыхляющую орбиталь. Альтернативный подход с использованием разделенных σ/π неподеленных пар также действителен, но он требует достижения баланса между максимальным перекрытием n O (π) -σ* (максимум при двугранном угле 90 °) и перекрытием n O (σ) -σ* ( максимум при двугранном угле 0 °), компромисс, который приводит к выводу, что конформация гош (двугранный угол 60 °) является наиболее предпочтительной, тот же вывод, который модель эквивалентных неподеленных пар объясняет гораздо более простым способом. [21] Точно так же водородные связи воды образуются вдоль направлений неподеленных пар «кроличьих ушей», что является отражением повышенной доступности электронов в этих областях. Эта точка зрения поддерживается вычислительно. [5] Однако, поскольку только канонические орбитали, адаптированные к симметрии, имеют физически значимые энергии, явления, связанные с энергиями отдельных орбиталей, такие как фотохимическая реактивность или фотоэлектронная спектроскопия , легче всего объяснить с использованием неподеленных пар σ и π, которые соблюдают молекулярная симметрия. [21] [22]
Из-за популярности теории VSEPR , отношение к неподеленным парам воды как к эквивалентам преобладает во вводных курсах химии, и многие практикующие химики продолжают рассматривать ее как полезную модель. Аналогичная ситуация возникает при описании двух неподеленных пар карбонильного атома кислорода кетона. [23] Однако вопрос о том, полезно ли концептуально выводить эквивалентные орбитали из адаптированных по симметрии орбиталей с точки зрения теории связей и педагогики, до сих пор остается спорным, причем недавние (2014 и 2015 гг.) статьи противостоят [24] и поддержка [25] этой практики.
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка ) CS1 maint: несколько имен: список авторов ( ссылка )