Церебральный шунт — это устройство, постоянно имплантируемое в голову и тело для отвода лишней жидкости из мозга. Их обычно используют для лечения гидроцефалии — отека головного мозга из-за избыточного накопления спинномозговой жидкости (СМЖ). Если его не остановить, избыток спинномозговой жидкости может привести к повышению внутричерепного давления (ВЧД), что может вызвать внутричерепную гематому , отек мозга , раздавливание тканей головного мозга или грыжу . [1] Дренаж, обеспечиваемый шунтом, может облегчить или предотвратить эти проблемы у пациентов с гидроцефалией или связанными с ней заболеваниями.
Шунты бывают самых разных форм, но большинство из них состоят из корпуса клапана, соединенного с катетером, нижний конец которого обычно помещается в брюшную полость . Основные различия между шунтами обычно заключаются в материалах, используемых для их изготовления, типах используемых клапанов (если таковые имеются), а также в том, является ли клапан программируемым или нет. [2]
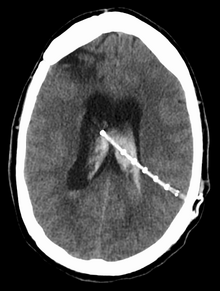

Местоположение шунта определяется нейрохирургом в зависимости от типа и местоположения закупорки, вызывающей гидроцефалию. Все желудочки головного мозга являются кандидатами на шунтирование. Катетер чаще всего устанавливают в брюшную полость, но могут быть и в сердце и легких. [10] Шунты часто называют по маршруту, используемому нейрохирургом. Дистальный конец катетера может быть расположен практически в любой ткани с достаточным количеством эпителиальных клеток для поглощения поступающей спинномозговой жидкости. Ниже приведены некоторые распространенные планы маршрутизации церебральных шунтов.
Он расположен на теменной кости, над ламбдовидным швом, на 3–4 см латеральнее средней линии и на 6 см выше ионической кости . [11] Это обычное место для желудочковой канюляции в контексте установки вентрикулоперитонеального шунта для лечения гидроцефалии. Впервые он был описан CH Frazier в 1928 году. [12]
Подапоневротический шунт обычно является временной мерой, используемой у младенцев, которые слишком малы или недоношенны, чтобы переносить другие типы шунтов. Хирург формирует карман под эпикраниальным апоневрозом (подапоневротическим пространством) и позволяет спинномозговой жидкости вытекать из желудочков, создавая заполненную жидкостью опухоль на коже головы ребенка. Эти шунты обычно преобразуются в шунты VP или другие типы, когда ребенок становится достаточно большим. [13]
Ниже приведен краткий список известных осложнений, которые могут привести к гидроцефалии, требующей шунтирования.
Установка шунта связана с рядом осложнений. Многие из этих осложнений возникают в детстве и прекращаются, когда пациент достигает зрелого возраста. Многие осложнения требуют немедленной ревизии шунта (замены или перепрограммирования уже существующего шунта). Общие симптомы часто напоминают новое начало гидроцефалии, например, головные боли, тошнота, рвота, двоение в глазах и изменение сознания. Это может привести к повреждению кратковременной памяти человека. [10] В педиатрической популяции частота отказов шунта через два года после имплантации оценивается в 50%. [23] Пациенты пожилого возраста, длительного пребывания в стационаре, оценки по шкале GCS менее 13, экстравентрикулярного дренирования in situ или удаления опухолей головного мозга с большей вероятностью имеют раннюю недостаточность шунта. [24]
Инфекция является распространенным осложнением, которое обычно поражает педиатрических пациентов, поскольку у них еще не выработан иммунитет к ряду различных заболеваний. Обычно частота заражения снижается по мере взросления пациента и формирования иммунитета организма к различным инфекционным агентам. [10] Инфекция шунта может возникнуть у 27% пациентов. Инфекция может привести к долгосрочным когнитивным дефектам, неврологическим проблемам и в некоторых случаях к смерти. Общие микробные агенты, вызывающие шунтовую инфекцию, включают Staphylococcus epidermidis , Staphylococcus aureus и Candida albicans . Дополнительные факторы, которые могут привести к инфекции шунта, включают установку шунта в молодом возрасте (менее шести месяцев) и тип гидроцефалии, которую лечат. Нет сильной корреляции между инфекцией и типом шунта. [25] Хотя симптомы шунтовой инфекции в целом аналогичны симптомам, наблюдаемым при гидроцефалии, симптомы инфекции также могут включать лихорадку и повышенное количество лейкоцитов. [26]
Лечение инфекции СМЖ-шунта обычно включает удаление шунта и установку временного желудочкового резервуара до тех пор, пока инфекция не будет устранена. [27] [28] Существует четыре основных метода лечения вентрикулоперитонеальных (ВП) шунтирующих инфекций: (1) антибиотики; (2) удаление инфицированного шунта с немедленной заменой; (3) экстернализация шунта с возможной заменой; (4) удаление инфицированного шунта с установкой наружного желудочкового дренажа (EVD) и возможной повторной установкой шунта. Последний метод имеет самый высокий показатель успеха – более 95%. [29]
Начальная эмпирическая терапия шунтирующей инфекции спинномозговой жидкости должна включать широкий охват антибиотиками грамотрицательных аэробных бацилл, включая псевдомонады, а также грамположительных микроорганизмов, включая Staphylococcus aureus и коагулазонегативные стафилококки, например, комбинацию цефтазидима и ванкомицина. Некоторые врачи добавляют парентеральные или интратекальные аминогликозиды для усиления покрытия псевдомонадой, хотя эффективность аминогликозидов не ясна. Меропенем и азтреонам являются дополнительными вариантами антибиотиков, эффективными против грамотрицательных бактериальных инфекций. [30]
Чтобы оценить пользу хирургического удаления или экстернализации шунта с последующим удалением, Wong et al. сравнили две группы: одну, получавшую только медикаментозное лечение, и другую, получавшую одновременно медикаментозное и хирургическое лечение. Обследованы 28 пациентов с инфекцией после имплантации вентрикулоперитонеального шунта в течение 8 лет в нейрохирургическом центре. 17 из этих пациентов лечились удалением шунта или экстернализацией с последующим удалением в дополнение к внутривенным антибиотикам, тогда как остальные 11 лечились только внутривенными антибиотиками. В группе, получавшей как хирургическое удаление шунта, так и антибиотики, смертность была ниже – 19% против 42% (р = 0,231). Несмотря на то, что эти результаты не являются статистически значимыми, Wong et al. предлагают лечить инфекции VP-шунта как хирургическим, так и медикаментозным способом. [31]
Анализ 17 исследований, опубликованных за последние 30 лет в отношении детей с инфекциями ликворного шунта, показал, что лечение с помощью удаления шунта и применения антибиотиков успешно излечило 88% из 244 инфекций, в то время как только антибиотикотерапия успешно излечила инфекцию ликворного шунта только в 33% из 230. инфекции. [28] [32]
В то время как типичные хирургические методы лечения инфекций VP-шунта включают удаление и реимплантацию шунта, у некоторых пациентов с успехом применяются различные типы операций. Стейнбок и др. лечил случай рецидивирующей инфекции VP-шунта у экзематозного пациента с помощью вентрикуло-подапогеального шунта в течение двух месяцев до полного излечения экземы. Этот тип шунта позволил им избежать участка пораженной кожи, который послужил источником инфекции. [29] Джонс и др. пролечили 4 пациентов с несообщающейся гидроцефалией, у которых были инфекции VP-шунта, с удалением шунта и третьей вентрикулостомией. Эти пациенты были излечены от инфекции и не нуждались в повторной установке шунта, что свидетельствует об эффективности этой процедуры у таких пациентов. [33]
Другой основной причиной отказа шунта является закупорка шунта на проксимальном или дистальном конце. На проксимальном конце шунтирующий клапан может блокироваться из-за накопления избытка белка в спинномозговой жидкости. Лишний белок будет собираться в месте дренажа и медленно закупоривать клапан. Шунт также может заблокироваться на дистальном конце, если шунт вытянут из брюшной полости (в случае шунтов VP) или из-за аналогичного скопления белка. Другими причинами закупорки являются чрезмерный дренаж и синдром щелевого желудочка. [10]
Чрезмерный дренаж возникает, когда шунт не предназначен для конкретного пациента. Чрезмерный дренаж может привести к ряду различных осложнений, некоторые из которых описаны ниже.
Обычно может возникнуть один из двух типов чрезмерного дренажа. Во-первых, когда спинномозговая жидкость дренируется слишком быстро, может возникнуть состояние, известное как экстрааксиальное скопление жидкости. В этом состоянии мозг коллапсирует сам по себе, что приводит к скоплению спинномозговой жидкости или крови вокруг мозга. Это может привести к серьезному повреждению головного мозга из-за сдавления головного мозга и развитию субдуральной гематомы . Внеосевое скопление жидкости можно лечить тремя различными способами в зависимости от тяжести состояния. Обычно шунт заменяют или перепрограммируют для высвобождения меньшего количества спинномозговой жидкости, а жидкость, скопившуюся вокруг мозга, удаляется. Второе состояние, известное как синдром щелевого желудочка, возникает, когда СМЖ медленно истощается в течение нескольких лет. Более подробную информацию о синдроме щелевого желудочка можно найти ниже. [10] [34]
Недавние исследования показали, что чрезмерное дренирование спинномозговой жидкости из-за шунтирования может привести к приобретенной мальформации Киари I. [35] Ранее считалось, что мальформация Киари I является результатом врожденного дефекта, но новые исследования показали, что чрезмерное дренирование кистоперитонеальных шунтов, используемых для лечения арахноидальных кист, может привести к развитию переполненности задней ямки и грыжи миндалин , последнее из них является классическим определением мальформации Киари I. Общие симптомы включают сильные головные боли, потерю слуха, утомляемость, мышечную слабость и потерю функции мозжечка. [36]
Синдром щелевого желудочка — редкое заболевание, связанное с шунтирующими пациентами, но приводящее к большому количеству ревизий шунта. Заболевание обычно возникает через несколько лет после имплантации шунта. Наиболее распространенные симптомы аналогичны нормальной неисправности шунта, но есть несколько ключевых отличий. Во-первых, симптомы часто носят циклический характер и появляются, а затем исчезают несколько раз в течение жизни. Во-вторых, симптомы можно облегчить, лежа на животе. В случае неисправности шунта ни время, ни положение позы не влияют на симптомы. [37]
Часто считается, что это состояние возникает в период, когда одновременно происходит чрезмерный дренаж и рост мозга. В этом случае мозг заполняет внутрижелудочковое пространство, оставляя желудочки спавшимися. Кроме того, податливость мозга уменьшится, что препятствует расширению желудочков, что снижает вероятность излечения синдрома. Коллапсированные желудочки также могут блокировать шунтирующий клапан, что приводит к обструкции. Поскольку последствия синдрома щелевого желудочка необратимы, необходим постоянный уход за этим состоянием. [34] [35]
Внутрижелудочковое кровоизлияние может произойти в любой момент во время или после установки или ревизии шунта. В педиатрической популяции после вентрикулоперитонеального шунтирования также были описаны внутрипаренхиматозные кровоизлияния, носящие мультифокальный характер. [38] Кровоизлияние может вызвать нарушение функции шунта, что может привести к тяжелым неврологическим нарушениям. [35] Исследования показали, что внутрижелудочковое кровоизлияние может возникнуть почти в 31% случаев ревизии шунта. [39]
Хотя было много случаев, когда пациенты достигали «независимости от шунта», среди врачей нет общего согласия относительно того, как определить, какие пациенты могут выжить без шунта. Может быть очень трудно определить, может ли пациент быть независимым от шунта, за исключением некоторых очень специфических обстоятельств. В целом, окончательное удаление шунта — редкая, но не беспрецедентная процедура. [40]