Газообразный хлор можно получать путем извлечения из природных материалов, в том числе электролизом раствора хлорида натрия ( рассола ) и другими способами.
Хлор может быть получен электролизом раствора хлорида натрия ( рассола ), который известен как процесс Chloralkali . Производство хлора приводит к побочным продуктам каустической соды ( гидроксид натрия , NaOH) и газообразного водорода (H2 ) . Эти два продукта, как и сам хлор, являются высокореактивными. Хлор также может быть получен электролизом раствора хлорида калия , в этом случае побочными продуктами являются водород и едкое кали ( гидроксид калия ). Существует три промышленных метода извлечения хлора электролизом хлоридных растворов, все из которых протекают по следующим уравнениям:
Общий процесс: 2 NaCl (или KCl) + 2 H 2 O → Cl 2 + H 2 + 2 NaOH (или KOH)
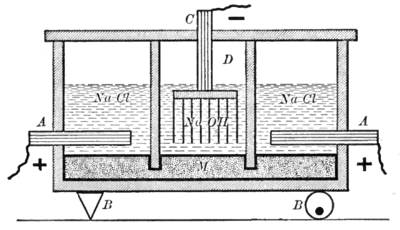
Электролиз в ртутной ячейке, также известный как процесс Кастнера-Кельнера , был первым методом, использованным в конце девятнадцатого века для производства хлора в промышленных масштабах. [1] [2] Используемые «качающиеся» ячейки были усовершенствованы с годами. [3] Сегодня в «первичной ячейке» титановые аноды, покрытые платиной [4] или проводящими оксидами металлов (ранее графитовые аноды), помещаются в раствор хлорида натрия (или калия), протекающий по жидкому ртутному катоду . Когда прикладывается разность потенциалов и протекает ток, хлор выделяется на титановом аноде , а натрий (или калий ) растворяется в ртутном катоде, образуя амальгаму . Она непрерывно течет в отдельный реактор («денюдер» или «вторичная ячейка»), где она обычно преобразуется обратно в ртуть путем реакции с водой , производя водород и гидроксид натрия (или калия) в коммерчески полезной концентрации (50% по весу). Затем ртуть возвращается в первичную ячейку с помощью насоса, расположенного внизу.
Ртутный процесс является наименее энергоэффективным из трех основных технологий (ртутный, диафрагменный и мембранный ), и существуют также опасения по поводу выбросов ртути .
По оценкам, в мире все еще работает около 100 предприятий с ртутными ячейками. В Японии производство хлорщелочного производства на основе ртути было фактически прекращено к 1987 году (за исключением двух последних установок по производству хлорида калия, закрытых в 2003 году). В Соединенных Штатах к концу 2008 года в эксплуатации останется всего пять ртутных предприятий. В Европе ртутные ячейки составляли 43% мощности в 2006 году, а западноевропейские производители взяли на себя обязательство закрыть или переоборудовать все оставшиеся предприятия по производству хлорщелочного производства ртути к 2020 году. [5]
В электролизе с диафрагмой асбестовая (или полимерно-волокнистая) диафрагма разделяет катод и анод, предотвращая повторное смешивание хлора, образующегося на аноде, с гидроксидом натрия и водородом, образующимися на катоде. [6] Эта технология также была разработана в конце девятнадцатого века. Существует несколько вариантов этого процесса: ячейка Ле Сюэра (1893), ячейка Харгривза-Берда (1901), ячейка Гиббса (1908) и ячейка Таунсенда (1904). [7] [8] Ячейки различаются по конструкции и размещению диафрагмы, причем в некоторых диафрагма находится в прямом контакте с катодом.
Раствор соли непрерывно подается в анодное отделение и протекает через диафрагму в катодное отделение, где образуется едкая щелочь , а рассол частично истощается. В результате диафрагменные методы производят щелочь, которая является довольно разбавленной (около 12%) и имеет меньшую чистоту, чем методы ртутных ячеек.
Диафрагменные ячейки не обременены проблемой предотвращения выброса ртути в окружающую среду; они также работают при более низком напряжении , что приводит к экономии энергии по сравнению с методом ртутных ячеек [8] , но требуются большие объемы пара , если каустическую соду необходимо испарить до коммерческой концентрации 50%.
Разработка этой технологии началась в 1970-х годах. Электролизер разделен на две «секции» катионопроницаемой мембраной , действующей как катионообменник . Насыщенный раствор хлорида натрия (или калия) пропускается через анодное отделение, выходя при более низкой концентрации . [9] Раствор гидроксида натрия (или калия) циркулирует через катодное отделение, выходя при более высокой концентрации. Часть концентрированного раствора гидроксида натрия, выходящего из электролизера, отводится в качестве продукта, а остальная часть разбавляется деионизированной водой и снова пропускается через электролизный аппарат.
Этот метод более эффективен, чем метод диафрагменной ячейки, и позволяет производить очень чистый гидроксид натрия (или калия) с концентрацией около 32%, но для этого требуется очень чистый рассол.

Хотя масштабы производства гораздо меньше, электролитические диафрагменные и мембранные технологии также используются в промышленности для извлечения хлора из растворов соляной кислоты , в результате чего в качестве побочного продукта получается водород (но не едкая щелочь).
Кроме того, электролиз расплавленных хлоридных солей ( процесс Даунса ) также позволяет получать хлор, в данном случае как побочный продукт производства металлического натрия или магния .
До того , как электролитические методы стали использоваться для производства хлора, прямое окисление хлористого водорода кислородом (часто посредством воздействия воздуха) осуществлялось в процессе Дикона :
Эта реакция осуществляется с использованием хлорида меди(II) (CuCl2 ) в качестве катализатора и проводится при высокой температуре (около 400 °C). Количество извлеченного хлора составляет приблизительно 80%. Из-за чрезвычайно едкой реакционной смеси промышленное использование этого метода затруднено, и несколько пилотных испытаний в прошлом потерпели неудачу. Тем не менее, недавние разработки являются многообещающими. Недавно Sumitomo запатентовала катализатор для процесса Deacon с использованием оксида рутения(IV) (RuO2 ) . [10]
Другим более ранним способом получения хлора было нагревание рассола с кислотой и диоксидом марганца .
Используя этот процесс, химик Карл Вильгельм Шееле был первым, кто выделил хлор в лаборатории. Марганец может быть восстановлен с помощью процесса Уэлдона . [11]
Небольшие количества газообразного хлора можно получить в лаборатории, поместив концентрированную соляную кислоту в колбу с боковым отводом и присоединенной резиновой трубкой. Затем добавляют диоксид марганца и закупоривают колбу. Реакция не сильно экзотермическая. Поскольку хлор плотнее воздуха, его можно легко собрать, поместив трубку в колбу, где он вытеснит воздух. После заполнения собирающую колбу можно закупорить.
Другой метод получения небольших количеств газообразного хлора в лабораторных условиях — добавление концентрированной соляной кислоты (обычно около 5 М) к раствору гипохлорита натрия или хлората натрия .
Перманганат калия можно использовать для получения газообразного хлора при добавлении к соляной кислоте.
Крупномасштабное производство хлора включает несколько этапов и множество единиц оборудования. Ниже приведено типичное описание мембранной установки. Установка также одновременно производит гидроксид натрия (каустическую соду) и газообразный водород. Типичная установка состоит из производства/обработки рассола, операций с ячейками, охлаждения и сушки хлора, сжатия и сжижения хлора, хранения и загрузки жидкого хлора, обработки каустика, испарения, хранения и загрузки и обработки водорода.
Ключом к производству хлора является работа системы насыщения/очистки рассола. Поддержание правильно насыщенного раствора с правильной чистотой имеет жизненно важное значение, особенно для мембранных ячеек. На многих заводах есть соляная куча, которая опрыскивается переработанным рассолом. На других есть шламовые баки, в которые подается сырая соль и переработанный рассол. Сырой рассол обрабатывается карбонатом натрия и гидроксидом натрия для осаждения кальция и магния. Реакции часто проводятся в серии реакторов, прежде чем обработанный рассол отправляется в большой осветлитель , где карбонат кальция и гидроксид магния осаждаются. Флокулянт может быть добавлен непосредственно перед осветлителем для улучшения осаждения. Затем декантированный рассол механически фильтруется с помощью песчаных фильтров или листовых фильтров перед поступлением в серию ионообменников для дальнейшего удаления примесей . На нескольких этапах этого процесса рассол проверяется на твердость и прочность.
После ионообменников рассол считается чистым и перекачивается в резервуары для хранения, чтобы быть закачанным в камеру. Чистый рассол нагревается до нужной температуры для контроля температуры рассола на выходе в соответствии с электрической нагрузкой . Рассол, выходящий из камеры, должен быть обработан для удаления остаточного хлора и контроля уровня pH перед возвращением на стадию насыщения . Это можно сделать с помощью башен дехлорирования с добавлением кислоты и бисульфита натрия . Неспособность удалить хлор может привести к повреждению ионообменных блоков. Рассол следует контролировать на предмет накопления как хлорат-анионов , так и сульфат-анионов , и либо иметь систему очистки, либо продувать контур рассола для поддержания безопасных уровней, поскольку хлорат-анионы могут диффундировать через мембраны и загрязнять каустическую соду, в то время как сульфат-анионы могут повредить покрытие поверхности анода.
Здание, в котором размещаются многочисленные электролитические ячейки, обычно называют ячеечным помещением или ячеечным домом, хотя некоторые установки строятся на открытом воздухе. Это здание содержит опорные конструкции для ячеек, соединения для подачи электроэнергии к ячейкам и трубопроводы для жидкостей. Мониторинг и контроль температур исходного каустика и рассола осуществляется для контроля выходных температур. Также контролируются напряжения каждой ячейки, которые изменяются в зависимости от электрической нагрузки на ячеечное помещение, которое используется для контроля скорости производства. Мониторинг и контроль давления в коллекторах хлора и водорода также осуществляется с помощью клапанов регулирования давления .
Постоянный ток подается через выпрямленный источник питания. Нагрузка установки регулируется путем изменения тока на ячейках. По мере увеличения тока увеличиваются скорости потока рассола, каустической и деионизированной воды , при этом снижаются температуры подачи.
Выходящий из линии ячеек хлорный газ должен быть охлажден и высушен, поскольку температура выходящего газа может превышать 80 °C и содержать влагу, из-за которой хлорный газ может вызывать коррозию железных труб. Охлаждение газа позволяет большому количеству влаги из рассола конденсироваться из газового потока. Охлаждение также повышает эффективность как сжатия , так и последующей стадии сжижения . Выход хлора в идеале находится между 18 °C и 25 °C. После охлаждения газовый поток проходит через ряд башен с противоточной серной кислотой . Эти башни постепенно удаляют всю оставшуюся влагу из хлорного газа. После выхода из сушильных башен хлор фильтруется для удаления всей оставшейся серной кислоты.
Могут использоваться несколько методов сжатия: жидкостное кольцо , возвратно-поступательное движение или центробежное . На этом этапе газообразный хлор сжимается и может быть дополнительно охлажден промежуточными и конечными охладителями. После сжатия он поступает в сжижители, где охлаждается достаточно для сжижения. Неконденсирующиеся газы и оставшийся газообразный хлор сбрасываются в ходе контроля давления в системах сжижения. Эти газы направляются в газоочиститель, производящий гипохлорит натрия , или используются в производстве соляной кислоты (путем сжигания с водородом) или дихлорида этилена (путем реакции с этиленом ).
Жидкий хлор обычно подается в резервуары самотеком. Его можно загружать в железнодорожные или автомобильные цистерны с помощью насосов или заполнять сжатым сухим газом.
Каустик, подаваемый в камеру ячейки, течет в петле, которая одновременно отводится в хранилище с частью, разбавленной деионизированной водой, и возвращается в линию ячеек для укрепления внутри ячеек. Каустик, выходящий из линии ячеек, должен контролироваться на прочность, чтобы поддерживать безопасные концентрации. Слишком сильный или слишком слабый раствор может повредить мембраны. Мембранные ячейки обычно производят каустик в диапазоне от 30% до 33% по весу. Поток подаваемого каустика нагревается при низких электрических нагрузках для контроля его температуры на выходе. Более высокие нагрузки требуют охлаждения каустика для поддержания правильной температуры на выходе. Каустик, выходящий в хранилище, извлекается из резервуара для хранения и может быть разбавлен для продажи клиентам, которым требуется слабый каустик, или для использования на месте. Другой поток может быть закачан в многокорпусный испаритель для производства коммерческой 50% каустика. Железнодорожные вагоны и автоцистерны загружаются на станциях загрузки с помощью насосов.
Водород, полученный в качестве побочного продукта, может быть выброшен в атмосферу необработанным или охлажденным, сжатым и высушенным для использования в других процессах на месте или продан потребителю по трубопроводу, в баллонах или грузовиках. Некоторые возможные применения включают производство соляной кислоты или перекиси водорода , а также десульфурацию нефти или использование в качестве топлива в котлах или топливных элементах .
Производство хлора является чрезвычайно энергоемким. [12] Потребление энергии на единицу веса продукта не намного ниже, чем при производстве чугуна и стали [13] и больше, чем при производстве стекла [14] или цемента. [15]
Поскольку электричество является незаменимым сырьем для производства хлора, потребление энергии, соответствующее электрохимической реакции, не может быть уменьшено. Экономия энергии возникает в первую очередь за счет применения более эффективных технологий и сокращения использования вспомогательной энергии. Выбросы парниковых газов всего процесса, таким образом, во многом зависят от способа производства электроэнергии. Если используются гидроэнергетика , атомная энергетика или другие источники с низким содержанием углерода, выбросы будут намного ниже, чем при использовании ископаемого топлива .