В химии абсорбция — это физическое или химическое явление или процесс , в котором атомы , молекулы или ионы входят в некоторую объемную фазу — жидкий или твердый материал. Это процесс, отличный от адсорбции , поскольку поглощающиеся молекулы захватываются объемом, а не поверхностью (как в случае адсорбции).
Более распространенное определение гласит: «Абсорбция — это химическое или физическое явление, при котором молекулы, атомы и ионы поглощаемого вещества входят в объемную фазу (газовую, жидкую или твердую) материала, в котором оно поглощается».
Более общий термин — сорбция , который охватывает абсорбцию, адсорбцию и ионный обмен . Абсорбция – это состояние, при котором что-то поглощает другое вещество. [1]
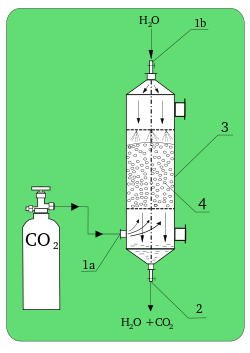
Во многих важных в технике процессах вместо физического процесса используется химическая абсорбция, например поглощение углекислого газа гидроксидом натрия, — такие кислотно-основные процессы не подчиняются закону распределения Нернста (см.: Растворимость ).
Некоторые примеры этого эффекта см. в разделе « Жидкостно-жидкостная экстракция» . Можно экстрагировать растворенное вещество из одной жидкой фазы в другую без химической реакции. Примерами таких растворенных веществ являются благородные газы и четырехокись осмия . [1]
Процесс поглощения означает, что вещество захватывает и преобразует энергию. Абсорбент распределяет захватываемый им материал по всему объему, а адсорбент распределяет его только по поверхности.
Процесс проникновения газа или жидкости в тело адсорбента широко известен как абсорбция.
Если поглощение представляет собой физический процесс, не сопровождающийся каким-либо другим физическим или химическим процессом, оно обычно подчиняется закону распределения Нернста :
Величина константы K N зависит от температуры и называется коэффициентом разделения . Это уравнение справедливо, если концентрации не слишком велики и если вид «х» не меняет свою форму ни в одной из двух фаз «1» или «2». Если такая молекула претерпевает ассоциацию или диссоциацию , то это уравнение по-прежнему описывает равновесие между «х» в обеих фазах, но только для одной и той же формы – концентрации всех остальных форм необходимо рассчитывать с учетом всех остальных равновесий. [1]
В случае поглощения газа его концентрацию можно рассчитать, используя, например, закон идеального газа : c = p/RT . Альтернативно вместо концентраций можно использовать парциальные давления .
Абсорбция – это процесс, который может быть химическим (реактивным) или физическим (нереактивным).
Химическая абсорбция или реактивная абсорбция – это химическая реакция между поглощаемыми и поглощающими веществами. Иногда это сочетается с физическим поглощением. Этот тип поглощения зависит от стехиометрии реакции и концентрации ее реагентов. Они могут осуществляться в различных установках, с широким спектром типов фазовых потоков и взаимодействий. В большинстве случаев РА проводят в тарельчатых или насадочных колонках. [2]
Гидрофильные твердые вещества, к которым относятся многие твердые вещества биологического происхождения, легко поглощают воду. Полярные взаимодействия между водой и молекулами твердого тела способствуют разделению воды на твердое вещество, что может обеспечить значительное поглощение водяного пара даже при относительно низкой влажности.
Волокно (или другой гидрофильный материал), подвергшееся воздействию атмосферы, обычно содержит некоторое количество воды, даже если оно кажется сухим . Воду можно удалить путем нагревания в печи, что приведет к измеримому уменьшению веса, который постепенно восстановится, если волокно будет возвращено в «нормальную» атмосферу. Этот эффект имеет решающее значение в текстильной промышленности, где доля воды в весе материала называется возвратом влаги . [3]