
Потенциал-управляемые ионные каналы представляют собой класс трансмембранных белков , которые образуют ионные каналы , которые активируются изменениями электрического мембранного потенциала вблизи канала. Мембранный потенциал изменяет конформацию белков каналов, регулируя их открытие и закрытие. Клеточные мембраны обычно непроницаемы для ионов , поэтому они должны диффундировать через мембрану через трансмембранные белковые каналы. Они играют решающую роль в возбудимых клетках, таких как нейронные и мышечные ткани, обеспечивая быструю и скоординированную деполяризацию в ответ на изменение напряжения . Расположенные вдоль аксона и в синапсе потенциалзависимые ионные каналы направленно распространяют электрические сигналы. Потенциал-управляемые ионные каналы обычно ион-специфичны, и были идентифицированы каналы, специфичные для ионов натрия (Na + ), калия (K + ), кальция (Ca2 + ) и хлорида (Cl- ) . [1] Открытие и закрытие каналов инициируется изменением концентрации ионов и, следовательно, градиента заряда между сторонами клеточной мембраны. [2]
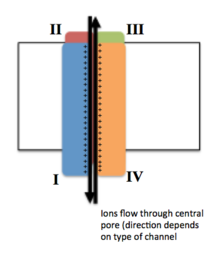
Потенциал-управляемые ионные каналы обычно состоят из нескольких субъединиц, расположенных таким образом, что имеется центральная пора, через которую ионы могут перемещаться вниз по своим электрохимическим градиентам . Каналы, как правило, специфичны для ионов, хотя иногда через них могут проходить ионы одинакового размера и заряда. Функциональность потенциалзависимых ионных каналов объясняется тремя его основными дискретными блоками: датчиком напряжения, порой или проводящим путем и воротами. [3] Каналы Na + , K + и Ca 2+ состоят из четырех трансмембранных доменов, расположенных вокруг центральной поры; эти четыре домена являются частью одной α-субъединицы в случае большинства каналов Na + и Ca2 + , тогда как в большинстве K + -каналов имеется четыре α-субъединицы, каждая из которых вносит свой вклад в один трансмембранный домен . [4] Все мембранные сегменты, обозначенные S1-S6, имеют форму альфа-спиралей со специализированными функциями. Пятый и шестой трансмембранные сегменты (S5 и S6) и поровая петля выполняют основную роль ионной проводимости, включая ворота и поры канала, а S1-S4 служат областью восприятия напряжения. [3] Четыре субъединицы могут быть идентичными или отличаться друг от друга. Помимо четырех центральных α-субъединиц существуют еще регуляторные β-субъединицы, обладающие оксидоредуктазной активностью, которые расположены на внутренней поверхности клеточной мембраны и не пересекают мембрану и которые собираются вместе с α-субъединицами в эндоплазматическая сеть . [5]
Кристаллографические структурные исследования калиевого канала показали, что когда над мембраной вводится разность потенциалов , связанное с ним электрическое поле вызывает конформационные изменения в калиевом канале. Конформационное изменение настолько искажает форму белков канала, что полость или канал открывается, обеспечивая приток или отток через мембрану. Это движение ионов вниз по градиенту концентрации впоследствии генерирует электрический ток , достаточный для деполяризации клеточной мембраны.
Потенциал-управляемые натриевые и кальциевые каналы состоят из одного полипептида с четырьмя гомологичными доменами. Каждый домен содержит 6 мембран, охватывающих альфа-спирали . Одна из этих спиралей, S4, является спиралью, чувствительной к напряжению. [6] Сегмент S4 содержит много положительных зарядов, поэтому высокий положительный заряд снаружи клетки отталкивает спираль, удерживая канал в закрытом состоянии.
В общем, часть ионного канала, чувствительная к напряжению, отвечает за обнаружение изменений трансмембранного потенциала, которые вызывают открытие или закрытие канала. Обычно считается, что эту роль выполняют альфа-спирали S1-4. В калиевых и натриевых каналах потенциал-чувствительные спирали S4 содержат положительно заряженные остатки лизина или аргинина в повторяющихся мотивах. [3] В состоянии покоя половина каждой спирали S4 контактирует с цитозолем клетки. При деполяризации положительно заряженные остатки доменов S4 движутся к экзоплазматической поверхности мембраны. Считается, что первые четыре аргинина отвечают за ток управления, движущийся к внеклеточному растворителю при активации канала в ответ на деполяризацию мембраны. Движение 10–12 из этих связанных с белком положительных зарядов запускает конформационные изменения, которые открывают канал. [4] Точный механизм, посредством которого происходит это движение, в настоящее время не согласован, однако каноническая, транспортная, лопастная и скрученная модели являются примерами современных теорий. [7]
Движение датчика напряжения вызывает конформационное изменение ворот проводящего пути, контролируя поток ионов через канал. [3]
Основная функциональная часть потенциал-чувствительного белкового домена этих каналов обычно содержит область, состоящую из спиралей S3b и S4, известную как «лопатка» из-за ее формы, которая, по-видимому, представляет собой консервативную последовательность , взаимозаменяемую в широком диапазоне. клетки и виды. Подобная лопатка датчика напряжения также была обнаружена в семействе потенциал-чувствительных фосфатаз у различных видов. [8] Генная инженерия области лопасти из вида обитающих в вулкане архебактерий в калиевых каналах мозга крысы приводит к созданию полностью функционального ионного канала при условии, что вся неповрежденная лопасть будет заменена. [9] Эта « модульность » позволяет использовать простые и недорогие модельные системы для изучения функции этой области, ее роли в заболевании и фармацевтического контроля ее поведения, а не ограничиваться плохо охарактеризованными, дорогими и/или трудными для изучения. препараты. [10]
Хотя потенциалзависимые ионные каналы обычно активируются деполяризацией мембраны , некоторые каналы, такие как каналы ионов калия с внутренним выпрямителем , вместо этого активируются гиперполяризацией .
Считается, что затвор соединен с областями измерения напряжения каналов и, по-видимому, содержит механическое препятствие для потока ионов. [11] Хотя домен S6 считается сегментом, действующим как это препятствие, его точный механизм неизвестен. Возможные объяснения включают в себя: сегмент S6 совершает ножницеобразное движение, позволяя ионам проходить через него, [12] сегмент S6 распадается на два сегмента, позволяя ионам проходить через канал, [13] или канал S6 служит самими воротами. . [14] Механизм, с помощью которого движение сегмента S4 влияет на движение сегмента S6, до сих пор неизвестен, однако предполагается, что существует линкер S4-S5, движение которого позволяет открыть S6. [3]
Инактивация ионных каналов происходит в течение миллисекунд после открытия. Считается, что инактивация опосредуется внутриклеточными воротами, которые контролируют открытие пор внутри клетки. [15] Эти ворота выполнены в виде шара, привязанного к гибкой цепи . Во время инактивации цепочка складывается сама по себе, и шарик блокирует поток ионов через канал. [16] Быстрая инактивация напрямую связана с активацией, вызванной внутримембранными движениями сегментов S4, [17] хотя механизм, связывающий движение S4 и задействование ворот инактивации, неизвестен.
Натриевые каналы имеют схожие функциональные свойства во многих разных типах клеток. Хотя идентифицировано десять человеческих генов, кодирующих натриевые каналы, их функция обычно консервативна у разных видов и разных типов клеток. [17]
Поскольку идентифицировано шестнадцать различных генов кальциевых каналов человека, этот тип каналов различается по функциям в зависимости от типа клеток. Ca 2+ -каналы производят потенциалы действия аналогично Na + -каналам в некоторых нейронах. Они также играют роль в высвобождении нейромедиаторов в пресинаптических нервных окончаниях. В большинстве клеток Ca 2+ каналы регулируют широкий спектр биохимических процессов благодаря своей роли в контроле внутриклеточной концентрации Ca 2+ . [13]
Калиевые каналы представляют собой самый крупный и разнообразный класс потенциалзависимых каналов, в котором более 100 кодируют гены человека. Эти типы каналов существенно различаются по своим стробирующим свойствам; некоторые инактивируются очень медленно, а другие очень быстро. Эта разница во времени активации влияет на продолжительность и скорость срабатывания потенциала действия, что оказывает существенное влияние на электрическую проводимость по аксону, а также на синаптическую передачу. Калиевые каналы отличаются по структуре от других каналов тем, что они содержат четыре отдельные полипептидные субъединицы, тогда как другие каналы содержат четыре гомологичных домена, но на одной полипептидной единице. [7]
Хлоридные каналы присутствуют во всех типах нейронов. Основная ответственность за контроль возбудимости лежит на хлоридных каналах, которые способствуют поддержанию потенциала покоя клеток и помогают регулировать объем клеток. [1]
Потенциал-управляемые протонные каналы проводят токи, опосредованные ионами водорода в форме гидроксония , и активируются деполяризацией в зависимости от pH . Их функция заключается в удалении кислоты из клеток. [18] [19] [20]
Филогенетические исследования белков, экспрессируемых в бактериях, выявили существование суперсемейства потенциалзависимых натриевых каналов. [21] Последующие исследования показали, что множество других ионных каналов и переносчиков филогенетически связаны с потенциал-управляемыми ионными каналами, в том числе: