В химии гипервалентная молекула ( это явление иногда в просторечии называют расширенным октетом ) — это молекула , которая содержит один или несколько элементов главной группы, по-видимому, несущих более восьми электронов в своих валентных оболочках . Пентахлорид фосфора ( PCl 5 ), гексафторид серы ( SF 6 ), трифторид хлора ( ClF 3 ), хлорит ( ClO−2) ион в хлористой кислоте и трииодиде ( I−3) ион являются примерами гипервалентных молекул.
Гипервалентные молекулы были впервые формально определены Джереми И. Машером в 1969 году как молекулы, имеющие центральные атомы групп 15–18 с любой валентностью , кроме самой низкой (т.е. 3, 2, 1, 0 для групп 15, 16, 17, 18 соответственно, на основе правила октетов ). [1]
Существует несколько конкретных классов гипервалентных молекул:
Номенклатура NXL, введенная совместно исследовательскими группами Мартина , Ардуэнго и Кочи в 1980 году [2] , часто используется для классификации гипервалентных соединений элементов основной группы, где:
Примеры номенклатуры NXL включают:
Споры о природе и классификации гипервалентных молекул восходят к Гилберту Н. Льюису и Ирвингу Ленгмюру , а также к дебатам о природе химической связи в 1920-х годах. [3] Льюис поддерживал важность двухцентровой двухэлектронной связи (2c-2e) при описании гипервалентности, используя таким образом расширенные октеты для объяснения таких молекул. Используя язык орбитальной гибридизации, считалось, что связи таких молекул, как PF 5 и SF 6 , построены из sp 3 d n -орбиталей на центральном атоме. Ленгмюр, с другой стороны, поддерживал доминирование правила октетов и предпочитал использовать ионные связи для учета гипервалентности, не нарушая правила (например, « SF2+
42F − " для SF 6 ).
В конце 1920-х и 1930-х годах Сагден приводил доводы в пользу существования двухцентровой одноэлектронной (2c-1e) связи и, таким образом, рационализировал связь в гипервалентных молекулах без необходимости в расширенных октетах или характере ионной связи; в то время это было плохо принято. [3] В 1940-х и 1950-х годах Рандл и Пиментель популяризировали идею трехцентровой четырехэлектронной связи , которая, по сути, является той же концепцией, которую Сагден пытался продвигать десятилетиями ранее; Трехцентровую четырехэлектронную связь можно альтернативно рассматривать как состоящую из двух коллинеарных двухцентровых одноэлектронных связей, при этом оставшиеся два несвязывающих электрона локализованы на лигандах. [3]
Попытка фактически получить гипервалентные органические молекулы началась с Германа Штаудингера и Георга Виттига в первой половине двадцатого века, которые стремились бросить вызов существующей теории валентности и успешно получить гипервалентные молекулы с азотом и фосфором. [4] Теоретическая основа гипервалентности не была сформулирована до работы Дж. И. Мушера в 1969 году. [1]
В 1990 году Магнуссон опубликовал плодотворную работу, окончательно исключающую значение d-орбитальной гибридизации в связывании гипервалентных соединений элементов второго ряда. Это долгое время было предметом разногласий и путаницы при описании этих молекул с использованием теории молекулярных орбиталей . Частично путаница здесь возникает из-за того, что необходимо включать d-функции в базисные наборы, используемые для описания этих соединений (иначе это приведет к неоправданно высоким энергиям и искаженной геометрии), а вклад d-функции в молекулярную волновую функцию равен большой. Исторически эти факты интерпретировались как означающие, что в связывании должны участвовать d-орбитали. Однако Магнуссон в своей работе заключает, что вовлечение d-орбитали не связано с гипервалентностью. [5]
Тем не менее, исследование 2013 года показало, что, хотя ионная модель Пиментеля лучше всего объясняет связь гипервалентных частиц, энергетический вклад структуры расширенного октета также не равен нулю. В этом современном исследовании теории валентных связей связи дифторида ксенона было обнаружено, что ионные структуры составляют около 81% общей волновой функции, из которых 70% возникают из ионных структур, использующих только p-орбиталь ксенона, а 11% возникают из-за ионных структур, использующих только p-орбиталь ксенона. ионные структуры с использованием гибрида ксенона. Вклад формально гипервалентной структуры, использующей орбиталь sp 3 d-гибридизации на ксеноне, составляет 11% волновой функции, а дирадикальный вклад составляет оставшиеся 8%. Вклад sp 3 d в размере 11% приводит к чистой стабилизации молекулы на 7,2 ккал (30 кДж) моль -1 , [6] незначительную, но значительную часть общей энергии общей энергии связи (64 ккал (270 кДж) моль -1 ). [7] Другие исследования аналогичным образом обнаружили незначительный, но существенный энергетический вклад от расширенных октетных структур в SF 6 (17%) и XeF 6 (14%). [8]
Несмотря на отсутствие химического реализма, ИЮПАК рекомендует рисовать расширенные октетные структуры для функциональных групп, таких как сульфоны и фосфораны , чтобы избежать изображения большого количества формальных зарядов или частичных одинарных связей. [9]
Особый тип гипервалентных молекул — гипервалентные гидриды. Большинство известных гипервалентных молекул содержат заместители, более электроотрицательные, чем их центральные атомы. [10] [11] Гипервалентные гидриды представляют особый интерес, поскольку водород обычно менее электроотрицательен, чем центральный атом. Ряд компьютерных исследований был проведен на гидридах халькогенов [11] [12] [13] [14] [15] [16] и гидридах пниктогенов . [17] [18] [19] [20] [21] Недавно новое компьютерное исследование показало, что большинство гипервалентных галогенгидридов XH n могут существовать. Предполагается, что IH 3 и IH 5 достаточно стабильны, чтобы их можно было наблюдать или, возможно, даже выделить. [22]
И термин, и концепция гипервалентности до сих пор подвергаются критике. В 1984 году, в ответ на это общее противоречие, Пауль фон Раге Шлейер предложил заменить «гипервалентность» использованием термина «гиперкоординация» , поскольку этот термин не подразумевает какой-либо тип химической связи, и, таким образом, этого вопроса можно было бы вообще избежать. [3]
Сама концепция подверглась критике со стороны Рональда Гиллеспи , который на основе анализа функций локализации электронов написал в 2002 году, что «поскольку нет фундаментальной разницы между связями в гипервалентных и негипервалентных (октет Льюиса) молекулах, нет никаких оснований продолжайте использовать термин «гипервалент». [23]
Для гиперкоординированных молекул с электроотрицательными лигандами, такими как PF 5 , было продемонстрировано, что лиганды могут оттягивать достаточную электронную плотность от центрального атома, так что его чистое содержание снова составляет 8 электронов или меньше. С этой альтернативной точкой зрения согласуется тот факт, что гиперкоординированные молекулы на основе фторсодержащих лигандов, например PF 5 , не имеют гидридных аналогов, например фосфорана (PH 5 ), который неизвестен.
Ионная модель хорошо подходит для термохимических расчетов. Это предсказывает благоприятное экзотермическое образование PF.+
4Ф−
из трифторида фосфора PF 3 и фтора F 2 , тогда как аналогичная реакция с образованием PH+
4ЧАС−
не является благоприятным. [24]
Даррант предложил альтернативное определение гипервалентности, основанное на анализе карт зарядов атомов, полученных из атомов в теории молекул. [25] Этот подход определяет параметр, называемый эквивалентом валентных электронов, γ, как «формальное количество общих электронов в данном атоме, полученное любой комбинацией действительных форм ионного и ковалентного резонанса, которая воспроизводит наблюдаемое распределение заряда». Для любого конкретного атома X, если значение γ(X) больше 8, этот атом является гипервалентным. Используя это альтернативное определение, многие виды, такие как PCl 5 , SO2−
4и XeF 4 , которые по определению Мушера являются гипервалентными, переклассифицируются как гиперкоординированные, но не гипервалентные, из-за сильной ионной связи, которая оттягивает электроны от центрального атома. С другой стороны, некоторые соединения, которые обычно записываются ионными связями, чтобы соответствовать правилу октетов, такие как озон O 3 , закись азота NNO и N-оксид триметиламина (CH
3)
3НЕТ , оказываются действительно гипервалентными. Примеры расчетов γ для фосфатов PO3−
4(γ(P) = 2,6, негипервалентный) и ортонитрат NO3−
4(γ(N) = 8,5, гипервалентный) показаны ниже.

Ранние рассмотрения геометрии гипервалентных молекул выявили знакомые механизмы, которые хорошо объяснялись моделью атомных связей VSEPR . Соответственно, молекулы типа AB 5 и AB 6 будут иметь тригональную бипирамидальную и октаэдрическую геометрию соответственно. Однако для учета наблюдаемых валентных углов, длин связей и очевидного нарушения правила октета Льюиса было предложено несколько альтернативных моделей.
В 1950-х годах для объяснения молекулярной архитектуры была предложена трактовка гипервалентной связи с расширенной валентной оболочкой, в которой центральный атом пента- и гексакоординированных молекул будет использовать d-АО в дополнение к s- и p-АО. Однако успехи в изучении расчетов ab initio показали, что вклад d-орбиталей в гипервалентную связь слишком мал, чтобы описать свойства связи, и это описание теперь считается гораздо менее важным. [5] Было показано, что в случае гексакоординированного SF 6 d-орбитали не участвуют в образовании SF-связи, но перенос заряда между атомами серы и фтора и соответствующие резонансные структуры смогли объяснить гипервалентность (см. ниже). ).
Были предприняты попытки дополнительных модификаций правила октетов для включения ионных характеристик в гипервалентную связь. В качестве одной из таких модификаций в 1951 году была предложена концепция 3-центровой 4-электронной (3c-4e) связи , описывающая гипервалентную связь с качественной молекулярной орбиталью . Связь 3c-4e описывается как три молекулярные орбитали, образованные комбинацией атомной орбитали ap на центральном атоме и атомной орбитали каждого из двух лигандов на противоположных сторонах центрального атома. Только одна из двух пар электронов занимает молекулярную орбиталь, которая связана с центральным атомом, вторая пара является несвязывающей и занимает молекулярную орбиталь, состоящую только из атомных орбиталей двух лигандов. Эту модель, в которой сохраняется правило октетов, также отстаивал Мушер. [3]

Полное описание гипервалентных молекул возникает в результате рассмотрения теории молекулярных орбиталей с помощью квантово-механических методов. LCAO , например, в гексафториде серы, взяв за основу одну 3s-орбиталь серы, три 3p-орбитали серы и шесть линейных комбинаций октаэдрической геометрии, адаптированных к симметрии (SALC) орбиталей фтора, всего десять молекулярных образуются орбитали (четыре полностью занятых связывающих МО с самой низкой энергией, две полностью занятых несвязывающих МО с промежуточной энергией и четыре вакантных разрыхляющих МО с самой высокой энергией), обеспечивающих место для всех 12 валентных электронов. Это стабильная конфигурация только для молекул S X 6 , содержащих электроотрицательные атомы лиганда, такие как фтор, что объясняет, почему SH 6 не является стабильной молекулой. В связывающей модели две несвязывающие МО (1e g ) локализованы одинаково на всех шести атомах фтора.
Для гипервалентных соединений, в которых лиганды более электроотрицательны , чем центральный гипервалентный атом, резонансные структуры могут быть нарисованы не более чем с четырьмя связями ковалентных электронных пар и дополнены ионными связями, чтобы подчиняться правилу октетов. Например, в пентафториде фосфора (PF 5 ) могут быть созданы 5 резонансных структур, каждая с четырьмя ковалентными связями и одной ионной связью с большим весом в структурах, придающих ионный характер аксиальным связям, тем самым удовлетворяя правилу октетов и объясняя как наблюдаемые тригонально-бипирамидальная молекулярная геометрия и тот факт, что длина аксиальной связи (158 пм) больше экваториальной (154 пм). [26]
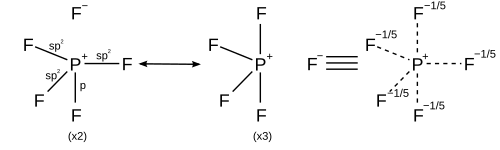
В гексакоординированной молекуле, такой как гексафторид серы , каждая из шести связей имеет одинаковую длину. Описанная выше рационализация может быть применена для создания 15 резонансных структур каждая с четырьмя ковалентными связями и двумя ионными связями, так что ионный характер равномерно распределяется по каждой из связей сера-фтор.

Теория спин-связанных валентных связей была применена к диазометану , и полученный орбитальный анализ был интерпретирован с точки зрения химической структуры, в которой центральный азот имеет пять ковалентных связей;

Это привело авторов к интересному выводу: «Вопреки тому, чему нас всех учили, когда мы были студентами, атом азота действительно образует пять ковалентных связей, и наличие или отсутствие d-орбиталей не имеет ничего общего с таким положением дел». [27]
Шестикоординированные молекулы фосфора , включающие лиганды азота, кислорода или серы, являются примерами гексакоординации кислоты Льюиса и основания Льюиса. [28] Для двух подобных комплексов, показанных ниже, длина связи C–P увеличивается с уменьшением длины связи N–P; прочность связи C–P уменьшается с увеличением силы взаимодействия N–P кислота Льюиса с основанием Льюиса.

Эта тенденция также в целом справедлива для пентакоординированных элементов основной группы с одним или несколькими лигандами, содержащими неподеленную пару, включая примеры кремния с пентакоординированным кислородом , показанные ниже.

Связи Si-галоген варьируются от ожидаемого значения Ван-дер-Ваальса в A (слабая связь) почти до ожидаемого значения ковалентной одинарной связи в C (сильная связь). [28]
Корриу и его коллеги провели раннюю работу, характеризующую реакции, которые, как считается, протекают через гипервалентное переходное состояние. [29] Измерения скоростей реакций гидролиза четырехвалентных хлорсиланов, инкубированных с каталитическими количествами воды, показали скорость первого порядка по хлорсилану и второго порядка по воде. Это указывало на то, что две молекулы воды взаимодействовали с силаном во время гидролиза, и на этом основании был предложен бинуклеофильный механизм реакции. Затем Корриу и его коллеги измерили скорость гидролиза в присутствии нуклеофильного катализатора HMPT, ДМСО или ДМФ. Было показано, что скорость гидролиза снова имеет первый порядок по хлорсилану, первый порядок по катализатору и теперь первый порядок по воде. Соответственно, скорости гидролиза также зависели от величины заряда кислорода нуклеофила.
В совокупности это привело группу к предложению механизма реакции, в котором происходит предопределяющая скорость нуклеофильная атака тетракоординированного силана нуклеофилом (или водой), в результате которой образуется гипервалентный пентакоординированный силан. За этим следует нуклеофильная атака промежуточного соединения водой на этапе, определяющем скорость, что приводит к образованию гексакоординированных частиц, которые быстро разлагаются с образованием гидроксисилана.
Гидролиз силана был дополнительно исследован Холмсом и его сотрудниками [30], в которых тетракоординированный Mes
2СиФ
2(Mes = мезитил ) и пентакоординированный Mes
2СиФ−
3прореагировали с двумя эквивалентами воды. По прошествии двадцати четырех часов почти не наблюдалось гидролиза тетракоординированного силана, тогда как пентакоординированный силан полностью гидролизовался через пятнадцать минут. Кроме того, данные рентгеновской дифракции, собранные для тетраэтиламмониевых солей фторсиланов, показали образование решетки бисилоната водорода, поддерживающей гексакоординированное промежуточное соединение, из которого HF−
2быстро вытесняется, приводя к гидроксилированному продукту. Эта реакция и кристаллографические данные подтверждают механизм, предложенный Корриу и др. .

Очевидная повышенная реакционная способность гипервалентных молекул по сравнению с четырехвалентными аналогами наблюдалась также для реакций Гриньяра. Группа Корриу измерила [31] периоды полураспада реакции Гриньяра с помощью ЯМР для родственных 18-краун-6 калиевых солей различных тетра- и пентакоординированных фторсиланов в присутствии каталитических количеств нуклеофила.
Хотя метод полуреакции является неточным, огромные различия в скоростях реакций позволили предложить предложенную схему реакции, в которой предварительная определяющая скорость атака четырехвалентного силана нуклеофилом приводит к равновесию между нейтральными тетракоординированными частицами и анионным пятивалентным соединением. За этим следует нуклеофильная координация с помощью двух реагентов Гриньяра, как обычно видно, с образованием гексакоординированного переходного состояния и получением ожидаемого продукта.

Механистические последствия этого распространяются на гексакоординированные виды кремния, которые, как полагают, активны в качестве переходного состояния в некоторых реакциях. Реакции аллил- или кротил -трифторсиланов с альдегидами и кетонами предшествует только фторидная активация с образованием пентакоординированного кремния. Это промежуточное соединение затем действует как кислота Льюиса, координируясь с карбонильным атомом кислорода. Дальнейшее ослабление связи кремний-углерод по мере того, как кремний становится гексакоординированным, помогает стимулировать эту реакцию. [32]

Подобная реакционная способность наблюдалась и для других гипервалентных структур, таких как смесь соединений фосфора, для которых были предложены гексакоординированные переходные состояния. Гидролиз фосфоранов и оксифосфоранов был изучен [33] и показал, что он протекает второго порядка в воде. Бельский и др. . предложили нуклеофильную атаку воды, определяющую предварительную скорость, приводящую к равновесию между пента- и гексакоординированными видами фосфора, за которым следует перенос протона с участием второй молекулы воды на стадии раскрытия кольца, определяющей скорость, что приводит к гидроксилированному продукту.

Также предполагается, что алкоголиз пентакоординированных соединений фосфора, таких как триметоксифосфолен с бензиловым спиртом, происходит через такое же октаэдрическое переходное состояние, как и при гидролизе, однако без раскрытия кольца. [34]

Из этих экспериментов можно понять, что повышенная реакционная способность, наблюдаемая для гипервалентных молекул, по сравнению с аналогичными негипервалентными соединениями, может быть объяснена конгруэнтностью этих частиц гиперкоординированным активированным состояниям, обычно образующимся в ходе реакции.
Повышенная реакционная способность пентакоординированного кремния до конца не изучена. Корриу и его коллеги предположили, что больший электроположительный характер атома пятивалентного кремния может быть ответственен за его повышенную реакционную способность. [35] Предварительные расчеты ab initio в некоторой степени подтвердили эту гипотезу, но использовали небольшой базисный набор. [36]
Программное обеспечение для расчетов ab initio, Gaussian 86 , использовалось Дитерсом и его коллегами для сравнения тетракоординированных кремния и фосфора с их пентакоординатными аналогами. Этот подход ab initio используется в качестве дополнения для определения того, почему реакционная способность улучшается в нуклеофильных реакциях с пентакоординированными соединениями. Для кремния использовался базисный набор 6-31+G* из-за его пентакоординированного анионного характера, а для фосфора использовался базисный набор 6-31G* . [36]
Пентакоординированные соединения теоретически должны быть менее электрофильными, чем тетракоординированные аналоги, из-за стерических затруднений и большей электронной плотности лигандов, но экспериментально демонстрируют большую реакционную способность с нуклеофилами, чем их тетракоординированные аналоги. Расширенные расчеты ab initio были выполнены на ряде тетракоординированных и пентакоординированных видов, чтобы лучше понять это явление реакционной способности. Каждая серия различалась по степени фторирования. Длины связей и плотности заряда показаны как функции количества гидридных лигандов на центральных атомах. В каждом новом гидриде на один фторид меньше. [36]
С помощью этого подхода ab initio для длин связей кремния и фосфора, плотности заряда и перекрытия связей Малликена были рассчитаны популяции тетра- и пентакоординированных частиц. [36] Добавление фторид-иона к тетракоординированному кремнию приводит к общему среднему увеличению заряда электрона на 0,1, что считается незначительным. В целом длины связей в тригонально-бипирамидальных пятикоординатных видах больше, чем в тетракоординатных аналогах. Связи Si-F и связи Si-H увеличиваются в длине при пентакоординации, и соответствующие эффекты наблюдаются у видов фосфора, но в меньшей степени. Причиной большей величины изменения длины связи для видов кремния по сравнению с видами фосфора является увеличение эффективного ядерного заряда фосфора. Таким образом, сделан вывод, что кремний более слабо связан со своими лигандами.
Кроме того, Дитерс и его коллеги [36] показали обратную корреляцию между длиной связи и перекрытием связей для всех серий. Сделан вывод, что пентакоординированные виды более реакционноспособны из-за их более слабых связей в виде тригонально-бипирамидальных структур.
Путем расчета энергий присоединения и удаления фторид-иона в различных соединениях кремния и фосфора было обнаружено несколько тенденций. В частности, тетракоординированные виды имеют гораздо более высокие энергетические потребности для удаления лиганда, чем пентакоординированные виды. Кроме того, виды кремния требуют меньше энергии для удаления лиганда, чем виды фосфора, что является показателем более слабых связей в кремнии.
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ){{cite journal}}: Отсутствует или пусто |title=( помощь )