
Тилакоиды представляют собой мембраносвязанные отсеки внутри хлоропластов и цианобактерий . Они являются местом светозависимых реакций фотосинтеза . Тилакоиды состоят из тилакоидной мембраны, окружающей просвет тилакоида. Тилакоиды хлоропластов часто образуют стопки дисков, называемые гранами (единственное число: granum ). Граны соединены межгранальными или стромальными тилакоидами, которые объединяют стопки гранумов в единый функциональный отсек.
В мембранах тилакоидов пигменты хлорофилла находятся в пакетах, называемых квантазомами . Каждая квантасома содержит от 230 до 250 молекул хлорофилла.
Слово «тилакоид» происходит от греческого слова «thilakos » или θύλακος , что означает «мешочек» или «мешочек». [1] Таким образом, тилакоид означает «мешочек» или «мешочек».



Тилакоиды представляют собой мембраносвязанные структуры, встроенные в строму хлоропласта . Стопка тилакоидов называется гранумом и напоминает стопку монет.
Тилакоидная мембрана является местом светозависимых реакций фотосинтеза, при этом фотосинтетические пигменты встроены непосредственно в мембрану. Это чередующийся узор из темных и светлых полос размером 1 нанометр каждая . [3] Липидный бислой тилакоида имеет общие характеристики с мембранами прокариот и внутренней мембраной хлоропластов. Например, кислые липиды содержатся в мембранах тилакоидов, цианобактерий и других фотосинтезирующих бактерий и участвуют в функциональной целостности фотосистем. [4] Тилакоидные мембраны высших растений состоят в основном из фосфолипидов [5] и галактолипидов , которые асимметрично расположены вдоль и поперек мембран. [6] Мембраны тилакоидов богаче галактолипидами, а не фосфолипидами; также они преимущественно состоят из гексагональной фазы II, образующей моногалактозилдиглицеридный липид. Было показано, что, несмотря на этот уникальный состав, мембраны тилакоидов растений в основном принимают динамическую организацию липидного бислоя. [7] Липиды, образующие тилакоидные мембраны, наиболее богатые высокотекучей линоленовой кислотой [8] , синтезируются сложным путем, включающим обмен липидных предшественников между эндоплазматическим ретикулумом и внутренней мембраной пластидной оболочки и транспортируются от внутренней мембраны к тилакоидам. через пузырьки. [9]
Просвет тилакоида представляет собой сплошную водную фазу , окруженную тилакоидной мембраной . Он играет важную роль в фотофосфорилировании во время фотосинтеза . Во время светозависимой реакции протоны перекачиваются через тилакоидную мембрану в полость, делая ее кислой до pH 4.
У высших растений тилакоиды организованы в мембранный комплекс гранум-строма. Гранум ( множественное число грана ) представляет собой стопку тилакоидных дисков. Хлоропласты могут иметь от 10 до 100 гран. Граны соединены тилакоидами стромы, также называемыми межгранальными тилакоидами или пластинками . Тилакоиды грана и тилакоиды стромы можно отличить по разному белковому составу. Граны способствуют большому соотношению площади поверхности к объему хлоропластов. Недавнее исследование электронной томографии тилакоидных мембран показало, что ламели стромы организованы в широкие листы, перпендикулярные оси стопки гран, и образуют множественные правосторонние спиральные поверхности на границе раздела гран. [2] Левые винтовые поверхности консолидируются между правыми спиралями и листами. Было показано, что эта сложная сеть чередующихся спиральных мембранных поверхностей разного радиуса и шага минимизирует поверхностную энергию и энергию изгиба мембран. [2] Эта новая модель, самая обширная из созданных на сегодняшний день, показала, что в структуре сосуществуют особенности двух, казалось бы, противоречивых старых моделей [10] [11] . Примечательно, что подобное расположение спиральных элементов чередующейся направленности, часто называемых структурами «гаража», предположительно присутствует в эндоплазматическом ретикулуме [12] и в сверхплотной ядерной материи. [13] [14] [15] Эта структурная организация может представлять собой фундаментальную геометрию для соединения между плотно упакованными слоями или листами. [2]
Хлоропласты развиваются из пропластид , когда всходы выходят из земли. Для формирования тилакоидов необходим свет. В зародыше растения и в отсутствие света пропластиды развиваются в этиопласты , содержащие полукристаллические мембранные структуры, называемые проламеллярными тельцами. Под воздействием света эти проламеллярные тельца развиваются в тилакоиды. Этого не происходит у выращенных в темноте сеянцев, подвергающихся этиоляции . Недостаточное воздействие света может привести к отказу тилакоидов. Это приводит к выходу из строя хлоропластов, что приводит к гибели растения.
Для формирования тилакоидов необходимо действие индуцирующего пузырьки белка в пластидах 1 (VIPP1). Растения не могут выжить без этого белка, а снижение уровня VIPP1 приводит к замедлению роста и бледности растений с пониженной способностью к фотосинтезу. VIPP1, по-видимому, необходим для формирования основной тилакоидной мембраны, но не для сборки белковых комплексов тилакоидной мембраны. [16] Он консервативен во всех организмах, содержащих тилакоиды, включая цианобактерии, [17] зеленые водоросли, такие как Chlamydomonas , [18] и высшие растения, такие как Arabidopsis thaliana . [19]
Тилакоиды можно очистить из растительных клеток, используя комбинацию дифференциального и градиентного центрифугирования . [20] Разрушение изолированных тилакоидов, например, механическим сдвигом, приводит к высвобождению просветной фракции. Периферийные и интегральные мембранные фракции можно выделить из оставшейся мембранной фракции. Обработка карбонатом натрия (Na 2 CO 3 ) отщепляет периферические мембранные белки , тогда как обработка детергентами и органическими растворителями солюбилизирует интегральные мембранные белки .

Тилакоиды содержат множество интегральных и периферических мембранных белков, а также люменальных белков. Недавние протеомные исследования фракций тилакоидов предоставили дополнительную информацию о белковом составе тилакоидов. [21] Эти данные были обобщены в нескольких базах данных пластидных белков, доступных в Интернете. [22] [23]
Согласно этим исследованиям, протеом тилакоида состоит как минимум из 335 различных белков. Из них 89 находятся в просвете, 116 являются интегральными мембранными белками, 62 являются периферическими белками на стороне стромы и 68 периферическими белками на стороне просвета. Дополнительные белки с низким содержанием просвета можно предсказать с помощью вычислительных методов. [20] [24] Из тилакоидных белков с известными функциями 42% участвуют в фотосинтезе. Следующие по величине функциональные группы включают белки, участвующие в нацеливании , процессинге и сворачивании белков ( 11%), реакции на окислительный стресс (9%) и трансляции (8%). [22]
Мембраны тилакоидов содержат интегральные мембранные белки , которые играют важную роль в светособирании и светозависимых реакциях фотосинтеза. В мембране тилакоида имеются четыре основных белковых комплекса:
Фотосистема II расположена преимущественно в тилакоидах гран, тогда как фотосистема I и АТФ-синтаза преимущественно расположены в тилакоидах стромы и наружных слоях гран. Комплекс цитохрома b6f равномерно распределен по мембранам тилакоидов. Из-за раздельного расположения двух фотосистем в мембранной системе тилакоидов мобильные переносчики электронов необходимы для перемещения электронов между ними. Этими носителями являются пластохинон и пластоцианин. Пластохинон переносит электроны от фотосистемы II к комплексу цитохрома b6f, тогда как пластоцианин переносит электроны от комплекса цитохрома b6f к фотосистеме I.
Вместе эти белки используют энергию света для управления цепями переноса электронов , которые генерируют хемиосмотический потенциал через тилакоидную мембрану и НАДФН , продукт терминальной окислительно-восстановительной реакции. АТФ -синтаза использует хемиосмотический потенциал для образования АТФ во время фотофосфорилирования .
Эти фотосистемы представляют собой управляемые светом окислительно-восстановительные центры, каждый из которых состоит из антенного комплекса , который использует хлорофиллы и дополнительные фотосинтетические пигменты , такие как каротиноиды и фикобилипротеины, для сбора света с различными длинами волн. Каждый антенный комплекс содержит от 250 до 400 молекул пигмента, и поглощаемая ими энергия передается посредством резонансной передачи энергии специализированному хлорофиллу а в реакционном центре каждой фотосистемы. Когда любая из двух молекул хлорофилла а в реакционном центре поглощает энергию, электрон возбуждается и передается молекуле-акцептору электронов. Фотосистема I содержит в своем реакционном центре пару молекул хлорофилла А , обозначенную P700 , которые максимально поглощают свет с длиной волны 700 нм. Фотосистема II содержит хлорофилл P680 , который лучше всего поглощает свет с длиной волны 680 нм (обратите внимание, что эти длины волн соответствуют темно-красному цвету — см. видимый спектр ). P — это сокращение от пигмента, а число — это удельный пик поглощения в нанометрах для молекул хлорофилла в каждом реакционном центре. Это зеленый пигмент, присутствующий в растениях, который не виден невооруженным глазом.
Комплекс цитохрома b6f является частью цепи переноса электронов тилакоида и связывает перенос электронов с перекачкой протонов в просвет тилакоида. Энергетически он расположен между двумя фотосистемами и переносит электроны от фотосистемы II-пластохинон к пластоцианин-фотосистеме I.
Тилакоидная АТФ-синтаза представляет собой CF1FO-АТФ-синтазу, аналогичную митохондриальной АТФазе. Он интегрирован в тилакоидную мембрану, а часть CF1 прикрепляется к строме. Таким образом, синтез АТФ происходит на стромальной стороне тилакоидов, где АТФ необходим для светонезависимых реакций фотосинтеза.
Белок-переносчик электронов пластоцианин присутствует в просвете и переносит электроны от белкового комплекса цитохрома b6f к фотосистеме I. Хотя пластохиноны являются жирорастворимыми и, следовательно, перемещаются внутри тилакоидной мембраны, пластоцианин перемещается через просвет тилакоида.
Просвет тилакоидов также является местом окисления воды комплексом, выделяющим кислород , связанным с люменальной стороной фотосистемы II.
Люменальные белки можно предсказать вычислительно на основе их нацеливающих сигналов. У арабидопсиса из предсказанных люменальных белков, обладающих сигналом Tat , самые большие группы с известными функциями 19% участвуют в процессинге белка (протеолиз и сворачивание), 18% в фотосинтезе, 11% в метаболизме и 7% являются окислительно-восстановительными переносчиками и защитой. . [20]
Хлоропласты имеют собственный геном , который кодирует ряд тилакоидных белков. Однако в ходе эволюции пластид от их цианобактериальных эндосимбиотических предков произошел обширный перенос генов из генома хлоропластов в ядро клетки . Это приводит к тому, что четыре основных белковых комплекса тилакоидов кодируются частично геномом хлоропластов, а частично ядерным геномом. Растения разработали несколько механизмов совместной регуляции экспрессии различных субъединиц, закодированных в двух разных органеллах, чтобы обеспечить правильную стехиометрию и сборку этих белковых комплексов. Например, транскрипция ядерных генов, кодирующих части фотосинтетического аппарата, регулируется светом . Биогенез, стабильность и оборот тилакоидных белковых комплексов регулируются фосфорилированием с помощью редокс-чувствительных киназ в тилакоидных мембранах. [25] Скорость трансляции белков, кодируемых хлоропластами, контролируется наличием или отсутствием партнеров по сборке (контроль эпистазией синтеза). [26] Этот механизм включает отрицательную обратную связь посредством связывания избыточного белка с 5'-нетранслируемой областью мРНК хлоропласта . [27] Хлоропластам также необходимо сбалансировать соотношение фотосистем I и II для цепи переноса электронов. Редокс-состояние переносчика электронов пластохинона в тилакоидной мембране напрямую влияет на транскрипцию генов хлоропластов, кодирующих белки реакционных центров фотосистем, противодействуя тем самым дисбалансам в цепи переноса электронов. [28]
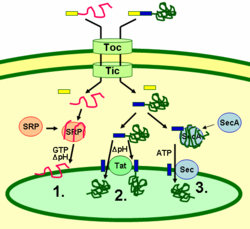
Тилакоидные белки доставляются к месту назначения с помощью сигнальных пептидов и секреторных путей прокариотического типа внутри хлоропласта. Большинству тилакоидных белков, кодируемых ядерным геномом растения, для правильной локализации необходимы два нацеливающих сигнала: N-концевой пептид, нацеливающий хлоропласты (показан желтым цветом на рисунке), за которым следует пептид, нацеливающий тилакоиды (показан синим цветом). Белки импортируются через транслокон комплексов внешней и внутренней мембраны ( Toc и Tic ). После попадания в хлоропласт первый целевой пептид отщепляется протеазой, обрабатывающей импортированные белки. Это демаскирует второй сигнал нацеливания, и белок экспортируется из стромы в тилакоид на втором этапе нацеливания. Этот второй этап требует действия белковых транслокационных компонентов тилакоидов и является энергозависимым. Белки встраиваются в мембрану по SRP-зависимому пути (1), Tat-зависимому пути (2) или спонтанно через свои трансмембранные домены (на рисунке не показаны). Люменальные белки экспортируются через тилакоидную мембрану в просвет либо по Tat-зависимому пути (2), либо по Sec-зависимому пути (3) и высвобождаются путем расщепления сигнала, направляющего тилакоиды. Различные пути используют разные сигналы и источники энергии. Путь Sec (секреторный) требует АТФ в качестве источника энергии и состоит из SecA, который связывается с импортированным белком, и мембранного комплекса Sec, обеспечивающего транспортировку белка. Белки с двойным аргининовым мотивом в сигнальном пептиде тилакоида перемещаются по пути Tat (двойная транслокация аргинина), который требует мембраносвязанного комплекса Tat и градиента pH в качестве источника энергии. Некоторые другие белки встраиваются в мембрану по пути SRP ( частица распознавания сигнала ). SRP хлоропласта может взаимодействовать со своими белками-мишенями либо посттрансляционно, либо котрансляционно, транспортируя таким образом импортированные белки, а также те, которые транслируются внутри хлоропласта. Путь SRP требует GTP и градиента pH в качестве источников энергии. Некоторые трансмембранные белки могут также спонтанно встраиваться в мембрану со стороны стромы без затрат энергии. [29]

Тилакоиды являются местом светозависимых реакций фотосинтеза. К ним относятся управляемое светом окисление воды и выделение кислорода , перекачка протонов через тилакоидные мембраны в сочетании с цепью переноса электронов фотосистем и цитохромного комплекса, а также синтез АТФ с помощью АТФ-синтазы с использованием генерируемого протонного градиента.
Первым шагом фотосинтеза является восстановление (расщепление) воды под действием света с целью получения электронов для фотосинтетических цепей переноса электронов, а также протонов для создания протонного градиента. Реакция расщепления воды происходит на просветной стороне тилакоидной мембраны и приводится в действие световой энергией, улавливаемой фотосистемами. В результате окисления воды образуются отходы O 2 , жизненно важные для клеточного дыхания . Молекулярный кислород, образующийся в результате реакции, выбрасывается в атмосферу.
Во время фотосинтеза используются два различных варианта транспорта электронов:
Нециклическая разновидность предполагает участие обеих фотосистем, тогда как циклический поток электронов зависит только от фотосистемы I.
Основной функцией тилакоидной мембраны и ее целостных фотосистем является создание хемиосмотического потенциала. Переносчики в цепи переноса электронов используют часть энергии электронов для активной транспортировки протонов из стромы в просвет . Во время фотосинтеза просвет становится кислым , уровень pH достигает 4 по сравнению с pH 8 в строме. [30] Это представляет собой 10000-кратный градиент концентрации протонов через тилакоидную мембрану.
Протоны в просвете происходят из трех основных источников.
Протонный градиент также вызван потреблением протонов в строме для образования НАДФН из НАДФ+ на НАДФ-редуктазе.
Молекулярный механизм образования АТФ (аденозинтрифосфата) в хлоропластах аналогичен таковому в митохондриях и забирает необходимую энергию за счет движущей силы протонов (ПМФ). [ нужна цитата ] Однако хлоропласты больше полагаются на химический потенциал PMF для генерации потенциальной энергии, необходимой для синтеза АТФ. PMF представляет собой сумму химического потенциала протона (задаваемого градиентом концентрации протонов) и трансмембранного электрического потенциала (задаваемого разделением зарядов на мембране). По сравнению с внутренними мембранами митохондрий, которые имеют значительно более высокий мембранный потенциал из-за разделения зарядов, тилакоидные мембраны лишены градиента заряда. [ нужна цитата ] Чтобы компенсировать это, 10 000-кратный градиент концентрации протонов на мембране тилакоида намного выше по сравнению с 10-кратным градиентом на внутренней мембране митохондрий. Результирующий хемиосмотический потенциал между просветом и стромой достаточно высок, чтобы стимулировать синтез АТФ с использованием АТФ-синтазы . Когда протоны движутся обратно по градиенту через каналы АТФ-синтазы , АДФ + P i объединяются в АТФ. Таким образом, светозависимые реакции связаны с синтезом АТФ через протонный градиент. [ нужна цитата ]
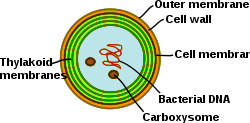
Цианобактерии — фотосинтезирующие прокариоты с высокодифференцированной мембранной системой. Цианобактерии имеют внутреннюю систему тилакоидных мембран, в которой находятся полнофункциональные цепи переноса электронов фотосинтеза и дыхания . Наличие различных мембранных систем придает этим клеткам уникальную сложность среди бактерий . Цианобактерии должны быть способны реорганизовать мембраны, синтезировать новые мембранные липиды и правильно направлять белки в правильную мембранную систему. Наружная мембрана , плазматическая мембрана и тилакоидные мембраны выполняют специализированные функции в цианобактериальной клетке. Понимание организации, функциональности, белкового состава и динамики мембранных систем остается серьезной проблемой в биологии цианобактерий. [31]
В отличие от сети тилакоидов высших растений, которая дифференцирована на пластинки граны и стромы, тилакоиды у цианобактерий организованы в несколько концентрических оболочек, которые расщепляются и сливаются в параллельные слои, образуя высокосвязанную сеть. В результате образуется непрерывная сеть, которая окружает один просвет (как в хлоропластах высших растений) и позволяет водорастворимым и жирорастворимым молекулам диффундировать через всю мембранную сеть. Кроме того, внутри параллельных листов тилакоидов часто наблюдаются перфорации. Эти промежутки в мембране обеспечивают перемещение частиц разного размера по клетке, включая рибосомы, гранулы гликогена и липидные тельца. [32] Относительно большое расстояние между тилакоидами обеспечивает пространство для внешних светособирающих антенн, фикобилисом . [33] Эта макроструктура, как и у высших растений, проявляет некоторую гибкость при изменении физико-химической среды. [34]