Сериновые протеазы (или сериновые эндопептидазы ) — ферменты , расщепляющие пептидные связи в белках . Серин служит нуклеофильной аминокислотой в активном центре (фермента) . [1] Они встречаются повсеместно как у эукариот , так и у прокариот . Сериновые протеазы делятся на две широкие категории в зависимости от их структуры: химотрипсиноподобные (трипсиноподобные) и субтилизинподобные . [2]
Система классификации протеаз MEROPS насчитывает 16 суперсемейств (по состоянию на 2013 год), каждое из которых содержит множество семейств . Каждое суперсемейство использует каталитическую триаду или диаду в различных белковых складках и, таким образом, представляет собой конвергентную эволюцию каталитического механизма . Большинство из них принадлежит к семейству S1 клана (суперсемейства) протеаз PA .
Для суперсемейств P: суперсемейство, содержащее смесь семейств классов нуклеофилов , S: чисто сериновые протеазы. суперсемья. Внутри каждого суперсемейства семейства обозначаются каталитическими нуклеофилами (S: сериновые протеазы).

Сериновые протеазы характеризуются своеобразной структурой, состоящей из двух доменов бета-бочонка, сходящихся в каталитическом активном центре. Эти ферменты можно далее классифицировать в зависимости от их субстратной специфичности: трипсиноподобные, химотрипсиноподобные или эластазоподобные. [5]
Трипсиноподобные протеазы расщепляют пептидные связи после положительно заряженной аминокислоты ( лизина или аргинина ). [6] Эта специфичность обусловлена остатком, который лежит в основании кармана S1 фермента (обычно отрицательно заряженная аспарагиновая кислота или глутаминовая кислота ).
Карман S1 химотрипсиноподобных ферментов более гидрофобен, чем у трипсиноподобных протеаз. Это приводит к специфичности к гидрофобным остаткам среднего и большого размера, таким как тирозин , фенилаланин и триптофан .
К ним относятся тромбин , тканеактивирующий плазминоген и плазмин . Было обнаружено, что они играют роль в коагуляции и пищеварении, а также в патофизиологии нейродегенеративных заболеваний, таких как деменция, вызванная болезнью Альцгеймера и Паркинсона. В ядах змей обнаружено множество высокотоксичных изоформ тромбиноподобных сериновых протеаз. [7]
Эластазоподобные протеазы имеют гораздо меньшую щель S1, чем трипсин- или химотрипсин-подобные протеазы. Следовательно, такие остатки, как аланин , глицин и валин, имеют тенденцию быть предпочтительными.
Субтилизин — сериновая протеаза прокариот . Субтилизин эволюционно не связан с кланом химотрипсина, но имеет тот же каталитический механизм, использующий каталитическую триаду для создания нуклеофильного серина . Это классический пример, используемый для иллюстрации конвергентной эволюции , поскольку один и тот же механизм развивался дважды независимо в ходе эволюции .
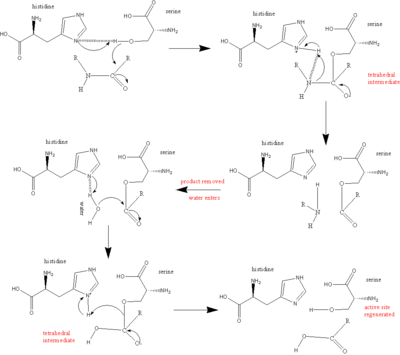
Основным участником каталитического механизма сериновых протеаз является каталитическая триада. Триада расположена в активном центре фермента, где происходит катализ, и сохраняется во всех суперсемействах ферментов сериновых протеаз. Триада представляет собой скоординированную структуру, состоящую из трех аминокислот : His 57, Ser 195 (отсюда и название «сериновая протеаза») и Asp 102. Каждая из этих трех ключевых аминокислот играет важную роль в расщепляющей способности протеаз. Хотя аминокислотные члены триады расположены далеко друг от друга в последовательности белка, из-за сворачивания они будут очень близки друг к другу в сердце фермента. Особая геометрия членов триады весьма характерна для их конкретной функции: было показано, что положение всего четырех точек триады характеризует функцию содержащего их фермента. [8]
В случае катализа возникает упорядоченный механизм, при котором образуется несколько промежуточных продуктов. Катализ расщепления пептида можно рассматривать как катализ «пинг-понг» , при котором связывается субстрат (в данном случае расщепляемый полипептид), высвобождается продукт (С-концевая «половина» пептида с аминогруппой видимый), связывается другой субстрат (в данном случае вода) и высвобождается другой продукт (видима N-концевая «половина» пептида с карбоксильной группой).
Каждая аминокислота в триаде выполняет в этом процессе определенную задачу:
Всю реакцию можно резюмировать следующим образом:
Было обнаружено, что дополнительные аминокислоты протеазы, Gly 193 и Ser 195 , участвуют в создании так называемой оксианионной дырки . И Gly 193 , и Ser 195 могут отдавать водороды основной цепи для образования водородных связей. Когда образуется тетраэдрический интермедиат на шаге 1 и шаге 3, отрицательный ион кислорода, приняв электроны от двойной карбонильной связи, идеально вписывается в оксианионную дырку. Фактически, сериновые протеазы преимущественно связывают переходное состояние , и общая структура благоприятствует, снижая энергию активации реакции. Это «предпочтительное связывание» отвечает за большую часть каталитической эффективности фермента.
Организмы-хозяева должны обеспечить адекватную регуляцию активности сериновых протеаз. Это достигается за счет необходимости начальной активации протеазы и секреции ингибиторов.
Зимогены обычно являются неактивными предшественниками фермента. Если бы пищеварительные ферменты были активны при синтезе, они немедленно начали бы пережевывать синтезирующие органы и ткани. Острый панкреатит – это состояние, при котором происходит преждевременная активация пищеварительных ферментов поджелудочной железы, что приводит к самоперевариванию (аутолизу). Это также усложняет посмертные исследования , поскольку поджелудочная железа часто переваривает себя прежде, чем ее можно будет оценить визуально.
Зимогены представляют собой крупные неактивные структуры, способные распадаться на части или превращаться в более мелкие активированные ферменты. Отличие зимогенов от активированных ферментов заключается в том, что активный центр катализа зимогенов искажен. В результате полипептид-субстрат не может эффективно связываться, и протеолиз не происходит. Только после активации, в ходе которой изменяются конформация и структура зимогена и открывается активный центр, может произойти протеолиз .
Как видно, активация трипсиногена на трипсин имеет важное значение, поскольку он активирует собственную реакцию, а также реакцию как химотрипсина , так и эластазы . Поэтому очень важно, чтобы эта активация не происходила преждевременно. Организм предпринимает несколько защитных мер для предотвращения самопереваривания:
Существуют определенные ингибиторы , которые напоминают тетраэдрический промежуточный продукт и, таким образом, заполняют активный центр, препятствуя правильной работе фермента. Трипсин, мощный пищеварительный фермент, вырабатывается в поджелудочной железе. Ингибиторы предотвращают самопереваривание самой поджелудочной железы.
Сериновые протеазы сочетаются с ингибиторами сериновых протеаз , которые отключают свою активность, когда они больше не нужны. [9] [ самостоятельный источник? ]
Сериновые протеазы ингибируются разнообразной группой ингибиторов , включая синтетические химические ингибиторы для исследовательских или терапевтических целей, а также природные белковые ингибиторы. Одно семейство природных ингибиторов, называемое «серпины» (сокращенно от « ингибиторы сериновой протеазы» ), может образовывать ковалентную связь с сериновой протеазой, ингибируя ее функцию. Наиболее изученными серпинами являются антитромбин и альфа-1-антитрипсин , изученные на предмет их роли в процессах коагуляции / тромбоза и эмфиземы / А1АТ соответственно. Искусственные необратимые низкомолекулярные ингибиторы включают AEBSF и PMSF .
Семейство ингибиторов сериновой пептидазы членистоногих , называемое пацифастин , было обнаружено у саранчи и раков и может действовать в иммунной системе членистоногих . [10]
Мутации могут приводить к снижению или повышению активности ферментов. Это может иметь разные последствия в зависимости от нормальной функции сериновой протеазы. Например, мутации белка С могут привести к дефициту белка С и предрасполагать к тромбозу . Кроме того, некоторые протеазы играют жизненно важную роль в активации слияния клетки-хозяина и вируса, запуская белок Spike вируса, чтобы показать белок, называемый «слитый белок» ( TMPRSS2 активирует слияние SARS-CoV-2 ). Экзогенные сериновые протеазы змеиного яда вызывают широкий спектр коагулопатий при введении хозяину из-за отсутствия регуляции их активности. [7]
Определение уровней сериновой протеазы может быть полезно в контексте конкретных заболеваний.
Благодаря своей каталитической активности некоторые сериновые протеазы обладают мощными противомикробными свойствами. Несколько исследований in vitro продемонстрировали эффективность некоторых протеаз в снижении вирулентности путем расщепления поверхностных белков вируса. Проникновение вируса в клетки-хозяева опосредовано взаимодействием этих поверхностных белков с клеткой-хозяином. Когда эти белки фрагментируются или инактивируются на поверхности вируса, проникновение вируса нарушается, что приводит к снижению инфекционности широкого спектра патологически значимых микроорганизмов, таких как грипп , hRSV и другие. [11] [12]