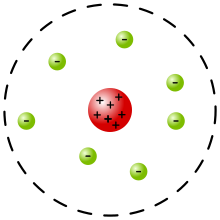
Модель Резерфорда была разработана Эрнестом Резерфордом для описания атома . Резерфорд руководил экспериментом Гейгера-Марсдена в 1909 году, который, на основе анализа Резерфорда 1911 года, показал, что модель атома сливового пудинга Дж. Дж. Томсона неверна . Новая модель атома Резерфорда [1] , основанная на экспериментальных результатах, содержала новые особенности относительно высокого центрального заряда, сконцентрированного в очень малом объеме по сравнению с остальной частью атома, причем этот центральный объем содержит большую часть массы атома . ; эта область будет известна как атомное ядро . Модель Резерфорда впоследствии была заменена моделью Бора .
В той же статье, в которой Дж. Дж. Томсон объявил о своих результатах о «корпускульной» природе катодных лучей , событии, которое считается открытием электрона , он начал размышлять об атомных моделях, состоящих из электронов. Он разработал свою модель, теперь называемую моделью сливового пудинга , в основном в 1904-06 годах. Он создал сложную механическую модель электронов, движущихся по концентрическим кольцам, но положительный заряд, необходимый для уравновешивания отрицательных электронов, представлял собой простую сферу с однородным зарядом и неизвестным составом. [2] : 13
Резерфорд опроверг модель Томсона в 1911 году своим известным экспериментом с золотой фольгой, в котором он продемонстрировал, что атом имеет крошечное и тяжелое ядро. Резерфорд разработал эксперимент по использованию альфа-частиц , испускаемых радиоактивным элементом, в качестве зондов невидимого мира атомной структуры. Если бы Томсон был прав, луч прошел бы прямо через золотую фольгу. Большая часть лучей прошла сквозь фольгу, но некоторые отклонились.
Резерфорд представил свою собственную физическую модель субатомной структуры как интерпретацию неожиданных экспериментальных результатов. В нем атом состоит из центрального заряда (это современное атомное ядро , хотя Резерфорд не использовал в своей работе термин «ядро»), окруженного облаком (предположительно) вращающихся по орбитам электронов . В этой статье, опубликованной в мае 1911 года, Резерфорд выделил лишь небольшую центральную область с очень высоким положительным или отрицательным зарядом в атоме.
Для конкретики рассмотрим прохождение высокоскоростной α-частицы через атом, имеющий положительный центральный заряд N e и окруженный компенсирующим зарядом из N электронов. [3]
Из чисто энергетических соображений о том, как далеко частицы с известной скоростью смогут проникнуть к центральному заряду в 100 е, Резерфорд смог вычислить, что радиус его золотого центрального заряда должен быть меньше (насколько меньше нельзя было сказать). ), чем 3,4 × 10 −14 метров. Это произошло в атоме золота, радиус которого, как известно, составлял 10–10 метров или около того — очень удивительное открытие, поскольку оно подразумевало сильный центральный заряд, составляющий менее 1/3000 диаметра атома.
Модель Резерфорда позволяла сконцентрировать большую часть заряда и массы атома в очень маленьком ядре, но не приписывала никакой структуры оставшимся электронам и оставшейся атомной массе. Там упоминалась атомная модель Хантаро Нагаока , в которой электроны расположены в одно или несколько колец, со специфической метафорической структурой стабильных колец Сатурна. Модель сливового пудинга Дж. Дж. Томсона также имела кольца вращающихся по орбитам электронов. Жан Батист Перрен в своей Нобелевской лекции [4] заявил , что он был первым, кто предложил эту модель в своей статье, датированной 1901 годом. Но на самом деле североирландский физик Джозеф Лармор создал первую модель атома Солнечной системы в 1897 году. [5]
В статье Резерфорда предполагалось, что центральный заряд атома может быть «пропорционален» его атомной массе в единицах массы водорода u (примерно 1/2 от нее в модели Резерфорда). Для золота это массовое число равно 197 (в то время оно не было известно с большой точностью), и поэтому Резерфорд смоделировал его как, возможно, 196 u. Однако Резерфорд не пытался установить прямую связь центрального заряда с атомным номером , поскольку «атомный номер» золота (в то время просто номер его позиции в периодической таблице ) был 79, и Резерфорд смоделировал заряд примерно равным + 100 единиц (на самом деле он предлагал 98 единиц положительного заряда, что составляет половину от 196). Таким образом, Резерфорд формально не предполагал, что эти два числа (место в таблице Менделеева, 79, и заряд ядра, 98 или 100) могут быть совершенно одинаковыми.
Через месяц после появления статьи Резерфорда предложение о точной идентичности атомного номера и заряда ядра было сделано Антониусом ван ден Бруком , а позже подтверждено экспериментально в течение двух лет Генри Мозли .
Это ключевые показатели:
После открытия Резерфорда последующие исследования определили атомную структуру, что привело к эксперименту Резерфорда с золотой фольгой . В конце концов ученые обнаружили, что атомы имеют положительно заряженное ядро (с атомным числом зарядов) в центре радиусом около 1,2 × 10 −15 метров × [атомное массовое число] 1 ⁄ 3 . Электроны оказались еще меньше.
Позже ученые с помощью рентгеновских лучей нашли ожидаемое количество электронов (такое же, как и атомный номер) в атоме . Когда рентгеновские лучи проходят через атом, часть их рассеивается , а остальная часть проходит сквозь атом. Поскольку рентгеновские лучи теряют свою интенсивность в первую очередь за счет рассеяния на электронах, отметив скорость уменьшения интенсивности рентгеновских лучей, можно точно оценить число электронов, содержащихся в атоме.

По мнению Нагаока, модель Резерфорда основывалась на идее множества электронов в кольцах. Однако как только Нильс Бор изменил эту точку зрения на картину всего лишь нескольких планетоподобных электронов для легких атомов, модель Резерфорда-Бора захватила воображение публики. С тех пор его постоянно использовали как символ атомов и даже «атомной» энергии (хотя правильнее было бы считать ее ядерной энергией). Примеры его использования за последнее столетие включают, помимо прочего: