
В химии резонанс , также называемый мезомерией , представляет собой способ описания связей в определенных молекулах или многоатомных ионах путем объединения нескольких способствующих структур (или форм , [1] также известных как резонансные структуры или канонические структуры ) в резонансный гибрид ( или гибридная структура ) в теории валентной связи . Это имеет особое значение для анализа делокализованных электронов , связь которых не может быть выражена одной-единственной структурой Льюиса . Резонансный гибрид — это точная структура молекулы или иона; это среднее значение теоретически способствующих структур.
В рамках теории валентных связей резонанс является расширением идеи о том, что связь в химических соединениях может быть описана структурой Льюиса. Для многих химических соединений одна структура Льюиса, состоящая из атомов, подчиняющихся правилу октетов , возможно, несущих формальные заряды и соединенных связями положительного целого порядка, достаточна для описания химической связи и рационализации экспериментально определенных молекулярных свойств, таких как длины связей , углы , и дипольный момент . [2] Однако в некоторых случаях можно нарисовать более одной структуры Льюиса, и экспериментальные свойства несовместимы ни с одной структурой. Чтобы справиться с ситуацией такого типа, несколько вносящих вклад структур рассматриваются вместе как среднее, и говорят, что молекула представляет собой резонансный гибрид, в котором несколько структур Льюиса используются вместе для описания ее истинной структуры.

Например, в нитрит-анионе NO 2 – длины двух связей NO равны, хотя ни одна структура Льюиса не имеет двух связей NO с одинаковым формальным порядком связей . Однако его измеренная структура согласуется с описанием как резонансного гибрида двух основных структур, показанных выше: он имеет две равные связи N–O длиной 125 мкм, промежуточные по длине между типичной одинарной связью N–O (145 мкм в гидроксиламин , H 2 N–OH) и двойную связь N–O (115 пм в ионе нитрония , [O=N=O] + ). В соответствии с участвующими структурами каждая связь NO – O представляет собой среднее значение формальной одинарной и формально двойной связи, что приводит к истинному порядку связи 1,5. Благодаря такому усреднению льюисовское описание связи в NO 2 – согласуется с экспериментальным фактом, что анион имеет эквивалентные связи N–O.
Резонансный гибрид представляет реальную молекулу как «среднее» из вносящих вклад структур, при этом длины связей и частичные заряды принимают промежуточные значения по сравнению с ожидаемыми для отдельных структур Льюиса вносящих вклады, если бы они существовали как «реальные» химические образования. . [3] Содействующие структуры различаются только формальным распределением электронов между атомами, а не фактической физически и химически значимой электронной или спиновой плотностью. Хотя вносящие вклад структуры могут различаться формальным порядком связей и формальным распределением заряда, все вносящие вклад структуры должны иметь одинаковое количество валентных электронов и одинаковую спиновую кратность . [4]
Поскольку делокализация электронов снижает потенциальную энергию системы, любая разновидность, представленная резонансным гибридом, более стабильна, чем любая из (гипотетических) вносящих вклад структур. [5] Делокализация электронов стабилизирует молекулу, поскольку электроны более равномерно распределяются по молекуле, уменьшая электрон-электронное отталкивание. [6] Разница в потенциальной энергии между реальными частицами и (вычисленной) энергией вносящей вклад структуры с наименьшей потенциальной энергией называется энергией резонанса [7] или энергией делокализации. Величина резонансной энергии зависит от предположений, сделанных о гипотетических «нестабилизированных» частицах и используемых вычислительных методах, и не представляет собой измеримую физическую величину, хотя сравнение резонансных энергий, рассчитанных при аналогичных предположениях и условиях, может иметь химический смысл.
Молекулы с расширенной π-системой, такие как линейные полиены и полиароматические соединения, хорошо описываются резонансными гибридами, а также делокализованными орбиталями в теории молекулярных орбиталей .
Резонанс следует отличать от изомерии . Изомеры — это молекулы с одинаковой химической формулой, но представляющие собой отдельные химические виды с разным расположением атомных ядер в пространстве. С другой стороны, вкладчики резонанса молекулы могут различаться только тем, как электроны формально приписываются атомам в изображениях структуры Льюиса молекулы. В частности, когда говорят, что молекулярная структура представлена резонансным гибридом, это не означает , что электроны молекулы «резонируют» или перемещаются вперед и назад между несколькими наборами положений, каждое из которых представлено структурой Льюиса. Скорее, это означает, что набор вносящих вклад структур представляет собой промежуточную структуру (средневзвешенное значение вкладчиков) с единой, четко определенной геометрией и распределением электронов. Неверно рассматривать резонансные гибриды как быстро взаимопревращающиеся изомеры, хотя термин «резонанс» может вызвать такой образ. [8] (Как описано ниже, термин «резонанс» возник как аналогия квантово-механического явления в классической физике, поэтому его не следует понимать слишком буквально.) Символически двунаправленная стрелка используется для обозначения того, что A и B представляют собой способствующие формы одного химического вида (в отличие от стрелки равновесия, например ; подробности использования см. ниже).
Показательна нехимическая аналогия: характеристики реального животного, нарвала , можно описать с точки зрения характеристик двух мифических существ: единорога , существа с единственным рогом на голове, и левиафана , большого , китообразное существо. Нарвал — это не существо, которое мечется между единорогом и левиафаном, а единорог и левиафан не имеют никакого физического существования за пределами коллективного человеческого воображения. Тем не менее, описание нарвала с точки зрения этих воображаемых существ дает достаточно хорошее описание его физических характеристик.
Из-за путаницы с физическим значением слова « резонанс », поскольку никакие сущности на самом деле физически не «резонируют», было предложено отказаться от термина «резонанс» в пользу делокализации [9] и отказаться от энергии резонанса в пользу энергии делокализации . Резонансная структура становится содействующей структурой , а резонансный гибрид становится гибридной структурой . Двуглавые стрелки будут заменены запятыми, чтобы проиллюстрировать набор структур, поскольку стрелки любого типа могут указывать начинающим студентам на то, что происходит химическое изменение.
На диаграммах участвующие структуры обычно разделяются двунаправленными стрелками (↔). Стрелку не следует путать со стрелками равновесия вправо и влево (⇌). Все структуры вместе могут быть заключены в большие квадратные скобки, чтобы указать, что они изображают одну молекулу или ион, а не разные виды, находящиеся в химическом равновесии .
В качестве альтернативы использованию дополнительных структур на диаграммах можно использовать гибридную структуру. В гибридной структуре пи-связи , участвующие в резонансе, обычно изображаются в виде кривых [10] или пунктирных линий, что указывает на то, что это частичные, а не нормальные полные пи-связи. В бензоле и других ароматических кольцах делокализованные пи-электроны иногда изображаются в виде сплошного круга. [11]
Эта концепция впервые появилась в 1899 году в «Гипотезе частичной валентности» Иоганна Тиле, чтобы объяснить необычную стабильность бензола, которую нельзя было ожидать от структуры Августа Кекуле, предложенной в 1865 году с чередующимися одинарными и двойными связями. [12] Бензол подвергается реакциям замещения, а не реакциям присоединения, типичным для алкенов . Он предположил, что углерод-углеродная связь в бензоле является промежуточной между одинарной и двойной связью.
Предложение о резонансе также помогло объяснить количество изомеров производных бензола. Например, структура Кекуле позволяет предсказать четыре изомера дибромбензола, включая два орто- изомера с бромированными атомами углерода, соединенными одинарной или двойной связью. В действительности существует только три изомера дибромбензола, и только один является орто-изомером, что согласуется с идеей о том, что существует только один тип связи углерод-углерод, промежуточный между одинарной и двойной связью. [13]
Механизм резонанса был введен в квантовую механику Вернером Гейзенбергом в 1926 году при обсуждении квантовых состояний атома гелия. Он сравнил строение атома гелия с классической системой резонирующих связанных гармонических осцилляторов . [3] [14] В классической системе связь создает две моды, одна из которых имеет более низкую частоту , чем любая из несвязанных колебаний; квантово-механически эта более низкая частота интерпретируется как более низкая энергия. Лайнус Полинг использовал этот механизм для объяснения частичной валентности молекул в 1928 году и развил его дальше в серии статей в 1931–1933 годах. [15] [16] Альтернативный термин «мезомерия» [17] , популярный в немецких и французских публикациях с тем же значением, был введен К. К. Ингольдом в 1938 году, но не прижился в английской литературе. Современная концепция мезомерного эффекта приобрела схожий, но другой смысл. Двуглавая стрела была введена немецким химиком Фрицем Арндтом , который предпочитал немецкую фразу zwischenstufe или промежуточную стадию .
Теория резонанса доминировала над конкурирующим методом Хюккеля в течение двух десятилетий благодаря тому, что ее относительно легче понять химикам без фундаментальной физики, даже если они не могли уловить концепцию квантовой суперпозиции и путали ее с таутомерией . Сами Полинг и Уиланд в то время охарактеризовали подход Эриха Хюкеля как «громоздкий», и этому способствовало отсутствие у него коммуникативных навыков: когда Роберт Робинсон отправил ему дружеский запрос, он высокомерно ответил, что органическая химия его не интересует. [18]
В Советском Союзе теория резонанса – особенно разработанная Полингом – подверглась критике в начале 1950-х годов как противоречащая марксистским принципам диалектического материализма , а в июне 1951 года Советская Академия наук под руководством Александра Несмеянова созвала конференцию по химическое строение органических соединений, в котором приняли участие 400 физиков, химиков и философов, где « была раскрыта и разоблачена псевдонаучная сущность теории резонанса». [19]
Одна участвующая структура может больше напоминать реальную молекулу, чем другая (в смысле энергии и стабильности). Структуры с низким значением потенциальной энергии более стабильны, чем структуры с высокими значениями, и больше напоминают реальную структуру. Наиболее стабильные структуры, вносящие вклад, называются основными вкладчиками . Энергетически неблагоприятные и, следовательно, менее выгодные структуры вносят незначительный вклад . Поскольку правила перечислены в примерном порядке по мере убывания важности, основными участниками, как правило, являются структуры, которые
Максимум восемь валентных электронов является строгим для элементов Периода 2 Be, B, C, N, O и F, как и максимум два для H и He, а также эффективно для Li. [20] Вопрос о расширении валентной оболочки третьего периода и более тяжелых элементов основной группы является спорным. Структура Льюиса, в которой центральный атом имеет число валентных электронов больше восьми, традиционно подразумевает участие d-орбиталей в связывании. Однако общее мнение состоит в том, что, хотя они могут вносить незначительный вклад, участие d-орбиталей не имеет значения, а связывание так называемых гипервалентных молекул по большей части лучше объясняется вкладывающими формами с разделенными зарядами, которые изображают три -центральная четырехэлектронная связь . Тем не менее, по традиции, структуры расширенных октетов по-прежнему обычно рисуются для таких функциональных групп, как, например, сульфоксиды , сульфоны и илиды фосфора . Рассматриваемые как формализм, который не обязательно отражает истинную электронную структуру, ИЮПАК предпочитает такие изображения структурам с частичными связями, разделением зарядов или дативными связями . [21]
Эквивалентные участники вносят одинаковый вклад в фактическую структуру, тогда как важность неэквивалентных участников определяется степенью их соответствия перечисленным выше свойствам. Большее количество значимых структур и более объемное пространство, доступное для делокализованных электронов, приводят к стабилизации (понижению энергии) молекулы.
В бензоле две циклогексатриеновые структуры Кекуле , впервые предложенные Кекуле , взяты вместе как способствующие структуры, чтобы представить общую структуру. В гибридной структуре справа пунктирный шестиугольник заменяет три двойные связи и представляет шесть электронов в наборе из трех молекулярных орбиталей π - симметрии с узловой плоскостью в плоскости молекулы.
В фуране неподеленная пара атома кислорода взаимодействует с π-орбиталями атомов углерода. Изогнутые стрелки изображают перестановку делокализованных π-электронов , в результате которой вносят разные вклады.
Молекула озона представлена двумя участвующими структурами. В действительности два концевых атома кислорода эквивалентны, и гибридная структура изображена справа с зарядом - 1 ⁄ 2 как на атомах кислорода, так и на частичных двойных связях сплошной и пунктирной линией и порядком связи 1.+1 ⁄ 2 . [22] [23]
Для гипервалентных молекул описанная выше рационализация может быть применена для создания структур, способствующих объяснению связей в таких молекулах. Ниже показаны структуры, способствующие образованию связи 3c-4e в дифториде ксенона .
Аллильный катион имеет две способствующие структуры с положительным зарядом на концевых атомах углерода. В гибридной структуре их заряд равен + 1 ⁄ 2 . Полный положительный заряд также можно изобразить как делокализованный между тремя атомами углерода.
Молекула диборана описывается участвующими структурами, каждая из которых имеет дефицит электронов на разных атомах . Это уменьшает дефицит электронов на каждом атоме и стабилизирует молекулу. Ниже приведены структуры, способствующие отдельной связи 3c-2e в диборане.
Часто реакционноспособные промежуточные соединения, такие как карбокатионы и свободные радикалы, имеют более делокализованную структуру, чем их исходные реагенты, что приводит к образованию неожиданных продуктов. Классический пример — аллильная перегруппировка . Когда 1 моль HCl присоединяется к 1 молю 1,3-бутадиена, помимо обычно ожидаемого продукта 3-хлор-1-бутена мы также обнаруживаем 1-хлор-2-бутен. Эксперименты по мечению изотопов показали, что здесь происходит то, что дополнительная двойная связь смещается из положения 1,2 в положение 2,3 в некоторых продуктах. Это и другие данные (например, ЯМР в растворах суперкислот ) показывают, что промежуточный карбокатион должен иметь сильно делокализованную структуру, отличную от его в основном классической (делокализация существует, но невелика) исходной молекулы. Этот катион (аллильный катион) можно представить с помощью резонанса, как показано выше.
Это наблюдение большей делокализации в менее стабильных молекулах является весьма общим. Возбужденные состояния сопряженных диенов стабилизируются в большей степени за счет сопряжения, чем их основные состояния, в результате чего они становятся органическими красителями.
Хорошо изученный пример делокализации без участия π-электронов ( гиперконъюгация ) можно наблюдать в неклассическом катионе 2-норборнила . Другой пример - метан ( CH+
5). Их можно рассматривать как содержащие трехцентровые двухэлектронные связи и они представлены либо вносящими вклад структурами, включающими перегруппировку σ-электронов, либо специальным обозначением Y, в трех точках которого находятся три ядра.
Делокализованные электроны важны по нескольким причинам; Главный из них заключается в том, что ожидаемая химическая реакция может не произойти, поскольку электроны делокализуются в более стабильную конфигурацию, в результате чего реакция происходит в другом месте. Примером может служить алкилирование бензола по Фриделю-Крафтсу 1-хлор-2-метилпропаном; карбокатион перегруппировывается в трет - бутильную группу , стабилизированную гиперконъюгацией , особой формой делокализации. Делокализация приводит к удлинению длины волны электрона, следовательно, уменьшает энергию.
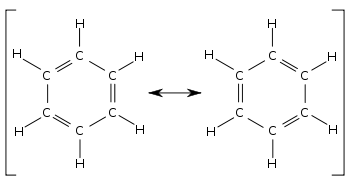
При сравнении двух участвующих структур бензола все одинарные и двойные связи меняются местами. Длины связей можно измерить, например, с помощью дифракции рентгеновских лучей . Средняя длина одинарной связи C–C составляет 154 пм ; для двойной связи C=C — 133 пм. В локализованном циклогексатриене связи углерод-углерод должны чередоваться 154 и 133 пм. Вместо этого обнаружено, что все связи углерод-углерод в бензоле имеют длину около 139 пм, что является промежуточной длиной связи между одинарной и двойной связью. Этот смешанный характер одинарных и двойных (или тройных) связей типичен для всех молекул, в которых связи имеют разный порядок связей в разных участвующих структурах. Длину облигаций можно сравнить с помощью ордеров на облигации. Например, в циклогексане порядок связи равен 1, а в бензоле - 1 + (3 ÷ 6) = 1.+1 ⁄ 2 . Следовательно, бензол имеет более двойную связь и, следовательно, более короткую длину связи, чем циклогексан.
Энергия резонанса (или делокализации) — это количество энергии, необходимое для преобразования истинной делокализованной структуры в структуру наиболее стабильной способствующей структуры. Эмпирическую резонансную энергию можно оценить путем сравнения изменения энтальпии гидрирования реального вещества с оценкой для вносящей вклад структуры.
Полное гидрирование бензола до циклогексана через 1,3-циклогексадиен и циклогексен является экзотермическим ; 1 моль бензола дает 208,4 кДж (49,8 ккал).
Гидрирование одного моля двойных связей дает 119,7 кДж (28,6 ккал), как следует из последнего этапа - гидрирования циклогексена. Однако в бензоле для гидрирования одного моля двойных связей необходимо 23,4 кДж (5,6 ккал). Разница, составляющая 143,1 кДж (34,2 ккал), представляет собой эмпирическую резонансную энергию бензола. Поскольку 1,3-циклогексадиен также имеет небольшую энергию делокализации (7,6 кДж или 1,8 ккал/моль), чистая резонансная энергия по сравнению с локализованным циклогексатриеном немного выше: 151 кДж или 36 ккал/моль. [24]
Эта измеренная резонансная энергия также представляет собой разницу между энергией гидрирования трех «нерезонансных» двойных связей и измеренной энергией гидрирования:
Независимо от их точных значений, резонансные энергии различных родственных соединений позволяют лучше понять их связь. Резонансные энергии пиррола , тиофена и фурана составляют соответственно 88, 121 и 67 кДж/моль (21, 29 и 16 ккал/моль). [26] Таким образом, эти гетероциклы гораздо менее ароматичны, чем бензол, что проявляется в лабильности этих колец.

Резонанс имеет более глубокое значение в математическом аппарате теории валентных связей (ВС). Квантовая механика требует, чтобы волновая функция молекулы подчинялась наблюдаемой симметрии. Если какая-то одна структура не достигает этого, возникает резонанс.
Например, в бензоле теория валентных связей начинается с двух структур Кекуле, которые по отдельности не обладают шестикратной симметрией реальной молекулы. Теория строит реальную волновую функцию как линейную суперпозицию волновых функций, представляющих две структуры. Поскольку обе структуры Кекуле имеют одинаковую энергию, они вносят одинаковый вклад в общую структуру - суперпозиция представляет собой равновзвешенное среднее или линейную комбинацию этих двух в соотношении 1:1 в случае бензола. Как показано, симметричная комбинация дает основное состояние, а антисимметричная комбинация дает первое возбужденное состояние .
Обычно суперпозиция записывается с неопределенными коэффициентами, которые затем вариационно оптимизируются , чтобы найти минимально возможную энергию для данного набора базисных волновых функций. Когда включено больше вносящих вклад структур, молекулярная волновая функция становится более точной, и больше возбужденных состояний можно получить из различных комбинаций вносящих вклад структур.

В теории молекулярных орбиталей , основной альтернативе теории валентных связей , молекулярные орбитали (МО) аппроксимируются как суммы всех атомных орбиталей (АО) на всех атомах; МО столько же, сколько и АО. Каждый АО i имеет весовой коэффициент c i , который указывает вклад АО в конкретную МО. Например, в бензоле модель МО дает нам 6 π-МО, которые представляют собой комбинации 2p z АО на каждом из 6 атомов C. Таким образом, каждая π-МО делокализована по всей молекуле бензола, а любой электрон, занимающий МО, будет делокализован по всей молекуле. Эта интерпретация МО вдохновила представление о бензольном кольце как шестиугольнике с кругом внутри. При описании бензола в курсах элементарной химии часто объединяют концепцию ВБ о локализованных σ-связях и концепцию МО о делокализованных π-орбиталях.
Структуры, способствующие модели VB, особенно полезны для прогнозирования влияния заместителей на π-системы, такие как бензол. Они приводят к моделям способствующих структур электроноакцепторной группы и электроновысвобождающей группы бензола. Полезность теории МО заключается в том, что количественное указание заряда π-системы на атоме можно получить из квадратов весового коэффициента c i на атоме C i . Заряд q i ≈ c2
я. Причина возведения коэффициента в квадрат заключается в том, что если электрон описывается АО, то квадрат АО дает плотность электронов . АО корректируются ( нормализуются ) так, что AO 2 = 1 и q i ≈ ( c i AO i ) 2 ≈ c2
я. В бензоле q i = 1 на каждом атоме углерода. С электроноакцепторной группой q i < 1 на орто- и пара -атомах С и q i > 1 для электроно-отдающей группы .
Взвешивание вносящих вклад структур с точки зрения их вклада в общую структуру можно рассчитать несколькими способами, используя методы «Ab initio» , полученные из теории валентных связей, или же из подходов орбиталей естественных связей (NBO) Weinhold NBO5. Архивировано 2008 г. 02-08 на Wayback Machine или, наконец, на основе эмпирических расчетов на основе метода Хюккеля. Программное обеспечение для обучения резонансу, основанное на методе Хюккеля, доступно на веб-сайте HuLiS.
В случае ионов принято говорить о делокализованном заряде (делокализации заряда). Пример делокализованного заряда ионов можно найти в карбоксилатной группе, в которой отрицательный заряд одинаково сосредоточен на двух атомах кислорода. Делокализация заряда анионов является важным фактором, определяющим их реакционную способность (обычно: чем выше степень делокализации, тем ниже реакционная способность) и, в частности, кислотную силу сопряженных с ними кислот. Как правило, чем лучше делокализован заряд аниона, тем сильнее его сопряженная кислота . Например, отрицательный заряд перхлорат- аниона ( ClO−
4) равномерно распределен среди симметрично ориентированных атомов кислорода (причем часть его удерживается и центральным атомом хлора). Эта превосходная делокализация заряда в сочетании с большим количеством атомов кислорода (четыре) и высокой электроотрицательностью центрального атома хлора приводит к тому, что хлорная кислота является одной из самых сильных известных кислот со значением ap K -10 . [28]
Степень делокализации заряда в анионе может быть количественно выражена с помощью параметра WAPS (средневзвешенная положительная сигма) [29] , а аналогичный параметр WANS (средневзвешенная отрицательная сигма) [30] [31] используется для катионов. .
Значения WAPS и WANS указаны в e / Å 4 . Большие значения указывают на более локализованный заряд соответствующего иона.
Резонансный гибрид более стабилен, чем любая из участвующих структур.
{{cite web}}: CS1 maint: bot: исходный статус URL неизвестен ( ссылка )См. последний абзац раздела 1.