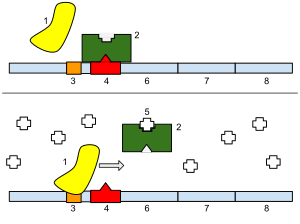
В молекулярной генетике репрессор — это ДНК- или РНК-связывающий белок, который ингибирует экспрессию одного или нескольких генов путем связывания с оператором или связанными с ним сайленсерами . ДНК-связывающий репрессор блокирует прикрепление РНК-полимеразы к промотору , тем самым предотвращая транскрипцию генов в информационную РНК . РНК-связывающий репрессор связывается с мРНК и предотвращает трансляцию мРНК в белок. Эта блокировка или уменьшение выражения называется репрессией.
Если присутствует индуктор , молекула, которая инициирует экспрессию гена, то она может взаимодействовать с белком-репрессором и отделять его от оператора. Затем РНК-полимераза может транскрибировать сообщение (экспрессируя ген). Корепрессор — это молекула , которая может связываться с репрессором и заставлять его прочно связываться с оператором, что снижает транскрипцию.
Репрессор, который связывается с ко-репрессором, называется апорепрессором или неактивным репрессором . Одним из типов апорепрессоров является репрессор trp , важный метаболический белок бактерий. Вышеописанный механизм репрессии является разновидностью механизма обратной связи, поскольку он позволяет осуществлять транскрипцию только при наличии определенного условия: присутствия специфического индуктора (ов). Напротив, активный репрессор напрямую связывается с оператором, подавляющим экспрессию гена.
Хотя репрессоры чаще встречаются у прокариот, у эукариот они встречаются редко. Более того, большинство известных эукариотических репрессоров обнаружены в простых организмах (например, дрожжах) и действуют путем непосредственного взаимодействия с активаторами. [1] Это контрастирует с прокариотическими репрессорами, которые также могут изменять структуру ДНК или РНК.
В геноме эукариот имеются участки ДНК, известные как сайленсеры . Это последовательности ДНК, которые связываются с репрессорами, частично или полностью подавляя ген. Сайленсеры могут располагаться на несколько оснований выше или ниже фактического промотора гена. Репрессоры также могут иметь два сайта связывания: один для сайленсера и один для промотора . Это вызывает петлеобразование хромосомы, позволяя промоторной области и сайленсерной области приближаться друг к другу.
В опероне lacZYA находятся гены, кодирующие белки, необходимые для расщепления лактозы. [2] Ген lacI кодирует белок, называемый «репрессором» или «lac-репрессором», который действует как репрессор lac-оперона. [2] Ген lacI расположен непосредственно перед lacZYA , но транскрибируется с промотора lacI . [2] Ген lacI синтезирует белок-репрессор LacI. Белок-репрессор LacI репрессирует lacZYA путем связывания с операторной последовательностью lacO . [2]
Репрессор lac конститутивно экспрессируется и обычно связан с операторной областью промотора , что препятствует способности РНК-полимеразы (РНКП) начинать транскрипцию оперона lac . [2] В присутствии индуктора аллолактозы репрессор меняет конформацию, снижает силу связывания с ДНК и диссоциирует от операторной последовательности ДНК в промоторной области lac-оперонга. Затем РНКП может связаться с промотором и начать транскрипцию гена lacZYA . [2]
Примером белка-репрессора является репрессор метионина MetJ. MetJ взаимодействует с основаниями ДНК посредством мотива лента-спираль-спираль (RHH). [3] MetJ представляет собой гомодимер, состоящий из двух мономеров , каждый из которых представляет собой бета-ленту и альфа-спираль . Вместе бета-ленты каждого мономера собираются вместе, образуя антипараллельный бета-лист , который связывается с оператором ДНК («Met-бокс») в своей главной бороздке. После связывания димер MetJ взаимодействует с другим димером MetJ, связанным с комплементарной цепью оператора через его альфа-спирали. AdoMet связывается с карманом MetJ, который не перекрывает сайт связывания ДНК.
Мет-бокс содержит последовательность ДНК AGACGTCT, палиндром (он демонстрирует диадную симметрию ), позволяющий распознавать одну и ту же последовательность на любой цепи ДНК. Соединение между C и G в середине Met-бокса содержит пиримидин-пуриновую ступень, которая становится положительно сверхспиральной , образуя излом в фосфодиэфирной основной цепи. Именно так белок проверяет сайт узнавания, поскольку это позволяет дуплексу ДНК повторять форму белка. Другими словами, распознавание происходит посредством косвенного считывания структурных параметров ДНК, а не посредством распознавания конкретной последовательности оснований.
Каждый димер MetJ содержит два сайта связывания для кофактора S-аденозилметионина (SAM), который является продуктом биосинтеза метионина. Когда присутствует SAM, он связывается с белком MetJ, увеличивая его сродство к родственному операторному сайту, что останавливает транскрипцию генов, участвующих в синтезе метионина. Когда концентрация SAM становится низкой, репрессор отделяется от оператора, позволяя производить больше метионина.
В опероне L-арабинозы находятся гены, кодирующие ферменты, расщепляющие арабинозу. Они действуют, расщепляя арабинозу как альтернативный источник энергии, когда глюкоза низкая или отсутствует. [4] Оперон состоит из регуляторного гена-репрессора (araC), трех контрольных сайтов (ara02, ara01, araI1 и araI2), двух промоторов (Parac/ParaBAD) и трех структурных генов (araBAD) . После образования araC действует как репрессор, связываясь с областью araI с образованием петли, которая предотвращает связывание полимераз с промотором и транскрипцию структурных генов в белки.
В отсутствие арабинозы и araC (репрессора) образование петель не инициируется, и экспрессия структурных генов будет ниже. В отсутствие арабинозы, но в присутствии araC, области araC образуют димеры и связываются, сближая домены ara02 и araI1 путем образования петли. [5] В присутствии арабинозы и araC araC связывается с арабинозой и действует как активатор. Это конформационное изменение в araC больше не может образовывать петлю, а линейный сегмент гена способствует рекрутированию РНК-полимеразы в структурную область araBAD. [4]

+
Оперон FLC представляет собой консервативный эукариотический локус, который отрицательно связан с цветением посредством репрессии генов, необходимых для развития меристемы для переключения в цветочное состояние у видов растений Arabidopsis thaliana . Было показано, что экспрессия FLC регулируется присутствием FRIGIDA и отрицательно коррелирует со снижением температуры, что приводит к предотвращению яровизации . [6] Степень снижения экспрессии зависит от температуры и времени воздействия в зависимости от сезона. После снижения экспрессии FLC появляется возможность цветения. В регуляции экспрессии FLC участвуют как генетические, так и эпигенетические факторы, такие как метилирование гистонов и метилирование ДНК . [7] Кроме того, ряд генов являются кофакторами и действуют как негативные факторы транскрипции для генов FLC. [8] Гены FLC также имеют большое количество гомологов у разных видов, что позволяет осуществлять специфическую адаптацию в различных климатических условиях. [9]