Скрытая теплота (также известная как скрытая энергия или теплота превращения ) — это энергия, выделяемая или поглощаемая телом или термодинамической системой в процессе при постоянной температуре — обычно фазовом переходе первого рода , таком как плавление или конденсация.
Скрытая теплота может пониматься как скрытая энергия, которая подается или извлекается для изменения состояния вещества без изменения его температуры или давления. Сюда входит скрытая теплота плавления (из твердого в жидкое), скрытая теплота испарения (из жидкого в газообразное) и скрытая теплота сублимации (из твердого в газообразное). [1] [2]
Термин был введен около 1762 года шотландским химиком Джозефом Блэком . Блэк использовал термин в контексте калориметрии , где передача тепла вызывала изменение объема тела, при этом его температура была постоянной.
В отличие от скрытого тепла, явное тепло — это энергия, передаваемая в виде тепла , что приводит к изменению температуры тела.
Термины явное тепло и скрытое тепло относятся к энергии, передаваемой между телом и его окружением, определяемой возникновением или отсутствием изменения температуры; они зависят от свойств тела. Явное тепло ощущается или ощущается в процессе как изменение температуры тела. Скрытое тепло — это энергия, передаваемая в процессе без изменения температуры тела, например, при фазовом переходе (твердое тело/жидкость/газ).
Как явное, так и скрытое тепло наблюдаются во многих процессах передачи энергии в природе. Скрытое тепло связано с изменением фазы атмосферной или океанической воды, испарением , конденсацией , замерзанием или таянием , тогда как явное тепло — это переданная энергия, которая проявляется в изменении температуры атмосферы, океана или льда без этих фазовых изменений, хотя оно связано с изменениями давления и объема.
Первоначальное использование термина, введенное Блэком, применялось к системам, которые намеренно поддерживались при постоянной температуре. Такое использование относилось к скрытой теплоте расширения и нескольким другим связанным скрытым теплотам. Эти скрытые теплоты определяются независимо от концептуальной основы термодинамики. [3]
Например, когда тело нагревается при постоянной температуре тепловым излучением в микроволновом поле, оно может расшириться на величину, описываемую его скрытой теплотой по отношению к объему или скрытой теплотой расширения , или увеличить свое давление на величину, описываемую его скрытой теплотой по отношению к давлению . [4]
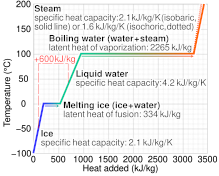
Скрытая теплота — это энергия, выделяемая или поглощаемая телом или термодинамической системой в процессе при постоянной температуре. Две распространенные формы скрытой теплоты — это скрытая теплота плавления ( плавления ) и скрытая теплота испарения ( кипения ). Эти названия описывают направление потока энергии при переходе из одной фазы в другую: из твердого состояния в жидкое и из жидкого в газообразное.
В обоих случаях изменение является эндотермическим , что означает, что система поглощает энергию. Например, когда вода испаряется, требуется затрата энергии, чтобы молекулы воды преодолели силы притяжения между ними и перешли из воды в пар.
Если пар затем конденсируется в жидкость на поверхности, то скрытая энергия пара, поглощенная во время испарения, высвобождается в виде явного тепла жидкости на поверхности.
Большое значение энтальпии конденсации водяного пара является причиной того, что пар является гораздо более эффективным теплоносителем, чем кипящая вода, и более опасен.
В метеорологии скрытый тепловой поток — это поток энергии от поверхности Земли в атмосферу , связанный с испарением или транспирацией воды на поверхности и последующей конденсацией водяного пара в тропосфере . Это важный компонент поверхностного энергетического баланса Земли. Скрытый тепловой поток обычно измеряется с помощью метода Боуэна или, с недавних пор, с середины 1900-х годов, методом вихревой ковариации .
.jpg/440px-William_Cullen_(cropped).jpg)
В 1748 году в «Эдинбургских физических и литературных очерках» был опубликован отчет об эксперименте шотландского врача и химика Уильяма Каллена . Каллен использовал воздушный насос , чтобы понизить давление в контейнере с диэтиловым эфиром . Тепло не отводилось от эфира, однако эфир кипел, но его температура снижалась. [5] [6] А в 1758 году, в теплый день в Кембридже , Англия, Бенджамин Франклин и его коллега-ученый Джон Хэдли экспериментировали, непрерывно смачивая шарик ртутного термометра эфиром и используя мехи для испарения эфира. [7] С каждым последующим испарением термометр показывал более низкую температуру, в конечном итоге достигая 7 °F (−14 °C). Другой термометр показал, что комнатная температура была постоянной и составляла 65 °F (18 °C). В своем письме « Охлаждение испарением » Франклин отметил, что «можно увидеть возможность замерзания человека до смерти в теплый летний день». [8]
.jpg/440px-Black_Joseph_(cropped).jpg)
Английское слово latent происходит от латинского latēns , что означает «лежащий, скрытый» . [9] [10] Термин «латентная теплота» был введен в калориметрию около 1750 года Джозефом Блэком по заказу производителей шотландского виски в поисках идеального количества топлива и воды для процесса дистилляции с целью изучения изменений системы, таких как объем и давление, когда термодинамическая система поддерживалась при постоянной температуре в термальной ванне.
Было известно, что когда температура воздуха поднимается выше точки замерзания — воздух тогда становится очевидным источником тепла — снег тает очень медленно, а температура растаявшего снега близка к точке замерзания. [5] В 1757 году Блэк начал исследовать, требуется ли тепло для плавления твердого тела, независимо от какого-либо повышения температуры. Насколько знал Блэк, в то время общее мнение состояло в том, что плавление неизбежно сопровождается небольшим повышением температуры, и что не требуется больше тепла, чем то, что потребовало бы само по себе повышение температуры. Вскоре, однако, Блэк смог показать, что во время плавления требуется гораздо больше тепла, чем можно было бы объяснить только повышением температуры. [11] [12] Он также смог показать, что тепло выделяется жидкостью во время ее замерзания; опять же, гораздо больше, чем можно было бы объяснить только понижением ее температуры. [13]
Блэк сравнил бы изменение температуры двух одинаковых количеств воды, нагретых одинаковыми способами, одно из которых, скажем, было растоплено изо льда, тогда как другое было нагрето из просто холодного жидкого состояния. Сравнивая полученные температуры, он мог бы сделать вывод, что, например, температура образца, растопленного изо льда, была на 140 °F ниже, чем у другого образца, таким образом, расплавляя лед, он поглотил 140 «градусов тепла», которые не могли быть измерены термометром, но которые необходимо было подать, таким образом, они были «латентными» (скрытыми). Блэк также вывел, что столько же скрытого тепла, сколько было подано на кипение дистиллята (таким образом, давая необходимое количество топлива), также должно было быть поглощено для его повторной конденсации (таким образом, давая требуемую охлаждающую воду). [14]
В 1762 году Блэк объявил о следующих исследованиях и результатах обществу профессоров Университета Глазго. [15] Блэк поместил равные массы льда при температуре 32 °F (0 °C) и воды при температуре 33 °F (0,6 °C) соответственно в два идентичных, хорошо разделенных контейнера. Вода и лед были равномерно нагреты до 40 °F воздухом в комнате, который был при постоянной температуре 47 °F (8 °C). Таким образом, вода получила 40 – 33 = 7 «градусов тепла». Лед нагревался в 21 раз дольше и, следовательно, получил 7 × 21 = 147 «градусов тепла». [a] Температура льда увеличилась на 8 °F. Теперь лед хранил, так сказать, дополнительные 8 «градусов тепла» в форме, которую Блэк назвал явным теплом , проявляющимся как температура, которую можно было почувствовать и измерить. 147 – 8 = 139 «степеней тепла» были, так сказать, сохранены в виде скрытого тепла , не проявляя себя. [16] [17] (В современной термодинамике идея содержащегося тепла была отвергнута, поэтому явное тепло и скрытое тепло были переопределены. Они нигде не находятся.)
Затем Блэк показал, что для того, чтобы растопить такую же массу льда, пока она не станет 32 °F, нужна температура воды 176 °F. Так что теперь для того, чтобы растопить лед, требовалось 176 – 32 = 144 «градуса тепла». Современное значение теплоты плавления льда составило бы 143 «градуса тепла» по той же шкале (79,5 «градуса тепла по Цельсию»). [18] [15]
Наконец, Блэк увеличил температуру и испарил соответственно две равные массы воды посредством равномерного нагрева. Он показал, что для испарения необходимо 830 «градусов тепла»; опять же, исходя из требуемого времени. Современное значение теплоты испарения воды составило бы 967 «градусов тепла» по той же шкале. [19]
Позднее Джеймс Прескотт Джоуль охарактеризовал скрытую энергию как энергию взаимодействия в данной конфигурации частиц, т. е. форму потенциальной энергии , а явное тепло — как энергию, которая указывается термометром, [20] связав последнее с тепловой энергией .
Удельная скрытая теплота ( L ) выражает количество энергии в форме тепла ( Q ) , необходимое для полного осуществления фазового перехода единицы массы ( m ), обычно 1 кг , вещества как интенсивного свойства :
Интенсивные свойства являются материальными характеристиками и не зависят от размера или объема образца. Обычно в литературе цитируются и табулируются удельная скрытая теплота плавления и удельная скрытая теплота испарения для многих веществ.
Из этого определения скрытая теплота для данной массы вещества рассчитывается по формуле
где:
В следующей таблице показаны удельные скрытые теплоты и температуры фазового перехода (при стандартном давлении) некоторых распространенных жидкостей и газов. [ необходима ссылка ]
Удельная скрытая теплота конденсации воды в диапазоне температур от −25 °C до 40 °C аппроксимируется следующей эмпирической кубической функцией:
где температура принимается в виде числового значения в °C.
При сублимации и осаждении из льда и в лед удельная скрытая теплота практически постоянна в диапазоне температур от −40 °C до 0 °C и может быть аппроксимирована следующей эмпирической квадратичной функцией:

Когда температура (или давление) повышается до критической точки , скрытая теплота парообразования падает до нуля.
Я склонен полагать, что обе эти гипотезы окажутся верными, — что в некоторых случаях, особенно в случае явного тепла или такого, на которое указывает термометр, будет обнаружено, что тепло состоит из живой силы частиц тел, в которых оно индуцируется; тогда как в других случаях, особенно в случае скрытого тепла, явления производятся путем разделения частиц друг от друга, заставляя их притягиваться друг к другу через большее пространство., Лекция о материи, живой силе и тепле. 5 и 12 мая 1847 г.