При атмосферном давлении в зависимости от температуры существуют три аллотропные формы железа : альфа-железо (α-Fe, феррит) , гамма-железо (γ-Fe, аустенит) и дельта-железо (δ-Fe). При очень высоком давлении существует четвертая форма, эпсилон-железо (ε-Fe, гексаферрум) . Некоторые противоречивые экспериментальные данные предполагают существование пятой формы высокого давления, которая стабильна при очень высоких давлениях и температурах. [1]
Фазы железа при атмосферном давлении важны из-за различий в растворимости углерода , образующего разные типы стали . Фазы железа высокого давления важны как модели твердых частей планетных ядер. Обычно предполагается , что внутреннее ядро Земли состоит в основном из кристаллического железо-никелевого сплава с ε-структурой. [2] [3] [4] Считается, что внешнее ядро, окружающее твердое внутреннее ядро, состоит из жидкого железа, смешанного с никелем и следами более легких элементов.
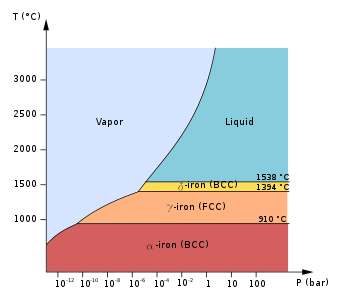
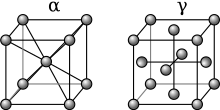
При температуре ниже 912 ° C (1674 ° F) железо имеет объемно-центрированную кубическую (ОЦК) кристаллическую структуру и известно как α-железо или феррит . Это термодинамически стабильный и довольно мягкий металл. α-Fe может подвергаться давлению до ок. 15 ГПа, прежде чем превратиться в форму высокого давления, называемую ε-Fe, обсуждаемую ниже.
В магнитном отношении α-железо парамагнитно при высоких температурах. Однако ниже температуры Кюри ( TC или A2 ) 771 °C (1044K или 1420 °F) [ 5] он становится ферромагнитным . Раньше парамагнитная форма α-железа была известна как бета-железо (β-Fe). [6] [7] Несмотря на то, что небольшое тетрагональное искажение в ферромагнитном состоянии действительно представляет собой настоящий фазовый переход, непрерывный характер этого перехода приводит к лишь незначительному значению при термообработке стали . Линия А 2 образует границу между полями бета-железа и альфа на фазовой диаграмме на рисунке 1.
Точно так же граница A 2 имеет лишь второстепенное значение по сравнению с критическими температурами A 1 ( эвтектоид ), A 3 и A cm . Поле A cm , где аустенит находится в равновесии с цементитом + γ-Fe, находится за правым краем на рис. 1. Поле фазы α + γ технически представляет собой поле β + γ над полем A 2 . Обозначение бета сохраняет непрерывность последовательности греческих букв фаз в железе и стали: α-Fe, β-Fe, аустенит (γ-Fe), высокотемпературное δ-Fe и гексаферрум высокого давления (ε-Fe). .

Первичной фазой низкоуглеродистой или мягкой стали и большинства чугунов при комнатной температуре является ферромагнитный α-Fe. [8] [9] Его твердость составляет около 80 по Бринеллю . [10] [11] Максимальная растворимость углерода составляет около 0,02% масс. при 727 °C (1341 °F) и 0,001% при 0 °C (32 °F). [12] Когда он растворяется в железе, атомы углерода занимают межузельные «дырки». Будучи примерно в два раза больше диаметра тетраэдрического отверстия , углерод создает сильное поле локальных деформаций.
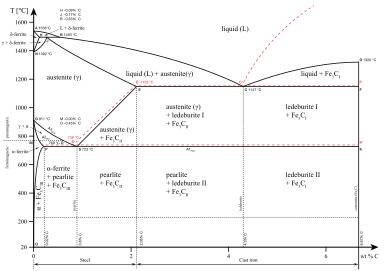
Мягкая сталь (углеродистая сталь с содержанием C примерно до 0,2 мас.%) состоит в основном из α-Fe и увеличивающегося количества цементита (Fe 3 C, карбида железа). Смесь имеет пластинчатую структуру, называемую перлитом . Поскольку бейнит и перлит содержат α-Fe в качестве компонента, любой железо-углеродный сплав будет содержать некоторое количество α-Fe, если ему позволить достичь равновесия при комнатной температуре. Количество α-Fe зависит от процесса охлаждения.

β-Fe и критическая температура A 2 важны при индукционном нагреве стали, например, при термообработке поверхностной закалки. Сталь обычно аустенитируют при температуре 900–1000 °C перед закалкой и отпуском . Высокочастотное переменное магнитное поле индукционного нагрева нагревает сталь ниже температуры Кюри по двум механизмам: резистивный или джоулевый нагрев и потери на ферромагнитный гистерезис . Выше границы А 2 механизм гистерезиса исчезает и требуемое количество энергии на градус повышения температуры, таким образом, существенно больше, чем ниже А 2 . Для изменения импеданса индукционного источника питания и компенсации этого изменения могут потребоваться схемы согласования нагрузки . [13]
При нагревании железа выше 912 ° C (1674 ° F) его кристаллическая структура меняется на гранецентрированную кубическую (ГЦК) кристаллическую структуру. В такой форме его называют гамма-железом (γ-Fe) или аустенитом . γ-железо может растворять значительно больше углерода (до 2,04% по массе при 1146 ° C). Эта γ-форма насыщения углеродом проявляется в аустенитной нержавеющей стали .
Примечательно, что при температуре выше 1394 °C (2541 °F) железо снова переходит в ОЦК-структуру, известную как δ-Fe. [14] δ-железо может растворять до 0,08% углерода по массе при температуре 1475 °C. Он стабилен до температуры плавления 1538 ° C (2800 ° F). δ-Fe не может существовать при давлении выше 5,2 ГПа, вместо этого аустенит переходит непосредственно в расплавленную фазу при таких высоких давлениях. [15]
При давлениях выше примерно 10–13 ГПа и температурах примерно до 700 К α-железо превращается в гексагональную плотноупакованную (ГПУ) структуру, которая также известна как ε-железо или гексаферрум; [16] более высокотемпературная γ-фаза также превращается в ε-железо, но обычно требует гораздо более высоких давлений при повышении температуры. Тройная точка гексаферрума, феррита и аустенита составляет 10,5 ГПа при 750 К. [15] Обнаружен антиферромагнетизм в сплавах эпсилон-Fe с Mn, Os и Ru. [17]
Альтернативная стабильная форма, если она существует, может появиться при давлении не менее 50 ГПа и температуре не менее 1500 К; Считалось, что он имеет ромбическую или двойную ГПУ-структуру. [1] По состоянию на декабрь 2011 года [обновлять]недавние и продолжающиеся эксперименты проводятся с аллотропами углерода под высоким давлением и сверхплотностью .
Температура плавления железа экспериментально хорошо определена при давлениях менее 50 ГПа.
Для более высоких давлений опубликованные данные (по состоянию на 2007 год) помещают тройную точку γ-ε-жидкости при давлениях, которые различаются на десятки гигапаскалей и 1000 К в температуре плавления. Вообще говоря, компьютерное моделирование молекулярной динамики плавления железа и эксперименты с ударной волной предполагают более высокие температуры плавления и гораздо более крутой наклон кривой плавления, чем статические эксперименты, проводимые в ячейках с алмазными наковальнями . [18]
Точки плавления и кипения железа, а также его энтальпия атомизации ниже, чем у 3d-элементов более ранней группы, от скандия до хрома , что указывает на меньший вклад 3d-электронов в металлическую связь, поскольку они все больше и больше притягиваются к инертное ядро у ядра ; Однако в [19] они выше, чем значения для предыдущего элемента марганца, поскольку этот элемент имеет наполовину заполненную 3d подоболочку и, следовательно, его d-электроны нелегко делокализовать . Та же самая тенденция наблюдается для рутения, но не для осмия . [20]
Точные температуры, при которых железо перейдет из одной кристаллической структуры в другую, зависит от того, сколько и какого типа других элементов растворено в железе. Фазовая граница между различными твердыми фазами проводится на бинарной фазовой диаграмме , обычно изображаемой как зависимость температуры от процентного содержания железа. Добавление некоторых элементов, таких как хром , сужает температурный диапазон гамма-фазы, тогда как другие увеличивают температурный диапазон гамма-фазы. В элементах, уменьшающих диапазон гамма-фаз, граница фаз альфа-гамма соединяется с границей фаз гамма-дельта, образуя то, что обычно называют гамма-петлей . Добавление добавок гамма-петли сохраняет чугун в объемноцентрированной кубической структуре и предотвращает фазовый переход стали в другие твердые состояния. [21]