
В биохимии фосфатаза представляет собой фермент , который использует воду для расщепления моноэфира фосфорной кислоты на ион фосфата и спирт . Поскольку фермент фосфатаза катализирует гидролиз своего субстрата , он относится к подкатегории гидролаз . [1] Ферменты фосфатазы необходимы для многих биологических функций, поскольку фосфорилирование (например, с помощью протеинкиназ ) и дефосфорилирование (с помощью фосфатаз) выполняют разнообразные роли в клеточной регуляции и передаче сигналов . [2] В то время как фосфатазы удаляют фосфатные группы из молекул, киназы катализируют перенос фосфатных групп к молекулам из АТФ . Вместе киназы и фосфатазы управляют формой посттрансляционной модификации , которая важна для регуляторной сети клетки. [3]
Ферменты фосфатазы не следует путать с ферментами фосфорилазами , которые катализируют перенос фосфатной группы от гидрофосфата к акцептору. Из-за своей распространенности в клеточной регуляции фосфатазы представляют собой область интереса для фармацевтических исследований. [4] [5]

Фосфатазы катализируют гидролиз фосфомоноэфира, удаляя фосфатный фрагмент из субстрата. В ходе реакции вода расщепляется, при этом группа -ОН присоединяется к фосфат-иону, а H+ протонирует гидроксильную группу другого продукта. Конечным результатом реакции является разрушение фосфомоноэфира и создание как фосфат-иона, так и молекулы со свободной гидроксильной группой. [4]
Фосфатазы способны с большой специфичностью дефосфорилировать, казалось бы, разные участки своих субстратов. Идентификация «кода фосфатазы», то есть механизмов и правил, которые управляют распознаванием субстратов фосфатаз, все еще находится в стадии разработки, но теперь доступен первый сравнительный анализ всех протеинфосфатаз, кодируемых в девяти «фосфатомных» геномах эукариот . [6] Исследования показывают, что так называемые «стыковочные взаимодействия» играют значительную роль в связывании субстрата. [3] Фосфатаза распознает различные мотивы (элементы вторичной структуры) на своем субстрате и взаимодействует с ними; эти мотивы связываются с низким сродством с сайтами стыковки фосфатазы, которые не содержатся в ее активном сайте . Хотя каждое отдельное стыковочное взаимодействие является слабым, многие взаимодействия происходят одновременно, оказывая кумулятивный эффект на специфичность связывания. [7] Стыковочные взаимодействия могут также аллостерически регулировать фосфатазы и, таким образом, влиять на их каталитическую активность. [8]
В отличие от киназ, ферменты фосфатазы распознают и катализируют более широкий спектр субстратов и реакций. Например, у людей количество киназ Ser/Thr превышает количество фосфатаз Ser/Thr в десять раз. [4] В некоторой степени это несоответствие является результатом неполного знания человеческого фосфатома , то есть полного набора фосфатаз, экспрессируемых в клетке, ткани или организме. [3] Многие фосфатазы еще предстоит открыть, а для многих известных фосфатаз еще не идентифицирован субстрат. Однако среди хорошо изученных пар фосфатаза/киназа фосфатазы демонстрируют большее разнообразие, чем их аналоги киназы, как по форме, так и по функциям; это может быть результатом меньшей степени консервативности фосфатаз. [4]

Фосфатазы не следует путать с фосфорилазами , которые добавляют фосфатные группы.
Протеинфосфатаза — это фермент , который дефосфорилирует аминокислотный остаток своего белкового субстрата. В то время как протеинкиназы действуют как сигнальные молекулы путем фосфорилирования белков, фосфатазы удаляют фосфатную группу, что важно для того, чтобы система внутриклеточной передачи сигналов могла перенастроиться для будущего использования. Тандемная работа киназ и фосфатаз представляет собой важный элемент регуляторной сети клетки. [9] Фосфорилирование (и дефосфорилирование) является одним из наиболее распространенных способов посттрансляционной модификации белков, и, по оценкам, в любой момент времени до 30% всех белков фосфорилируются. [10] [11] Двумя известными протеинфосфатазами являются PP2A и PP2B. PP2A участвует во многих регуляторных процессах, таких как репликация ДНК, метаболизм, транскрипция и развитие. PP2B, также называемый кальциневрином , участвует в пролиферации Т-клеток ; из-за этого он является мишенью некоторых лекарств, направленных на подавление иммунной системы. [9]
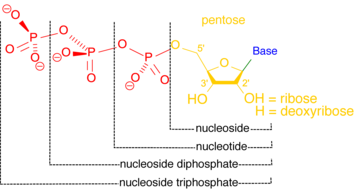
Нуклеотидаза — фермент, катализирующий гидролиз нуклеотида с образованием нуклеозида и фосфат-иона . [12] Нуклеотидазы необходимы для клеточного гомеостаза , поскольку они частично ответственны за поддержание сбалансированного соотношения нуклеотидов и нуклеозидов. [13] Некоторые нуклеотидазы функционируют вне клетки, создавая нуклеозиды, которые могут транспортироваться в клетку и использоваться для регенерации нуклеотидов посредством путей спасения . [14] Внутри клетки нуклеотидазы могут помочь поддерживать уровень энергии в условиях стресса. Клетка, лишенная кислорода и питательных веществ, может катаболизировать больше нуклеотидов, повышая уровень нуклеозидтрифосфатов, таких как АТФ , основной энергетической валюты клетки. [15]
Фосфатазы могут также действовать на углеводы , например, на промежуточные продукты глюконеогенеза . Глюконеогенез — это путь биосинтеза , при котором глюкоза создается из неуглеводных предшественников; этот путь важен, поскольку многие ткани могут получать энергию только из глюкозы. [9] Две фосфатазы, глюкозо-6-фосфатаза и фруктозо-1,6-бисфосфатаза, катализируют необратимые этапы глюконеогенеза. [16] [17] Каждый из них отщепляет фосфатную группу от шестиуглеродного промежуточного продукта сахарофосфата .
В пределах более широкого класса фосфатаз Комиссия по ферментам выделяет 104 различных семейства ферментов. Фосфатазы классифицируются по субстратной специфичности и гомологии последовательностей в каталитических доменах. [3] Несмотря на их классификацию на более чем сто семейств, все фосфатазы по-прежнему катализируют одну и ту же общую реакцию гидролиза. [1]
В экспериментах in vitro ферменты фосфатазы, по-видимому, распознают множество различных субстратов, и один субстрат может распознаваться многими различными фосфатазами. Однако эксперименты, проведенные in vivo, показали, что ферменты фосфатазы невероятно специфичны. [3] В некоторых случаях протеинфосфатаза (т.е. определенная по распознаванию белковых субстратов) может катализировать дефосфорилирование небелковых субстратов. [4] Аналогично, тирозинфосфатазы с двойной специфичностью могут дефосфорилировать не только остатки тирозина , но и остатки серина . Таким образом, одна фосфатаза может проявлять качества нескольких семейств фосфатаз. [9]
{{cite book}}: CS1 maint: multiple names: authors list (link)