В органической химии функциональная группа — это заместитель или фрагмент в молекуле , который вызывает характерные химические реакции молекулы . Одна и та же функциональная группа будет подвергаться тем же или подобным химическим реакциям независимо от остальной части состава молекулы. [1] [2] Это позволяет систематически прогнозировать химические реакции и поведение химических соединений , а также проектировать химический синтез . Реакционная способность функциональной группы может быть изменена другими функциональными группами поблизости. Взаимопревращение функциональных групп может использоваться в ретросинтетическом анализе для планирования органического синтеза .
Функциональная группа — это группа атомов в молекуле с отличительными химическими свойствами , независимо от других атомов в молекуле. Атомы в функциональной группе связаны друг с другом и с остальной частью молекулы ковалентными связями . Для повторяющихся звеньев полимеров функциональные группы присоединяются к их неполярному ядру атомов углерода и, таким образом, добавляют химический характер углеродным цепям. Функциональные группы также могут быть заряжены , например, в карбоксилатных солях ( −COO− ), что превращает молекулу в многоатомный ион или сложный ион . Функциональные группы, связывающиеся с центральным атомом в координационном комплексе, называются лигандами . Комплексообразование и сольватация также вызываются специфическими взаимодействиями функциональных групп. Согласно общему правилу «подобное растворяется в подобном», именно общие или взаимно хорошо взаимодействующие функциональные группы обуславливают растворимость . Например, сахар растворяется в воде, потому что оба имеют общую гидроксильную функциональную группу ( −OH ), а гидроксилы сильно взаимодействуют друг с другом. Кроме того, когда функциональные группы более электроотрицательны , чем атомы, к которым они присоединены, функциональные группы становятся полярными, а неполярные молекулы, содержащие эти функциональные группы, становятся полярными и, таким образом, растворимыми в некоторой водной среде.
Объединение названий функциональных групп с названиями исходных алканов создает то, что называется систематической номенклатурой для наименования органических соединений . В традиционной номенклатуре первый атом углерода после углерода, который присоединяется к функциональной группе, называется альфа-углеродом ; второй - бета-углеродом, третий - гамма-углеродом и т. д. Если у углерода есть другая функциональная группа, она может быть названа греческой буквой, например, гамма-амин в гамма-аминомасляной кислоте находится на третьем углероде углеродной цепи, присоединенной к группе карбоксильной кислоты. Соглашения ИЮПАК требуют числовой маркировки позиции, например, 4-аминобутановая кислота. В традиционных названиях используются различные квалификаторы для обозначения изомеров , например, изопропанол (название ИЮПАК: пропан-2-ол) является изомером н-пропанола (пропан-1-ол). Термин фрагмент имеет некоторое совпадение с термином «функциональная группа». Однако фрагмент представляет собой целую «половину» молекулы, которая может быть не только одной функциональной группой, но и более крупной единицей, состоящей из нескольких функциональных групп. Например, «арильный фрагмент» может быть любой группой, содержащей ароматическое кольцо , независимо от того, сколько функциональных групп имеет указанный арил.
Ниже приведен список общих функциональных групп. [3] В формулах символы R и R' обычно обозначают присоединенный водород или углеводородную боковую цепь любой длины, но иногда могут относиться к любой группе атомов.
Углеводороды — это класс молекул, определяемый функциональными группами, называемыми гидрокарбилами, которые содержат только углерод и водород, но различаются по количеству и порядку двойных связей. Каждый из них отличается по типу (и масштабу) реакционной способности.
Существует также большое количество разветвленных или кольцевых алканов, которые имеют особые названия, например, трет-бутил , борнил , циклогексил и т. д. Существует несколько функциональных групп, которые содержат алкен, например, винильная группа , аллильная группа или акриловая группа . Углеводороды могут образовывать заряженные структуры: положительно заряженные карбокатионы или отрицательные карбанионы . Карбокатионы часто называют -um . Примерами являются тропилий и трифенилметильные катионы, а также циклопентадиенильный анион.
Галогеналканы — это класс молекул, определяемых связью углерод- галоген . Эта связь может быть относительно слабой (в случае иодоалкана) или довольно стабильной (как в случае фторалкана). В целом, за исключением фторированных соединений, галогеналканы легко подвергаются реакциям нуклеофильного замещения или реакциям элиминирования . Замещение на углероде, кислотность соседнего протона, условия растворителя и т. д. — все это может влиять на результат реакции.
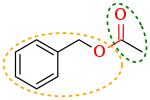
Соединения, содержащие связи CO, обладают различной реакционной способностью в зависимости от расположения и гибридизации связи CO из-за электроноакцепторного эффекта sp-гибридизованного кислорода (карбонильных групп) и донорного эффекта sp 2 -гибридизованного кислорода (спиртовых групп).
Соединения, содержащие азот в этой категории, могут содержать связи CO, как, например, в случае амидов .
Соединения, содержащие серу, демонстрируют уникальную химию из-за способности серы образовывать больше связей, чем кислород, ее более легкий аналог в периодической таблице. Заместительная номенклатура (отмечена как префикс в таблице) предпочтительнее функциональной номенклатуры класса (отмечена как суффикс в таблице) для сульфидов, дисульфидов, сульфоксидов и сульфонов.
Соединения, содержащие фосфор, демонстрируют уникальную химию, обусловленную способностью фосфора образовывать больше связей, чем азот, его более легкий аналог в периодической таблице.
Соединения, содержащие бор, демонстрируют уникальную химию, поскольку они имеют частично заполненные октеты и поэтому действуют как кислоты Льюиса .
примечание 1 Фтор слишком электроотрицателен, чтобы связываться с магнием; вместо этого он становится ионной солью .
Эти названия используются для обозначения самих фрагментов или радикальных видов, а также для образования названий галогенидов и заместителей в более крупных молекулах.
Если исходный углеводород ненасыщен, суффикс («-ил», «-илиден» или «-илидин») заменяет «-ан» (например, «этан» становится «этил»); в противном случае суффикс заменяет только конечный «-е» (например, « этин » становится « этинил »). [4]
При использовании для обозначения фрагментов, множественные одинарные связи отличаются от одинарной кратной связи. Например, метиленовый мостик (метандиил) имеет две одинарные связи, тогда как метилиденовая группа (метилиден) имеет одну двойную связь. Суффиксы могут быть объединены, как в метилидин (тройная связь) против метилилидена (одинарная связь и двойная связь) против метантриила (три двойные связи).
Некоторые названия сохранились, например, метилен для метандиила, 1,x- фенилен для фенил-1,x-диила (где x равно 2, 3 или 4), [5] карбин для метилидина и тритил для трифенилметила.