Хлорид железа(II) , также известный как хлорид железа , представляет собой химическое соединение формулы FeCl 2 . Это парамагнитное твердое вещество с высокой температурой плавления. Соединение белого цвета, но типичные образцы часто имеют не совсем белый цвет. FeCl 2 кристаллизуется из воды в виде зеленоватого тетрагидрата , формы, которая чаще всего встречается в торговле и лабораториях. Еще есть дигидрат. Соединение хорошо растворяется в воде, образуя бледно-зеленые растворы.

Гидратные формы хлорного железа образуются при обработке отходов сталеплавильного производства соляной кислотой . Такие растворы называются «отработанной кислотой» или «рассолом», особенно если соляная кислота израсходована не полностью:
Производство хлорного железа предполагает использование хлорного железа. Хлорид железа также является побочным продуктом производства титана, поскольку некоторые титановые руды содержат железо. [3]
Хлорид железа получают добавлением порошка железа к раствору соляной кислоты в метаноле. В результате этой реакции образуется метанольный сольват дихлорида, который при нагревании в вакууме при температуре около 160°С превращается в безводный FeCl 2 . [4] Показана чистая реакция:
FeBr 2 и FeI 2 можно получить аналогично.
Альтернативным синтезом безводного хлорида железа является восстановление FeCl 3 хлорбензолом : [5]
Для получения ферроцена хлорид железа получают in situ путем сопропорционирования FeCl 3 с порошком железа в тетрагидрофуране (ТГФ). [6] Хлорид железа разлагается до хлорида железа при высоких температурах.
Дигидрат FeCl 2 (H 2 O) 2 кристаллизуется из концентрированной соляной кислоты. [7] Дигидрат представляет собой координационный полимер . Каждый центр Fe координирован с четырьмя двумостиковыми хлоридными лигандами . Октаэдр завершается парой взаимно транс -аво-лигандов . [8]

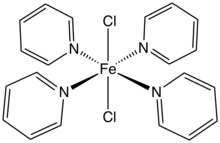
FeCl 2 и его гидраты образуют комплексы со многими лигандами. Например, растворы гидратов реагируют с двумя молярными эквивалентами [(C 2 H 5 ) 4 N]Cl с образованием соли [(C 2 H 5 ) 4 N] 2 [FeCl 4 ]. [10]
Безводный FeCl 2 , растворимый в ТГФ, [2] является стандартным предшественником в металлоорганическом синтезе. FeCl 2 используется для образования комплексов NHC in situ для реакций кросс-сочетания . [11]
В отличие от родственных сульфата железа и хлорида железа , хлорид железа имеет мало коммерческого применения. Помимо использования в лабораторном синтезе комплексов железа, хлорид железа служит коагулянтом и флокулянтом при очистке сточных вод , особенно отходов, содержащих хромат или сульфиды . [12] Используется для контроля запаха при очистке сточных вод. Он используется в качестве прекурсора для изготовления различных сортов гематита, которые можно использовать в различных пигментах. Это предшественник гидратированных оксидов железа (III), которые являются магнитными пигментами. [3] FeCl 2 находит применение в качестве реагента в органическом синтезе . [13]
Лоуренцит, (Fe,Ni)Cl 2 , является природным аналогом и типичным (хотя и редко встречающимся) метеоритным минералом. [14] Природной формой дигидрата является рокюнит — очень редкий минерал. [15] Родственными, но более сложными (в частности, основными или гидратированными) минералами являются гиббингит , дрониноит и кулигинит.
{{cite book}}: |journal=игнорируется ( помощь ){{cite book}}: |journal=игнорируется ( помощь ){{cite book}}: |journal=игнорируется ( помощь ){{cite book}}: |journal=игнорируется ( помощь )