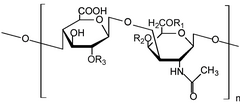
Хондроитинсульфат представляет собой сульфатированный гликозаминогликан (ГАГ) [1] , состоящий из цепочки чередующихся сахаров ( N-ацетилгалактозамин и глюкуроновая кислота ). Обычно он присоединяется к белкам как часть протеогликана . [1] Цепь хондроитина может содержать более 100 отдельных сахаров, каждый из которых может быть сульфатирован в различных положениях и количествах. Хондроитинсульфат является важным структурным компонентом хряща [2] и обеспечивает большую часть его устойчивости к сжатию . [3] Наряду с глюкозамином , хондроитинсульфат стал широко используемой пищевой добавкой для лечения остеоартрита , хотя крупные клинические испытания не смогли продемонстрировать какую-либо симптоматическую пользу хондроитина.
Хондроитин используется в пищевых добавках в качестве альтернативного лекарства для лечения остеоартрита . [4] Он также одобрен и регулируется как симптоматический препарат медленного действия для лечения этого заболевания (SYSADOA) в Европе и некоторых других странах. Обычно он продается вместе с глюкозамином . [5] Кокрейновский обзор клинических испытаний 2015 года показал, что большинство из них были низкого качества, но были некоторые доказательства кратковременного облегчения боли и небольшого количества побочных эффектов; похоже, что он не улучшает и не поддерживает здоровье пораженных суставов . [5]
Хондроитин, наряду с широко используемым глюкозамином, не следует использовать для лечения людей с симптоматическим остеоартритом коленного сустава, поскольку данные показывают, что эти методы лечения не могут облегчить это состояние. [6]
Хондроитин оказался многообещающим в лечении ишемической болезни сердца . В 6-летнем двойном слепом плацебо-контролируемом исследовании с участием 60 испытуемых, опубликованном в 1973 году, группа, принимавшая хондроитинсульфат, показала на 350% снижение числа смертельных сердечных приступов по сравнению с контрольной группой. При анализе данных о несмертельных сердечно-сосудистых событиях в контрольной группе несмертельные сердечные приступы наблюдались с частотой 16%, а в группе, получавшей хондроитинсульфат, - с 0%. [7]
Клинические исследования не выявили каких-либо существенных побочных эффектов или передозировок хондроитинсульфата, что позволяет предположить его долгосрочную безопасность. [8] В 2003 году рабочая группа комитета Европейской лиги борьбы с ревматизмом (EULAR) оценила уровень токсичности хондроитинсульфата 6 по шкале от 0 до 100. [9]
Хондроитинсульфат не метаболизируется цитохромом Р450 . [10]
Эффект хондроитинсульфата у людей с остеоартритом, вероятно, является результатом ряда реакций, включая его противовоспалительную активность, стимуляцию синтеза протеогликанов и гиалуроновой кислоты, а также снижение катаболической активности хондроцитов, ингибирование синтеза протеолитических ферменты , оксид азота и другие вещества, которые способствуют повреждению хрящевого матрикса и вызывают гибель суставных хондроцитов. В недавнем обзоре обобщены данные соответствующих отчетов, описывающих биохимические основы действия хондроитинсульфата на суставные ткани при остеоартрозе. [11]
Фармакокинетические исследования, проведенные на людях и экспериментальных животных после перорального введения хондроитинсульфата, показали, что он может всасываться перорально. Хондроитинсульфат демонстрирует кинетику первого порядка вплоть до однократных доз 3000 мг. [12] [13] [14] [15] Многократные дозы 800 мг у людей с остеоартритом не изменяют кинетику хондроитинсульфата. Биодоступность хондроитинсульфата колеблется от 15% до 24% от перорально принимаемой дозы . В частности, в отношении суставной ткани Ronca et al. [16] сообщили, что хондроитинсульфат не быстро всасывается в желудочно-кишечном тракте, а высокое содержание меченого хондроитинсульфата обнаруживается в синовиальной жидкости и хрящах.
Цепи хондроитинсульфата представляют собой неразветвленные полисахариды переменной длины, содержащие два чередующихся моносахарида: D -глюкуроновую кислоту (GlcA) и N -ацетил- D -галактозамин (GalNAc). Некоторые из этих остатков GlcA могут быть эпимеризованы в L -идуроновую кислоту (IdoA), после чего образующийся гликозаминогликан затем называют дерматансульфатом , ранее называвшимся хондроитинсульфатом B.
Хондроитинсульфат получают из натуральных продуктов с высокой вариабельностью длины цепи и характера сульфатации. Вариабельность состава хондроитинсульфата распространяется на его происхождение, что позволяет дифференцировать хондроитинсульфат из наземных и морских источников. Один из способов взглянуть на эту разницу - с точки зрения доли дисахаридных единиц: хондроитинсульфат у наземных животных почти исключительно состоит из несульфатированных (О) и моносульфатированных (А и С) единиц, в то время как у морских видов доля дисульфатированных (D, E и B) единиц выше. Кроме того, цепи морского хондроитинсульфата, как правило, длиннее, с молекулярной массой до 70 кДа в хондроитинсульфате акулы, тогда как у наземных животных молекулярная масса обычно ниже 45 кДа. [17] [18]
Цепи хондроитинсульфата связаны с гидроксильными группами сериновых остатков некоторых белков. Как именно отбираются белки для прикрепления гликозаминогликанов, неясно. За гликозилированными серинами часто следует глицин и они имеют соседние кислотные остатки, но этот мотив не всегда предсказывает гликозилирование.
Прикрепление цепи ГАГ начинается с четырех моносахаридов по фиксированной схеме: Ксил – Гал – Гал – GlcA. Каждый сахар связывается с помощью определенного фермента, что позволяет контролировать синтез ГАГ на нескольких уровнях. Ксилоза начинает прикрепляться к белкам в эндоплазматическом ретикулуме , а остальные сахара прикрепляются в аппарате Гольджи . [19]
Хондроитинсульфат хорошо растворим в воде . [20]
Хондроитинсульфат был первоначально выделен задолго до того, как была охарактеризована его структура, что со временем привело к изменениям в терминологии. [21] Ранние исследователи обозначали различные фракции вещества буквами.
«Хондроитинсульфат B» — старое название дерматансульфата , и он больше не классифицируется как форма хондроитинсульфата. [22]
Хондроитин без «сульфата» использовался для описания фракции с небольшим сульфатированием или без него. [23] Однако это различие используется не всеми.
Хотя название «хондроитинсульфат» предполагает соль с сульфатным противоанионом , это не так, поскольку сульфат ковалентно связан с сахаром. Скорее, поскольку молекула имеет несколько отрицательных зарядов при физиологическом pH, в солях сульфата хондроитина присутствует катион . Коммерческие препараты хондроитинсульфата обычно представляют собой натриевую соль. Барнхилл и др. предложили называть все такие препараты хондроитинсульфата «хондроитином натрия» независимо от их сульфатационного статуса. [24]
В 2008 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) определило «сверхсульфатированный сульфат хондроитина» как примесь в гепарине , происходящем из Китая . [25] [26] [27]
В 2004 году в FDA было подано ходатайство о том, чтобы пищевая добавка хондроитинсульфата была отмечена как снижающая риск остеоартрита, ухудшения состояния хряща и связанных с остеоартритом болей в суставах, болезненности и отека. FDA отклонило запрос, заявив, что эксперименты, проведенные компанией, недостаточно продемонстрировали эффективность заявления. Среди других комментариев FDA отметило плохой экспериментальный дизайн некоторых исследований. [28]
В 2007 году Райхенбах и др. использовали явные методы для проведения и составления систематического обзора 20 исследований и пришли к выводу, что «крупномасштабные, методологически обоснованные исследования показывают, что симптоматическая польза от хондроитина минимальна или отсутствует. Поэтому использование хондроитина в рутинной клинической практике не рекомендуется». Напротив, а также в 2007 г. Bruyere et al. пришли к выводу, что «есть убедительные доказательства того, что сульфат глюкозамина и хондроитинсульфат могут препятствовать прогрессированию ОА».
По состоянию на 2015 год крупнейшим исследованием, проведенным с продуктом, было исследование по вмешательству при артрите с глюкозамином и хондроитином (GAIT), двойное слепое рандомизированное многоцентровое клиническое исследование, спонсируемое Национальными институтами здравоохранения США, с участием 1583 человек с остеоартритом коленного сустава, которое было опубликовано. в Медицинском журнале Новой Англии в 2006 году. [5] [29] Субъекты были случайным образом распределены на одну из пяти пероральных форм лечения: две капсулы гидрохлорида глюкозамина по 250 мг три раза в день, две капсулы хондроитинсульфата по 200 мг три раза в день, две капсулы по 250 мг глюкозамина гидрохлорида плюс 200 мг хондроитинсульфата три раза в день, 200 мг целекоксиба в день или плацебо. Лечение проводилось в течение 24 недель. Это не показало никакой разницы с плацебо. [5]
Савицке А и др. В 2010 г. оценивалась эффективность и безопасность глюкозамина и хондроитинсульфата, отдельно или в комбинации, а также целекоксиба и плацебо при болезненном остеоартрите коленного сустава в течение 2 лет в качестве продолжения исследования GAIT. Это было 24-месячное двойное слепое плацебо-контролируемое исследование, в котором приняли участие 662 человека с остеоартритом коленного сустава, которые соответствовали рентгенологическим критериям (изменения 2 или 3 степени по Келлгрену/Лоуренсу и исходная ширина суставной щели не менее 2 мм). Эта подгруппа продолжала получать рандомизированное лечение (глюкозамин 500 мг три раза в день, хондроитинсульфат 400 мг три раза в день, комбинация глюкозамина и хондроитинсульфата, целекоксиб 200 мг в день или плацебо) в течение 24 месяцев. Первичным результатом было снижение боли на 20% в течение 24 месяцев по данным Индекса остеоартрита Университета Западного Онтарио и Макмастера (WOMAC). Вторичные результаты включали реакцию Международного общества исследований ревматологии/остеоартрита и изменение по сравнению с исходным уровнем боли и функции WOMAC. [5] [30] За 2 года ни один из методов лечения (даже целекоксиб с положительным контролем) не достиг клинически значимого различия в боли или функции WOMAC по сравнению с плацебо. Побочные реакции были одинаковыми в группах лечения, а серьезные нежелательные явления были редки для всех видов лечения. [30]
Исследование 2021 года показало значительное (около 40%) снижение риска острого инфаркта миокарда у нынешних пользователей хондроитинсульфата в подгруппах сердечно-сосудистого риска высокого риска. [31]
Большая часть хондроитина, по-видимому, производится из экстрактов хрящевых тканей коров и свиней (коровьей трахеи , свиного уха и носа), но также используются и другие источники, такие как хрящи акул , рыб и птиц. Поскольку хондроитин не является однородным веществом и в природе присутствует в самых разных формах, точный состав каждой добавки будет различаться. [24] Фактически, хотя многие компании, производящие пищевые добавки , производят свою продукцию в соответствии с Надлежащей производственной практикой (GMP) при переработке пищевых продуктов , большинство из них не производят свою продукцию в соответствии с правилами GMP для фармацевтических препаратов, в результате чего продукция не соответствует фармацевтическим требованиям. требования. [32]
Хотя хондроитин продается по рецепту или без рецепта в 22 странах, в США он регулируется Управлением по контролю за продуктами и лекарствами США в качестве пищевой добавки [ 33 ] . В Европе препараты хондроитинсульфата одобрены как препараты с доказанной эффективностью и безопасностью, продемонстрированными клиническими испытаниями на людях с остеоартритом. [34] Адебовале и др. сообщили в 2000 году, что из 32 добавок хондроитина, которые они проанализировали, только 5 были маркированы правильно, и более половины содержали менее 40% указанного количества. [35] С введением правил GMP для пищевых добавок в 2008 году препараты хондроитинсульфата в США подлежат обязательным стандартам маркировки, а также требованиям к тестированию на идентичность, чистоту, прочность и состав. [ нужна ссылка ] Стандарты тестирования Фармакопеи США (USP) для идентификации и количественного определения хондроитина хорошо известны. [ нужна цитата ]
Не существует правил FDA в отношении хондроитинсульфата в качестве пищевой добавки, поскольку он признан FDA компонентом пищевых продуктов и «в целом признан безопасным». [28] Однако предложенное применение пищевой добавки хондроитинсульфата в качестве средства предотвращения дегенерации суставов было тщательно изучено FDA, которое заявило:
«Для обычных пищевых продуктов эта оценка включает рассмотрение того, является ли ингредиент, являющийся источником вещества, общепризнанным безопасным (GRAS), одобренным в качестве пищевой добавки или разрешенным предварительной санкцией, выданной FDA (см. 21 CFR 101.70(f) Однако на пищевые ингредиенты в пищевых добавках не распространяются положения Закона о пищевых добавках (см. раздел 201(s)(6) Закона (21 USC § 321(s)(6)). на них распространяются положения о фальсификации в разделе 402 Закона (21 USC 342) и, если применимо, новые положения о пищевых ингредиентах в разделе 413 Закона (21 USC 350b), которые относятся к диетическим ингредиентам, которые не продавались в США. США до 15 октября 1994 года».
— Письмо о связи между потреблением глюкозамина и/или хондроитинсульфата и снижением риска: остеоартрита; Боль в суставах, связанная с остеоартритом, болезненность и отек суставов; Дегенерация суставов; и разрушение хряща
В том же письме FDA обнаружило, что исследования, проведенные с пищевой добавкой хондроитинсульфата, были недостаточными для обоснования утверждений о том, что она эффективна в предотвращении ухудшения состояния суставов, и отклонило просьбу о разрешении маркировать добавку как таковую. Они также отклонили просьбу продавать его как безопасную, учитывая, что клинических испытаний на людях не проводилось, сославшись на то, что исследований на животных недостаточно для одобрения пищевой добавки. [28]
Хондроитин и глюкозамин также используются в ветеринарии при остеоартрите. [36] [37] [38]
{{cite journal}}: CS1 maint: числовые имена: список авторов ( ссылка ){{cite journal}}: CS1 maint: числовые имена: список авторов ( ссылка )