Хроматные соли содержат хромат-анион CrO .2−
4. Дихроматные соли содержат дихромат-анион Cr .
2О2−
7. Они представляют собой оксианионы хрома в степени окисления +6 и являются умеренно сильными окислителями . В водном растворе ионы хромата и дихромата могут быть взаимопревращаемыми.
Хроматы реагируют с перекисью водорода , образуя продукты , в которых перекись O2−
2, заменяет один или несколько атомов кислорода. В кислом растворе образуется нестабильный синий пероксокомплекс пероксида хрома(VI) CrO(O 2 ) 2 ; это незаряженная ковалентная молекула, которую можно экстрагировать эфиром . Добавление пиридина приводит к образованию более устойчивого комплекса CrO(O 2 ) 2 py. [1]
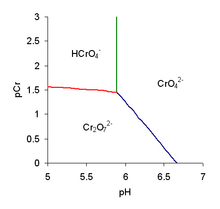
В водном растворе хромат- и дихромат-анионы находятся в химическом равновесии .
Диаграмма преобладания показывает, что положение равновесия зависит как от pH , так и от аналитической концентрации хрома. [примечания 1] Ион хромата является преобладающим ионом в щелочных растворах, но дихромат может стать преобладающим ионом в кислых растворах.
Дальнейшие реакции конденсации могут протекать в сильнокислом растворе с образованием трихроматов Cr
3О2−
10, и тетрахроматы , Cr
4О2−
13. [2] Все полиоксианионы хрома(VI) имеют структуру, состоящую из тетраэдрических звеньев CrO 4 , имеющих общие углы. [3]
Ион хромата водорода HcrO 4 − является слабой кислотой :
Он также находится в равновесии с дихромат-ионом:
Это равновесие не связано с изменением концентрации ионов водорода, что предполагает независимость равновесия от pH. Красная линия на диаграмме доминирования не совсем горизонтальна из-за одновременного равновесия с хромат-ионом. Ион хромата водорода может быть протонирован с образованием молекулярной хромовой кислоты H 2 CrO 4 , но p K a для равновесия
не очень хорошо охарактеризован. Зарегистрированные значения варьируются от -0,8 до 1,6. [4]
Дихромат-ион является несколько более слабым основанием, чем хромат-ион: [5]
Значение p K для этой реакции показывает, что ею можно пренебречь при pH > 4.
Хромат- и дихромат-ионы являются довольно сильными окислителями . Обычно к атому хрома присоединяются три электрона, восстанавливая его до степени окисления +3. В кислом растворе образуется водный ион Cr 3+ .
В щелочном растворе образуется гидроксид хрома(III). Окислительно -восстановительный потенциал показывает, что хроматы являются более слабым окислителем в щелочном растворе, чем в кислом растворе. [6]

В 1985 году было произведено около 136 000 тонн (150 000 тонн) шестивалентного хрома , в основном бихромата натрия. [8] Хроматы и дихроматы используются при хромировании для защиты металлов от коррозии и улучшения адгезии краски. Хроматы и дихроматы тяжелых металлов , лантаноидов и щелочноземельных металлов очень мало растворимы в воде и поэтому используются в качестве пигментов. Содержащий свинец пигмент хром-желтый использовался в течение очень долгого времени, прежде чем экологические нормы запретили его использование. [7] При использовании в качестве окислителей или титрантов в окислительно-восстановительной химической реакции хроматы и дихроматы превращаются в трехвалентный хром Cr 3+ , соли которого обычно имеют совершенно другой сине-зеленый цвет. [8]

Первичная хромовая руда представляет собой смешанный оксидный хромит металлов FeCr 2 O 4 , встречающийся в виде хрупких металлических черных кристаллов или гранул. Хромитовую руду нагревают смесью карбоната кальция и карбоната натрия в присутствии воздуха. Хром окисляется до шестивалентной формы, а железо образует оксид железа(III) Fe 2 O 3 :
Последующее выщелачивание этого материала при более высоких температурах растворяет хроматы, оставляя остаток нерастворимого оксида железа. Обычно раствор хромата подвергают дальнейшей обработке для получения металлического хрома, но соль хромата можно получить непосредственно из щелока. [9]
Хроматсодержащие минералы встречаются редко. Крокоит PbCrO 4 , который может встречаться в виде впечатляющих длинных красных кристаллов, является наиболее часто встречающимся хроматным минералом. Редкие минералы хромата калия и родственные ему соединения встречаются в пустыне Атакама . Среди них лопезит – единственный известный бихроматный минерал. [10]
Соединения шестивалентного хрома могут быть токсичными и канцерогенными ( группа 1 IARC ). Вдыхание частиц соединений шестивалентного хрома может вызвать рак легких . Также наблюдалась положительная связь между воздействием соединений хрома (VI) и раком носа и носовых пазух . [11] Использование хроматных соединений в промышленных товарах ограничено в ЕС (и в силу общности рынка в остальном мире) директивой Парламента ЕС об ограничении использования опасных веществ (RoHS) (2002/95/EC) .
Имеется достаточно доказательств канцерогенности соединений хрома (VI) для человека . Соединения хрома (VI) вызывают рак легких. Также наблюдалась положительная связь между воздействием соединений хрома (VI) и раком носа и носовых пазух. Имеются достаточные доказательства канцерогенности соединений хрома (VI) на экспериментальных животных. Соединения хрома (VI) канцерогенны для человека (группа 1) .