
Хромофор — это молекула , которая поглощает свет на определенной длине волны и в результате отражает цвет . По этой причине хромофоры обычно называют цветными молекулами . Слово происходит от древнегреческого χρῶμᾰ (chroma) «цвет» и -φόρος (phoros) «носитель». Многие молекулы в природе являются хромофорами, включая хлорофилл , молекулу, отвечающую за зеленый цвет листьев . Цвет, который видят наши глаза, — это цвет света, не поглощенного отражающим объектом в пределах определенного спектра длин волн видимого света . Хромофор указывает область в молекуле, где разница энергий между двумя отдельными молекулярными орбиталями попадает в диапазон видимого спектра (или, в неформальном контексте, в рассматриваемый спектр). Таким образом, видимый свет, который попадает на хромофор, может быть поглощен путем возбуждения электрона из его основного состояния в возбужденное состояние . В биологических молекулах, которые служат для захвата или обнаружения световой энергии, хромофор — это фрагмент , который вызывает конформационное изменение молекулы при воздействии света.



Точно так же, как две соседние p-орбитали в молекуле образуют пи-связь , три или более соседних p-орбиталей в молекуле могут образовывать сопряженную пи-систему . В сопряженной пи-системе электроны способны захватывать определенные фотоны, когда электроны резонируют вдоль определенного расстояния p-орбиталей - подобно тому, как радиоантенна обнаруживает фотоны по своей длине. Как правило, чем более сопряженной (длинной) является пи-система, тем большую длину волны фотона можно захватить. Другими словами, с каждой добавленной соседней двойной связью, которую мы видим на диаграмме молекулы, мы можем предсказать, что система будет все более и более вероятно казаться желтой для наших глаз, поскольку она с меньшей вероятностью будет поглощать желтый свет и с большей вероятностью будет поглощать красный свет. («Сопряженные системы, содержащие менее восьми сопряженных двойных связей, поглощают только в ультрафиолетовой области и бесцветны для человеческого глаза», «Соединения синего или зеленого цвета обычно не зависят только от сопряженных двойных связей».) [3]
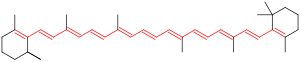
В сопряженных хромофорах электроны прыгают между энергетическими уровнями , которые являются расширенными пи-орбиталями , созданными электронными облаками, такими как в ароматических системах. Обычными примерами являются ретиналь (используется в глазу для обнаружения света), различные пищевые красители , красители для тканей ( азосоединения ), индикаторы pH , ликопин , β-каротин и антоцианы . Различные факторы в структуре хромофора влияют на то, в какой области спектра хромофор будет поглощать. Удлинение или расширение сопряженной системы с большим количеством ненасыщенных (множественных) связей в молекуле будет иметь тенденцию смещать поглощение в сторону более длинных волн. Правила Вудворда-Физера можно использовать для аппроксимации максимальной длины волны поглощения в ультрафиолетово -видимом диапазоне в органических соединениях с сопряженными системами пи-связей. [ необходима цитата ]
Некоторые из них являются хромофорами комплексов металлов, которые содержат металл в координационном комплексе с лигандами. Примерами являются хлорофилл , который используется растениями для фотосинтеза, и гемоглобин , переносчик кислорода в крови позвоночных животных. В этих двух примерах металл образует комплекс в центре тетрапиррольного макроциклического кольца : металлом является железо в гемовой группе (железо в порфириновом кольце) гемоглобина, или магний, образующий комплекс в хлориновом кольце в случае хлорофилла. Высокосопряженная система пи-связей макроциклического кольца поглощает видимый свет. Природа центрального металла также может влиять на спектр поглощения комплекса металл-макроцикл или такие свойства, как время жизни возбужденного состояния. [4] [5] [6] Тетрапиррольная часть в органических соединениях, которая не является макроциклической, но все еще имеет сопряженную систему пи-связей, все еще действует как хромофор. Примерами таких соединений являются билирубин и уробилин , которые имеют желтый цвет.
Ауксохром — это функциональная группа атомов , присоединенная к хромофору, которая изменяет способность хромофора поглощать свет, изменяя длину волны или интенсивность поглощения.
Галохромизм происходит, когда вещество меняет цвет при изменении pH . Это свойство индикаторов pH , молекулярная структура которых изменяется при определенных изменениях окружающего pH. Это изменение структуры влияет на хромофор в молекуле индикатора pH. Например, фенолфталеин является индикатором pH, структура которого изменяется при изменении pH, как показано в следующей таблице:
В диапазоне pH около 0-8 молекула имеет три ароматических кольца, все из которых связаны с тетраэдрическим sp 3 гибридизированным атомом углерода в середине, что не делает π-связь в ароматических кольцах сопряженной. Из-за своей ограниченной протяженности ароматические кольца поглощают свет только в ультрафиолетовой области, и поэтому соединение кажется бесцветным в диапазоне pH 0-8. Однако, когда pH увеличивается выше 8,2, этот центральный углерод становится частью двойной связи, становясь sp 2 гибридизированным и оставляя ap-орбиталь перекрываться с π-связью в кольцах. Это заставляет три кольца конъюгировать вместе, образуя расширенный хромофор, поглощающий более длинноволновой видимый свет, демонстрируя цвет фуксии. [7] В диапазонах pH за пределами 0-12 другие изменения молекулярной структуры приводят к другим изменениям цвета; см. подробности о фенолфталеине .