В органической химии циклоприсоединение — это химическая реакция , в которой «две или более ненасыщенные молекулы (или части одной и той же молекулы) соединяются с образованием циклического аддукта , в котором происходит чистое уменьшение кратности связи ». Получающаяся реакция представляет собой реакцию циклизации . Многие, но не все циклоприсоединения являются согласованными и, следовательно, перициклическими . [1] Несогласованные циклоприсоединения не являются перициклическими. [2] Как класс реакций присоединения , циклоприсоединения позволяют образовывать связи углерод-углерод без использования нуклеофила или электрофила .
Циклоприсоединения можно описать с помощью двух систем обозначений. Более старые, но все еще распространенные обозначения основаны на размере линейного расположения атомов в реагентах. Здесь используются круглые скобки : ( i + j + …) , где переменные — это количество линейных атомов в каждом реагенте. Продукт представляет собой цикл размера ( i + j + …) . В этой системе стандартная реакция Дильса-Альдера представляет собой (4+2)-циклоприсоединение, 1,3-диполярное циклоприсоединение представляет собой (3+2)-циклоприсоединение и циклопропанирование карбена с алкеном а(2+1) -циклоприсоединение. [1]
Более поздняя система обозначений, предпочитаемая ИЮПАК, впервые введенная Вудвордом и Хоффманном , использует квадратные скобки для обозначения количества электронов , а не атомов углерода, участвующих в образовании продукта. В обозначениях [ i + j + ...] стандартная реакция Дильса-Альдера представляет собой [4 + 2]-циклоприсоединение, тогда как 1,3-диполярное циклоприсоединение также является [4 + 2]-циклоприсоединением. [1]
Термические циклоприсоединения — это те циклоприсоединения, при которых реагенты находятся в основном электронном состоянии. Обычно они имеют (4 n + 2) π-электронов, участвующих в исходном материале, для некоторого целого числа n . Эти реакции в большинстве случаев происходят по причинам орбитальной симметрии в супрафациально -супрафациальной ( син / син- стереохимии). Сообщалось также об очень небольшом количестве примеров антарафациально -антарафациальных ( анти / антистереохимических ) реакций. Есть несколько примеров термического циклоприсоединения, которые имеют 4 n π-электрона (например, [2 + 2]-циклоприсоединение). Они протекают в супрафациально-антарафациальном смысле ( син / антистереохимия ), например, реакции циклоприсоединения производных кетена и аллена , в которых ортогональный набор р-орбиталей позволяет реакции протекать через скрещенное переходное состояние , хотя анализ этих реакции как [ π 2 s + π 2 a ] является спорным. Сообщалось также, что напряженные алкены, такие как производные транс -циклогептена, реагируют антарафациальным образом в реакциях [2 + 2]-циклоприсоединения.
Деринг (в личном сообщении Вудворду ) обнаружил, что гептафульвален и тетрацианоэтилен могут вступать в реакцию супрафациально-антарафациального [14+2]-циклоприсоединения. Этот результат позже был подтвержден и расширен Эрденом и Кауфманном, которые сообщили о супрафациально-антарафациальном циклоприсоединении гептафульвалена с N -фенилтриазолиндионом. [3]

Циклоприсоединения с участием 4n π-электронов могут происходить и за счет фотохимической активации. Здесь один компонент имеет электрон, перешедший из ВЗМО (π-связь) в НСМО (π* разрыхление ). Тогда орбитальная симметрия такова, что реакция может протекать супрафациально-супрафациально. Примером может служить реакция ДеМайо . Ниже показан еще один пример: фотохимическая димеризация коричной кислоты . [4] Два транс- алкена реагируют «голова к хвосту», а изолированные изомеры называются труксиловыми кислотами .
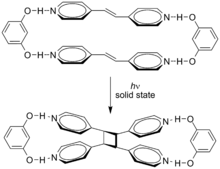
Супрамолекулярные эффекты могут влиять на эти циклоприсоединения. Циклоприсоединение транс -1,2-бис(4-пиридил)этена направляется резорцином в твердом состоянии с выходом 100% . [5]
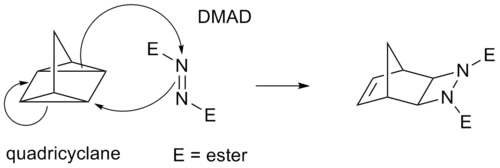
Некоторые циклоприсоединения вместо π-связей действуют через напряженные циклопропановые кольца, поскольку они имеют значительный π-характер. Например, аналогом реакции Дильса-Альдера является реакция квадрициклан - ДМАД :
В обозначениях циклоприсоединения (i+j+...) i и j относятся к числу атомов, участвующих в циклоприсоединении. В этих обозначениях реакция Дильса-Альдера представляет собой (4+2)циклоприсоединение, а 1,3-диполярное присоединение, такое как первая стадия озонолиза , представляет собой (3+2)циклоприсоединение. Однако предпочтительное обозначение ИЮПАК : [i+ j +...] учитывает электроны, а не атомы. В этих обозначениях и DA-реакция, и диполярная реакция становятся [4+2]-циклоприсоединением. Реакция между норборнадиеном и активированным алкином представляет собой [2+2+2]циклоприсоединение.
Реакция Дильса -Альдера , пожалуй, самая важная и часто изучаемая реакция циклоприсоединения. Формально это реакция [4+2] циклоприсоединения, которая существует в огромном диапазоне форм, включая обратную реакцию Дильса-Альдера с обратным электронным требованием , гексадегидро-реакцию Дильса-Альдера и связанную с ней тримеризацию алкинов . Реакцию также можно протекать в обратном порядке ( реакция ретро-Дильса-Альдера) .
Реакции с участием гетероатомов известны; включая реакции аза-Дильса-Альдера и Имина Дильса-Альдера .
Реакция циклоприсоединения Хейсгена представляет собой (2+3)циклоприсоединение.
Нитрон -олефиновое циклоприсоединение представляет собой (3+2)циклоприсоединение.
Хелетропные реакции представляют собой подкласс циклоприсоединения. Ключевой отличительной особенностью хелетропных реакций является то, что в одном из реагентов обе новые связи образуются с одним и тем же атомом. Классический пример — реакция диоксида серы с диеном .
Существуют и другие реакции циклоприсоединения: [4+3] циклоприсоединение , [6+4] циклоприсоединение , [2 + 2] фотоциклоприсоединение , металлоцентрированное циклоприсоединение и [4+4] фотоциклоприсоединение.
Циклоприсоединения часто имеют катализируемые металлами и ступенчатые радикальные аналоги, однако, строго говоря, это не перициклические реакции. Когда в циклоприсоединении участвуют заряженные или радикальные промежуточные соединения или когда результат циклоприсоединения получается в результате серии стадий реакции, их иногда называют формальными циклоприсоединениями , чтобы отличить их от истинных перициклических циклоприсоединений.
Одним из примеров формального [3+3]циклоприсоединения между циклическим еноном и енамином , катализируемого н -бутиллитием , является каскадная реакция Сторка енамин / 1,2-присоединение : [6]
![Межмолекулярное формальное [3+3] циклоприсоединение между циклическим хлоридом иминия и циклопентеноном.](http://upload.wikimedia.org/wikipedia/commons/thumb/5/53/3%2B3_cycloaddition_-_cyclic_iminium_to_cyclic_enone.svg/500px-3%2B3_cycloaddition_-_cyclic_iminium_to_cyclic_enone.svg.png)
Железо -дииминопиридиновые катализаторы содержат окислительно-восстановительный активный лиганд, в котором центральный атом железа может координировать свои действия с двумя простыми нефункционализированными двойными связями олефина. Катализатор можно записать как резонанс между структурой, содержащей неспаренные электроны с центральным атомом железа в степени окисления II, и структурой, в которой железо находится в степени окисления 0. Это дает ему возможность участвовать в связывании двойных связей, когда они подвергаются реакции циклизации, создавая циклобутановую структуру посредством восстановительного элиминирования CC; альтернативно циклобутеновая структура может быть получена путем отщепления бета-водорода. Эффективность реакции существенно варьируется в зависимости от используемых алкенов, но рациональный дизайн лигандов может позволить расширить диапазон катализируемых реакций. [7] [8]