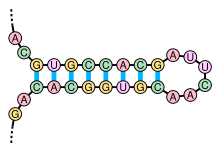
Стебель-петля — это вторичные структурные элементы нуклеиновой кислоты , которые образуются посредством внутримолекулярного спаривания оснований в одноцепочечной ДНК или РНК . Их также называют шпильками или шпильковыми петлями. Стебель-петля возникает, когда два участка одной и той же цепи нуклеиновой кислоты, обычно комплементарные по последовательности нуклеотидов , спариваются, образуя двойную спираль, которая заканчивается петлей неспаренных нуклеотидов.
Стебель-петли чаще всего встречаются в РНК и являются ключевым строительным блоком многих вторичных структур РНК . Стебель-петли могут направлять сворачивание РНК, защищать структурную стабильность для информационной РНК (мРНК), обеспечивать сайты распознавания для связывающих РНК белков и служить субстратом для ферментативных реакций . [1]
Образование стебля-петли зависит от стабильности областей спирали и петли. Первым предварительным условием является наличие последовательности, которая может складываться сама на себя, образуя парную двойную спираль. Стабильность этой спирали определяется ее длиной, количеством несовпадений или выпуклостей, которые она содержит (небольшое количество допустимо, особенно в длинной спирали), и составом оснований парной области. Спаривания между гуанином и цитозином имеют три водородные связи и более стабильны по сравнению с парами аденин - урацил , которые имеют только две. В РНК пары аденин-урацил с двумя водородными связями эквивалентны связи аденин- тимин в ДНК. Взаимодействия укладки оснований, которые выравнивают пи-связи ароматических колец оснований в благоприятной ориентации, также способствуют образованию спирали.
Стабильность петли также влияет на формирование структуры стебель-петля. Оптимальная длина петли, как правило, составляет около 4-8 оснований; петли, длина которых меньше трех оснований, стерически невозможны и, таким образом, не образуются, а большие петли без собственной вторичной структуры (например, спаривание псевдоузлов ) нестабильны. Одна общая петля с последовательностью UUCG известна как « тетрапетля», и она особенно стабильна из-за взаимодействий укладки оснований ее компонентов нуклеотидов. Поэтому такие петли могут образовываться в масштабе микросекундного времени. [2]
Стебель-петля встречается в структурах пре- микроРНК и наиболее известна в транспортной РНК , которая содержит три настоящих стебель-петли и один стебель, которые встречаются в виде клеверного листа. Антикодон, который распознает кодон в процессе трансляции , расположен на одной из непарных петель в тРНК. Две вложенные структуры стебель-петля встречаются в псевдоузлах РНК , где петля одной структуры образует часть второго стебля.
Многие рибозимы также имеют стебельно-петлевые структуры. Саморасщепляющийся молоткообразный рибозим содержит три стебельно-петлевых структуры, которые встречаются в центральной непарной области, где находится сайт расщепления. Основная вторичная структура молоткообразного рибозима необходима для активности саморасщепления.
Шпильковые петли часто являются элементами, которые можно обнаружить в 5'UTR прокариот. Эти структуры часто связаны с белками или вызывают ослабление транскрипта с целью регулирования трансляции. [3]
Структура мРНК «стебель-петля», образующаяся в месте связывания рибосомы, может контролировать начало трансляции . [4] [5]
Структуры стебля-петли также важны в прокариотической rho-независимой терминации транскрипции . Шпильковая петля образуется в цепи мРНК во время транскрипции и заставляет РНК-полимеразу диссоциировать от цепи ДНК-матрицы. Этот процесс известен как rho-независимая или внутренняя терминация, а вовлеченные последовательности называются терминаторными последовательностями.
{{cite journal}}: CS1 maint: multiple names: authors list (link)