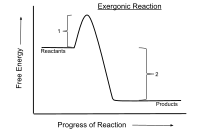
В химической термодинамике экзергоническая реакция — это химическая реакция , в которой изменение свободной энергии отрицательно (происходит чистое высвобождение свободной энергии). [1] Это указывает на самопроизвольную реакцию , если система закрыта и начальная и конечная температуры одинаковы. Для процессов, протекающих в закрытой системе при постоянном давлении и температуре, используется свободная энергия Гиббса , тогда как энергия Гельмгольца актуальна для процессов, протекающих при постоянном объеме и температуре. Согласно второму закону термодинамики, любая реакция, происходящая при постоянной температуре без подвода электрической или фотонной энергии, является экзергонической . Примером является клеточное дыхание .
Символически выделение свободной энергии , в экзергонической реакции (при постоянном давлении и температуре) обозначается как
Хотя говорят, что экзергонические реакции происходят спонтанно , это не означает, что реакция будет происходить с наблюдаемой скоростью . Например, диспропорционирование перекиси водорода высвобождает свободную энергию, но происходит очень медленно в отсутствие подходящего катализатора. Было высказано предположение, что в этом контексте термин «жадный» будет более интуитивным. [2]
В более общем смысле термины экзергонический и эндергонический относятся к изменению свободной энергии в любом процессе, а не только в химических реакциях. Напротив, термины экзотермический и эндотермический относятся к изменению энтальпии в закрытой системе во время процесса, обычно связанного с теплообменом .