
В термохимии экзотермическая реакция — это «реакция, для которой общее стандартное изменение энтальпии Δ H ⚬ отрицательно». [1] [2] Экзотермические реакции обычно выделяют тепло . Этот термин часто путают с экзергонической реакцией , которую ИЮПАК определяет как «... реакцию, для которой общее стандартное изменение энергии Гиббса Δ G ⚬ отрицательно». [2] Сильно экзотермическая реакция обычно также будет экзергонической, поскольку Δ H ⚬ вносит основной вклад в Δ G ⚬ . Большинство впечатляющих химических реакций, демонстрируемых в классах, являются экзотермическими и экзергоническими. Противоположной является эндотермическая реакция , которая обычно поглощает тепло и вызывается увеличением энтропии в системе.
Примеры многочисленны: горение , термитная реакция , соединение сильных кислот и оснований, полимеризация . Например, в повседневной жизни грелки для рук используют окисление железа для достижения экзотермической реакции:
Особенно важным классом экзотермических реакций является сжигание углеводородного топлива, например сжигание природного газа:
Реакции этих образцов сильно экзотермичны.
Неконтролируемые экзотермические реакции, приводящие к пожарам и взрывам, расточительны, поскольку трудно уловить высвободившуюся энергию. Природа осуществляет реакции горения в строго контролируемых условиях, избегая пожаров и взрывов, при аэробном дыхании , чтобы улавливать высвобождаемую энергию, например, для образования АТФ .
Энтальпия химической системы — это, по сути, ее энергия . Изменение энтальпии реакции Δ H равно теплу q , передаваемому из (или в) замкнутой системы при постоянном давлении без поступления или вывода электрической энергии. Выделение или поглощение тепла в химической реакции измеряется с помощью калориметрии , например, с помощью бомбового калориметра . Одним из распространенных лабораторных приборов является реакционный калориметр , с помощью которого контролируется тепловой поток из реакционного сосуда или в него. Выделение тепла и соответствующее изменение энергии Δ H реакции горения можно измерить особенно точно.
Измеренная тепловая энергия, выделяющаяся в экзотермической реакции, преобразуется в Δ H ⚬ в Джоулях на моль (ранее кал/моль ). Стандартное изменение энтальпии Δ H ⚬ по существу представляет собой изменение энтальпии, когда стехиометрические коэффициенты реакции рассматриваются как количества реагентов и продуктов (в молях) ; обычно начальная и конечная температура принимается равной 25 °C. Для газофазных реакций значения Δ H ⚬ связаны с энергиями связи с хорошим приближением следующим образом:
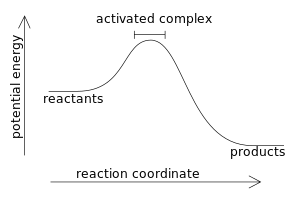
В экзотермической реакции по определению изменение энтальпии имеет отрицательное значение:
где большее значение (более высокая энергия реагентов) вычитается из меньшего значения (более низкая энергия продуктов). Например, при горении водорода: