
Вирус Escherichia T4 представляет собой разновидность бактериофагов , инфицирующих бактерии Escherichia coli . Это вирус с двухцепочечной ДНК подсемейства Tevenvirinae семейства Straboviridae . Т4 способен проходить только литический жизненный цикл , а не лизогенный жизненный цикл . Этот вид ранее назывался Т-четным бактериофагом , это название также включает, среди других штаммов (или изолятов), фаг энтеробактерий Т2 , фаг энтеробактерий Т4 и фаг энтеробактерий Т6 .
Начиная с 1940-х годов и по сей день, Т-четные фаги считаются наиболее изученными модельными организмами. Модельные организмы обычно должны быть простыми и содержать всего пять генов . Тем не менее, Т-четные фаги на самом деле являются одними из самых крупных и сложных вирусов , в которых генетическая информация этих фагов состоит примерно из 300 генов . В соответствии с их сложностью было обнаружено, что Т-четные вирусы имеют необычное основание гидроксиметилцитозин (HMC) вместо основания цитозина нуклеиновой кислоты . [4]
Геном двухцепочечной ДНК вируса Т4 имеет длину около 169 т.п.н. [5] и кодирует 289 белков . Геном Т4 окончательно избыточен . При репликации ДНК образуются конкатемеры длинной мультигеномной длины, возможно, по механизму репликации по катящемуся кругу. [6] При упаковке конкатемер разрезается на неспецифические позиции одинаковой длины, что приводит к образованию нескольких геномов, которые представляют собой круговые перестановки оригинала. [7] Геном Т4 несет эукариоподобные последовательности интронов .
Последовательность Шайна-Дальгарно GAGG доминирует в ранних генах вируса Т4, тогда как последовательность GGAG является мишенью для эндонуклеазы Т4 RegB, которая инициирует раннюю деградацию мРНК. [8]

Т4 — относительно крупный вирус, шириной примерно 90 нм и длиной 200 нм (длина большинства вирусов варьируется от 25 до 200 нм). Геном ДНК содержится в икосаэдрической головке, также известной как капсид . [9] Хвост Т4 полый, поэтому после прикрепления он может передавать свою нуклеиновую кислоту в клетку, которую заражает. Фаги Myoviridae, такие как T4, имеют сложные сократительные структуры хвоста с большим количеством белков, участвующих в сборке и функционировании хвоста. [10] Хвостовые волокна также важны для распознавания поверхностных рецепторов клетки-хозяина, поэтому они определяют, находится ли бактерия в пределах диапазона хозяина вируса. [11]
Недавно была описана структура базовой пластинки Т4 массой 6 мегадальтон, которая включает 127 полипептидных цепей 13 различных белков (генные продукты 5, 5.4, 6, 7, 8, 9, 10, 11, 12, 25, 27, 48 и 53). в атомарных деталях. Также создана атомная модель проксимальной области хвостовой трубки, образованной gp54 и белком основной трубки gp19. Белок рулетки gp29 присутствует в комплексах опорная пластинка-хвостовая трубка, но его невозможно смоделировать. [12]
При сборке вириона бактериофага (фага) Т4 морфогенетические белки, кодируемые фаговыми генами, взаимодействуют друг с другом в характерной последовательности. Поддержание соответствующего баланса в количествах каждого из этих белков, вырабатываемых во время вирусной инфекции, по-видимому, имеет решающее значение для нормального морфогенеза фага Т4. [13] Белки, кодируемые фагом Т4, которые определяют структуру вириона, включают основные структурные компоненты, второстепенные структурные компоненты и неструктурные белки, которые катализируют определенные этапы последовательности морфогенеза. [14] Морфогенез фага Т4 разделен на три независимых пути: головной, хвостовой и длинные хвостовые волокна, как подробно описано Япом и Россманом. [15]
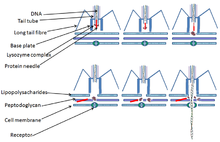
Вирус Т4 инициирует инфекцию Escherichia coli, связывая порины OmpC и липополисахарид (ЛПС) на поверхности клеток E. coli своими длинными хвостовыми волокнами (LTF). [16] [17] Сигнал распознавания передается через LTF на базовую плату. Это распутывает короткие хвостовые волокна (STF), которые необратимо связываются с поверхностью клеток E. coli . Опорная пластинка меняет конформацию, а хвостовая оболочка сжимается, в результате чего GP5 на конце хвостовой трубки прокалывает внешнюю мембрану клетки. [18] Лизоцимный домен GP5 активируется и разрушает периплазматический слой пептидогликана . Оставшаяся часть мембраны разрушается, и тогда ДНК из головки вируса может пройти через хвостовую трубку и попасть в клетку E. coli . [ нужна цитата ]
В 1952 году Херши и Чейз [19] предоставили ключевые доказательства того, что ДНК фага, в отличие от белка, проникает в бактериальную клетку-хозяина при инфекции и, таким образом, является генетическим материалом фага. Это открытие позволило предположить, что ДНК в целом является генетическим материалом различных организмов. [ нужна цитата ]
Литический жизненный цикл (от попадания в бактерию до ее уничтожения) занимает около 30 минут (при 37 °С). Вирулентные бактериофаги размножаются в бактериальном хозяине сразу после проникновения. После того, как количество дочерних фагов достигает определенного количества, они вызывают лизис или разрушение хозяина, поэтому они высвобождаются и заражают новые клетки-хозяева. [20] Процесс лизиса и высвобождения хозяина называется литическим циклом . Литический цикл — это цикл размножения вируса, который включает разрушение инфицированной клетки и ее мембраны. В этом цикле участвует вирус, который захватывает клетку-хозяина и ее механизм размножения. Следовательно , вирус должен пройти 5 стадий, чтобы размножиться и заразить клетку- хозяина :
После завершения жизненного цикла клетка-хозяин разрывается и выбрасывает вновь созданные вирусы в окружающую среду, разрушая клетку-хозяина. T4 имеет размер вспышки примерно 100-150 вирусных частиц на инфицированного хозяина. [ нужна цитата ]
Бензер (1955 – 1959) разработал систему изучения тонкой структуры гена с использованием мутантов бактериофага Т4, дефектных по генам rIIA и rIIB . [21] [22] [23] Используемые методы включали тесты комплементации и скрещивания для обнаружения рекомбинации , особенно между делеционными мутациями. Эти генетические эксперименты привели к обнаружению уникального линейного порядка мест мутаций внутри генов. Этот результат предоставил убедительные доказательства ключевой идеи о том, что ген имеет линейную структуру, эквивалентную длине ДНК, со многими сайтами, которые могут независимо мутировать. [ нужна цитата ]
Как и все другие вирусы, Т-четные фаги не прикрепляются к поверхности хозяина случайным образом; вместо этого они «ищут» и связываются с рецепторами , специфическими белковыми структурами, обнаруженными на поверхности хозяина. Эти рецепторы различаются в зависимости от фага; тейхоевая кислота , белки клеточной стенки и липополисахариды , жгутики и пили — все они могут служить рецепторами для связывания фага. Чтобы Т-четный фаг заразил своего хозяина и начал свой жизненный цикл, он должен начать первый процесс заражения — адсорбцию фага бактериальной клеткой. Адсорбция является величиной, характеризующей пару фаг-хозяин, и адсорбция фага на поверхности клетки-хозяина представлена как двухэтапный процесс: обратимый и необратимый. Он включает в себя структуру хвоста фага, которая начинается, когда волокна хвоста фага помогают связывать фаг с соответствующим рецептором его хозяина. Этот процесс обратим. Один или несколько компонентов базовой пластинки опосредуют необратимый процесс связывания фага с бактерией. [ нужна цитата ]
Проникновение также является ценной характеристикой заражения фагом-хозяином , которая включает инъекцию генетического материала фага внутрь бактерии . Проникновение нуклеиновой кислоты происходит после фазы необратимой адсорбции. Механизмы проникновения нуклеиновой кислоты фага специфичны для каждого фага. Этот механизм проникновения может включать электрохимический мембранный потенциал, молекулы АТФ , ферментативное расщепление слоя пептидогликана , или все три фактора могут иметь жизненно важное значение для проникновения нуклеиновой кислоты внутрь бактериальной клетки. Были проведены исследования механизма проникновения бактериофага Т2 (Т4-подобного фага), и они показали, что хвост фага не проникает внутрь клеточной стенки бактерии, а проникновение этого фага связано с электрохимическим мембранным потенциалом на внутренней мембране. [24] [25]
Геном вируса Т4 синтезируется внутри клетки-хозяина с использованием репликации по катящемуся кругу. [6] Время, необходимое для репликации ДНК в живой клетке, измерялось как скорость удлинения ДНК вируса Т4 в инфицированной вирусом E. coli. [26] В период экспоненциального роста ДНК при 37 °C скорость составляла 749 нуклеотидов в секунду. Частота мутаций на пару оснований за репликацию во время синтеза ДНК вируса Т4 составляет 1,7 на 10 -8 , [27] это высокоточный механизм копирования ДНК, допускающий только 1 ошибку на 300 копий. Вирус также кодирует уникальные механизмы восстановления ДНК . [28] Головка фага Т4 собирается пустой вокруг каркасного белка, который позже разрушается. Следовательно, ДНК должна войти в проголовку через крошечную пору, что достигается за счет того, что сначала с ДНК взаимодействует гексамер gp17, который также служит мотором и нуклеазой. Было обнаружено, что двигатель упаковки ДНК T4 загружает ДНК в капсиды вируса со скоростью до 2000 пар оснований в секунду. Задействованная мощность, если ее увеличить, будет эквивалентна мощности среднего автомобильного двигателя. [29]
Заключительный этап репродукции и размножения вируса определяется высвобождением вирионов из клетки-хозяина. Высвобождение вирионов происходит после разрыва бактериальной плазматической мембраны. Вирусы без оболочки лизуют клетку-хозяина, для которой характерны вирусные белки, атакующие пептидогликан или мембрану. Лизис бактерий происходит, когда капсиды внутри клетки выделяют фермент лизоцим, который разрушает клеточную стенку. Высвободившиеся бактериофаги заражают другие клетки, и цикл размножения вируса повторяется внутри этих клеток. [ нужна цитата ]

Реактивация множественности (MR) — это процесс, посредством которого два или более вирусных генома, каждый из которых содержит инактивирующие повреждения генома, могут взаимодействовать внутри инфицированной клетки с образованием жизнеспособного вирусного генома. Сальвадор Лурия , изучая УФ-облученный вирус Т4 в 1946 году, обнаружил MR и предположил, что наблюдаемая реактивация поврежденного вируса происходит по механизму рекомбинации. (см. ссылки [30] [31] [32] ). Это предшествовало подтверждению того, что ДНК генетический материал в 1952 году в родственном вирусе Т2 в результате эксперимента Херши-Чейза . [19]
Как вспоминал Лурия (1984, [33], стр. 97), открытие реактивации облученного вируса (называемой « реактивацией множественности ») немедленно положило начало бурной активности в изучении восстановления радиационных повреждений в группе ранних фагов ( обзор Бернштейна [28] в 1981 г.). Позже выяснилось, что обнаруженное Лурией восстановление поврежденного вируса путем взаимопомощи было лишь одним частным случаем восстановления ДНК. Теперь известно, что клетки всех типов, не только бактерии и их вирусы, но и все изученные организмы, включая человека, имеют сложные биохимические процессы восстановления повреждений ДНК (см. Репарация ДНК ). В настоящее время признано, что процессы восстановления ДНК играют решающую роль в защите от старения , рака и бесплодия . [ нужна цитата ]
MR обычно представляют в виде «кривых выживания», где выживаемость бляшкообразующей способности многократно инфицированных клеток (мультикомплексов) отображается в зависимости от дозы агента, повреждающего геном. Для сравнения также построен график выживаемости вирусной бляшкообразующей способности одиночно инфицированных клеток (монокомплексов) в зависимости от дозы агента, повреждающего геном. На верхнем рисунке показаны кривые выживаемости мультикомплексов и монокомплексов вируса Т4 при увеличении дозы УФ-излучения. Поскольку выживаемость представлена в логарифмическом масштабе, ясно, что выживаемость мультикомплексов превышает выживаемость монокомплексов в очень больших количествах (в зависимости от дозы). Кривая УФ-инактивации мультикомплексов имеет начальное плечо. Другими агентами, повреждающими ДНК вируса Т4, имеющими плечи на мультикомплексных кривых выживаемости, являются рентгеновские лучи [34] [35] и этилметансульфонат (ЭМС). [28] Наличие плеча было интерпретировано как означающее, что используются два рекомбинационных процесса. [36] Первый восстанавливает ДНК с высокой эффективностью («в «плечо»), но насыщается по мере увеличения повреждений; второй путь функционирует на всех уровнях повреждения. Выживший вирус Т4, высвободившийся из мультикомплексов, не демонстрирует увеличения мутаций , что указывает на то, что MR вируса, облученного УФ-излучением, является точным процессом. [36]
На нижнем рисунке показаны кривые выживаемости при инактивации вируса Т4 агентом, повреждающим ДНК, митомицином С (ММС). В этом случае кривая выживаемости мультикомплексов не имеет начального плеча, что позволяет предположить, что активен только второй описанный выше процесс рекомбинационной репарации. Об эффективности восстановления с помощью этого процесса свидетельствует то наблюдение, что доза ММС, обеспечивающая выживание только 1 из 1000 монокомплексов, обеспечивает выживание около 70% мультикомплексов. Аналогичные мультикомплексные кривые выживаемости (без плеч) были также получены для повреждающих ДНК агентов распада P32 , псоралена плюс ближнего УФ-облучения (ПУВА), N-метил-N'-нитро-N-нитрозогуанидина (МННГ), метилметансульфоната (ММС ). ) и азотистая кислота . [28]
Некоторые из генов, которые оказались необходимыми для MR в вирусе Т4, оказались ортологами генов, необходимых для рекомбинации у прокариот , эукариот и архей . К ним относится, например, ген Т4 uvsX [37] , который определяет белок, имеющий трехмерную структурную гомологию с RecA из Escherichia coli и гомологичным белком RAD51 у эукариот и RadA у архей . Было высказано предположение, что эффективная и точная рекомбинационная репарация повреждений ДНК при МР может быть аналогична процессу рекомбинационной репарации, происходящему во время мейоза у эукариот . [38]
Бактериофаги были впервые обнаружены английским ученым Фредериком Твортом в 1915 году и Феликсом д'Эрелем в 1917 году. В конце 1930-х годов Т. Л. Ракиетен предложил двум исследователям Милиславу либо смесь неочищенных сточных вод, либо лизат кишечной палочки , зараженной неочищенными сточными водами. Демерец и Уго Фано . Эти два исследователя выделили Т3, Т4, Т5 и Т6 из E.coli . Также в 1932 г. исследователь Дж. Бронфенбреннер изучал и работал над фагом Т2, при котором фаг Т2 был выделен из вируса. [39] Эта изоляция была сделана из фекального материала, а не из сточных вод. В любом случае Макс Дельбрюк участвовал в открытии Т-фагов. Его роль заключалась в том , чтобы разделить бактериофаги на Тип 1 (Т1), Тип 2 (Т2), Тип 3 (Т3) и т. д .
Точное время и место выделения вируса Т4 остается неясным, хотя, вероятно, они были обнаружены в сточных водах или фекалиях. Т4 и подобные вирусы были описаны в статье Томаса Ф. Андерсона , Макса Дельбрюка и Милислава Демерека в ноябре 1944 года. [40] В 1943 году Сальвадор Лурия и Дельбрюк показали, что бактериальные мутации устойчивости к фагам возникают в отсутствие отбора , а не в результате чем быть ответом на выбор. [33] Традиционное мнение среди бактериологов до 1943 года заключалось в том, что у бактерий нет ни хромосом, ни генов. Эксперимент Лурии-Дельбрюка показал, что бактерии, как и другие признанные модельные генетические организмы, имеют гены и что они могут спонтанно мутировать, создавая мутантов, которые затем могут размножаться, образуя клональные линии. В том же году они также начали работать с Альфредом Херши , еще одним экспериментатором с фагами. [41] (Эти трое разделят Нобелевскую премию по физиологии и медицине 1969 года «за работу над механизмом репликации и генетикой вирусов».)
Группа фагов представляла собой неформальную сеть биологов во главе с Максом Дельбрюком, которая проводила фундаментальные исследования в основном бактериофага Т4 и внесла большой плодотворный вклад в генетику микробов и истоки молекулярной биологии в середине 20-го века. В 1961 году Сидней Бреннер , один из первых членов группы фагов, сотрудничал с Фрэнсисом Криком , Лесли Барнеттом и Ричардом Уоттс-Тобином в Кавендишской лаборатории в Кембридже для проведения генетических экспериментов, которые продемонстрировали основную природу генетического кода белков. [42] Эти эксперименты, проведенные с мутантами гена rIIB фага Т4, показали, что для гена, кодирующего белок, три последовательных основания ДНК гена определяют каждую последующую аминокислоту белка. Таким образом, генетический код представляет собой триплетный код, где каждый триплет (называемый кодоном) определяет определенную аминокислоту. Они также получили доказательства того, что кодоны не перекрываются друг с другом в последовательности ДНК, кодирующей белок, и что такая последовательность считывается с фиксированной начальной точки. [ нужна цитата ]
В течение 1962–1964 годов исследователи фага Т4 предоставили возможность изучить функцию практически всех генов, необходимых для роста фага в лабораторных условиях. [43] [44] Этим исследованиям способствовало открытие двух классов условно летальных мутантов . Один класс таких мутантов известен как янтарные мутанты . [45] Другой класс условно-летальных мутантов называется термочувствительными мутантами. [46] Исследования этих двух классов мутантов привели к значительному пониманию многочисленных фундаментальных биологических проблем. Таким образом, было получено понимание функций и взаимодействий белков, участвующих в механизме репликации , репарации и рекомбинации ДНК , а также того, как вирусы собираются из белковых компонентов и компонентов нуклеиновых кислот (молекулярный морфогенез ). Кроме того, была выяснена роль терминирующих кодонов цепи . В одном примечательном исследовании использовались янтарные мутанты, дефектные по гену, кодирующему основной головной белок фага Т4. [47] Этот эксперимент предоставил убедительные доказательства широко распространенной, но до 1964 года все еще недоказанной «гипотезы последовательности», согласно которой аминокислотная последовательность белка определяется нуклеотидной последовательностью гена, определяющего белок. Таким образом, это исследование продемонстрировало коллинеарность гена с кодируемым им белком.
Ряд лауреатов Нобелевской премии работали с вирусом Т4 или Т4-подобными вирусами, в том числе Макс Дельбрюк , Сальвадор Лурия , Альфред Херши , Джеймс Д. Уотсон и Фрэнсис Крик . Среди других важных учёных, работавших с вирусом Т4, — Майкл Россманн , Сеймур Бензер , Брюс Альбертс , Гизела Мозиг , [48] Ричард Ленски и Джеймс Булл .
Caudovirales
>
Myoviridae
>
Tevenvirinae
>
T4virus
>
Escherichia Virus T4