Гидрид алюминия (также известный как алан и алюман ) представляет собой неорганическое соединение формулы Al H 3 . Алан и его производные являются частью семейства обычных восстановителей в органическом синтезе , основанных на гидридах группы 13 . [1] В растворе — обычно в эфирных растворителях, таких как тетрагидрофуран или диэтиловый эфир — гидрид алюминия образует комплексы с основаниями Льюиса и избирательно реагирует с определенными органическими функциональными группами (например, с карбоновыми кислотами и сложными эфирами по сравнению с органическими галогенидами и нитрогруппами ), и хотя это не предпочтительный реагент, он может реагировать с кратными углерод-углеродными связями (т.е. посредством гидроалюминирования ). Учитывая его плотность и содержание водорода порядка 10% по массе, [2] некоторые формы алана по состоянию на 2016 год являются [3] активными кандидатами для хранения водорода и, следовательно, для выработки электроэнергии в топливных элементах, включая электрические. транспортные средства. [ не проверено в теле ] В 2006 году было отмечено, что необходимы дальнейшие исследования для определения эффективного и экономичного способа обратить вспять процесс регенерации аланов из отработанного алюминиевого продукта.
Твердый гидрид алюминия, или алан, бесцветен и нелетуч, и в своей наиболее распространенной реагентной форме он представляет собой высокополимеризованную разновидность (т.е. содержит несколько самоассоциированных звеньев AlH 3 ); плавится с разложением при 110 °C. [4] Хотя алановые твердые вещества и растворы не являются самовозгорающимися, при их использовании необходимо соблюдать меры предосторожности, как и при использовании других легковоспламеняющихся гидридов металлов , и при обращении с ними и их хранении необходимо активно исключать попадание влаги. Алан разлагается на воздухе (в основном из-за примеси влаги), хотя пассивация — в данном случае позволяющая создать инертное поверхностное покрытие — значительно снижает скорость разложения препаратов аланов. [ не проверено в теле ]
Алан — бесцветное и нелетучее твердое вещество, плавящееся с разложением при 110 °C. [4] Однако твердая форма часто представляет собой белое твердое вещество, которое может иметь серый оттенок (при уменьшении размера частиц реагента или увеличении уровня примесей). [ нужна цитация ] Эта окраска возникает из-за тонкого поверхностного пассивационного слоя оксида или гидроксида алюминия. [ нужна цитата ]
В обычных лабораторных условиях алан структурно «высокополимерен». [4] Иногда это обозначается формулой (AlH 3 ) n , где n не указывается. [5] [ необходим неосновной источник ] Препараты алан растворяются в тетрагидрофуране (ТГФ) или диэтиловом эфире (эфире), [4] из которого выпадают чистые аллотропы. [6] [ нужен неосновной источник ]
Структурно алан может принимать многочисленные полиморфные формы . К 2006 году было известно «по меньшей мере 7 несольватированных фаз AlH 3 »: α-, α'-, β-, γ-, ε- и ζ-аланы; [2] впоследствии были открыты δ- и θ-аланы. [ нужна цитация ] Каждый из них имеет различную структуру, причем α-алан является наиболее термически стабильным полиморфом. [ нужна цитация ] Например, кристаллографически α-алан принимает кубическую или ромбоэдрическую морфологию, в то время как α’-алан образует игольчатые кристаллы, а γ-алан образует пучки сросшихся иголок. [ нужна цитата ] Кристаллическая структура α-алана была определена и включает атомы алюминия, окруженные шестью октаэдрически ориентированными атомами водорода, которые соединяются с шестью другими атомами алюминия (см. таблицу), где все расстояния Al-H эквивалентны (172 пм). ) и угол Al-H-Al составляет 141°. [7]
Когда β- и γ-аланы образуются совместно, они при нагревании превращаются в α-аланы, тогда как δ-, ε- и θ-аланы образуются в других условиях кристаллизации; полиморфы δ-, ε- и θ-аланов, хотя они менее термически стабильны, не превращаются в α-аланы при нагревании. [6] [ нужен лучший источник ]
В особых условиях можно получить и изучить неполимерные аланы (т.е. их молекулярные формы). Мономерный AlH 3 был выделен при низкой температуре в твердой матрице благородного газа , где было показано, что он является плоским. [ 9] Димерная форма Al 2 H 6 была выделена в твердом водороде и изоструктурна диборану ( B 2 H 6 ) и дигаллану ( Ga 2 H 6 ). [10] [11] [ нужен неосновной источник ]
Алан не является самовозгорающимся. [12] Несмотря на это, рекомендуется «такое же обращение и меры предосторожности, как... с Li[AlH 4 ] » (химический реагент, литий-алюминийгидрид ), поскольку его «реакционная способность [сравнима]» с этим родственным восстанавливающим реагентом. [4] Для этих реагентов как препараты в растворах, так и изолированные твердые вещества «легко воспламеняются и должны храниться в условиях отсутствия влаги». [13] Лабораторные руководства рекомендуют использовать аланы в вытяжном шкафу . [4] [ почему? ] С твердыми веществами этого типа реагентов рекомендуется обращаться «в перчаточном мешке или сухом боксе ». [13] После использования контейнеры с раствором обычно плотно запечатывают с одновременной промывкой инертным газом, чтобы исключить попадание кислорода и влаги из окружающего воздуха. [13]
Пассивация [ необходимо разъяснение ] значительно снижает скорость разложения, связанную с препаратами аланов. [ нужна ссылка ] Пассивированный аланы, тем не менее, сохраняет класс опасности 4.3 (химические вещества, которые при контакте с водой выделяют легковоспламеняющиеся газы). [14]
Считается, что восстановление аланов происходит через промежуточный координационный комплекс , в котором алюминий присоединяется к частично восстановленной функциональной группе и высвобождается, когда реакция подвергается протонному тушению . Если подложка также фторирована , промежуточное соединение может вместо этого взорваться при воздействии горячей точки выше 60 ° C. [15]
Гидриды алюминия и различные их комплексы известны давно. [16] Его первый синтез был опубликован в 1947 году, а патент на синтез был присвоен в 1999 году. [17] [18] Гидрид алюминия получают путем обработки алюмогидрида лития трихлоридом алюминия . [19] Процедура сложная: необходимо уделить внимание удалению хлорида лития .
Эфирный раствор алан требует немедленного использования, поскольку полимерный материал быстро выпадает в осадок в виде твердого вещества. Известно, что растворы гидрида алюминия разлагаются через 3 дня. Гидрид алюминия более реакционноспособен, чем Li[AlH 4 ] . [6]
Существует несколько других методов получения гидрида алюминия:
Несколько групп показали, что аланы можно получать электрохимически . [20] [21] [22] [23] [24] Запатентованы различные электрохимические методы производства аланов. [25] [26] Электрохимическое получение алан позволяет избежать примесей хлоридов. Обсуждаются два возможных механизма образования алан в электрохимической ячейке Класена, содержащей ТГФ в качестве растворителя, алюмогидрид натрия в качестве электролита, алюминиевый анод и железную (Fe) проволоку, погруженную в ртуть (Hg) в качестве катода. Натрий образует амальгаму с ртутным катодом, предотвращая побочные реакции, а водород, образующийся в первой реакции, можно улавливать и подвергать обратной реакции с амальгамой натрия и ртути с образованием гидрида натрия. Система Clasen не приводит к потере исходного материала. Для нерастворимых анодов протекает реакция 1, а для растворимых анодов ожидается анодное растворение по реакции 2:
В реакции 2 алюминиевый анод расходуется, что ограничивает производство гидрида алюминия для данной электрохимической ячейки.
Показана кристаллизация и восстановление гидрида алюминия из аланов, генерируемых электрохимическим путем. [23] [24]
α- AlH 3 можно получить гидрированием металлического алюминия при давлении 10 ГПа и 600 °C (1112 °F). Реакция между сжиженным водородом приводит к образованию α- AlH 3 , который можно восстановить в условиях окружающей среды. [27]
AlH 3 легко образует аддукты с сильными основаниями Льюиса . Например, с триметиламином образуются комплексы как 1:1, так и 1:2 . Комплекс 1:1 в газовой фазе тетраэдрический [28] , но в твердой фазе он димерный с мостиковыми водородными центрами (N(CH 3 ) 3 Al(μ-H)) 2 . [29] Комплекс 1:2 принимает тригонально-бипирамидальную структуру . [28] Некоторые аддукты (например, диметилэтиламин алан, (CH 3 CH 2 )(CH 3 ) 2 N·AlH 3 ) термически разлагаются с образованием металлического алюминия и могут найти применение в приложениях MOCVD . [30]
Его комплекс с диэтиловым эфиром образуется согласно следующей стехиометрии:
Реакция с гидридом лития в эфире дает алюмогидрид лития :
В органической химии гидрид алюминия в основном используется для восстановления функциональных групп. [31] Во многих отношениях реакционная способность гидрида алюминия аналогична реакционной способности алюмогидрида лития . Гидрид алюминия восстанавливает альдегиды , кетоны , карбоновые кислоты , ангидриды , хлорангидриды , сложные эфиры и лактоны до соответствующих спиртов . Амиды , нитрилы и оксимы восстанавливаются до соответствующих аминов .
По селективности функциональных групп алан отличается от других гидридных реагентов. Например, при следующем восстановлении циклогексанона алюмогидрид лития дает соотношение транс:цис 1,9:1, тогда как гидрид алюминия дает соотношение транс:цис 7,3:1. [32]

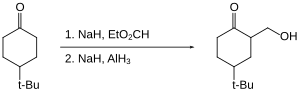
Алан обеспечивает гидроксиметилирование некоторых кетонов (то есть замену CH на C-CH 2 OH в альфа-положении ). [33] Сам кетон не восстанавливается, поскольку он «защищен» как его енолят.
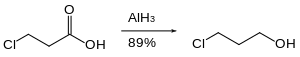
Галогенорганические соединения восстанавливаются гидридом алюминия медленно или не восстанавливаются вообще. Следовательно, реакционноспособные функциональные группы, такие как карбоновые кислоты, могут быть восстановлены в присутствии галогенидов. [34]
Нитрогруппы не восстанавливаются гидридом алюминия. Аналогичным образом, гидрид алюминия может восстанавливать сложный эфир в присутствии нитрогрупп. [35]

Гидрид алюминия можно использовать для восстановления ацеталей до полузащищенных диолов. [36]

Гидрид алюминия также можно использовать в реакции раскрытия эпоксидного кольца, как показано ниже. [37]

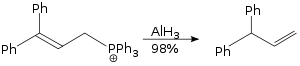
Реакция аллильной перегруппировки, проводимая с использованием гидрида алюминия, является реакцией S N 2 и не требует стерических требований. [38]
Гидрид алюминия восстанавливает углекислый газ до метана при нагревании: [ нужна ссылка ]
Подобно гидроборированию , гидрид алюминия в присутствии тетрахлорида титана может присоединяться по множественным связям . [39] [40] Когда рассматриваемая кратная связь представляет собой пропаргиловые спирты , в результате получаются соединения алкенилалюминия . [41]

В пассивированной форме алан является активным кандидатом для хранения водорода и может использоваться для эффективного производства электроэнергии с помощью топливных элементов, включая топливные элементы и электромобили, а также других легких энергетических устройств. [ нужна ссылка ] AlH 3 содержит до 10,1% водорода по весу (при плотности 1,48 грамма на миллилитр), [2] или в два раза превышает плотность водорода в жидком H 2 . [ нужна цитата ] По состоянию на 2006 год AlH 3 описывался как кандидат, для которого «потребуются дальнейшие исследования для разработки эффективного и экономичного процесса регенерации [его] из отработанного порошка Al». [2] [ нужно обновить ]
Аллан также является потенциальной добавкой к ракетному топливу , взрывчатым и пиротехническим составам. [ нужна цитата ] В непассивированной форме алан также является многообещающей добавкой к ракетному топливу , способной обеспечить повышение импульсной эффективности до 10%. [42]
{{cite journal}}: CS1 maint: периодическое издание без названия ( ссылка )