Круговой дихроизм ( CD ) — это дихроизм , включающий циркулярно поляризованный свет, т. е. дифференциальное поглощение левого и правого света . [1] [2] Свет с левой круговой (LHC) и правой круговой (RHC) поляризацией представляет собой два возможных состояния спинового углового момента для фотона, поэтому круговой дихроизм также называют дихроизмом для спинового углового момента. [3] Это явление было обнаружено Жаном-Батистом Био , Огюстеном Френелем и Эме Коттоном в первой половине 19 века. [4] Круговой дихроизм и круговое двойное лучепреломление являются проявлениями оптической активности . Он проявляется в полосах поглощения оптически активных хиральных молекул . КД- спектроскопия имеет широкий спектр применений во многих различных областях. В частности, УФ- КД используется для исследования вторичной структуры белков. [5] УФ/Вид КД используется для исследования переходов с переносом заряда . [6] КД ближнего инфракрасного диапазона используется для исследования геометрической и электронной структуры путем исследования d → d -переходов металлов . [2] Колебательный круговой дихроизм , в котором используется свет инфракрасной области энергии, используется для структурных исследований небольших органических молекул, а в последнее время белков и ДНК. [5]
Электромагнитное излучение состоит из электрического и магнитного полей, которые колеблются перпендикулярно друг другу и направлению распространения, [7] поперечная волна . В то время как линейно поляризованный свет возникает, когда вектор электрического поля колеблется только в одной плоскости, свет с круговой поляризацией возникает, когда направление вектора электрического поля вращается вокруг направления его распространения, в то время как вектор сохраняет постоянную величину. В одной точке пространства вектор круговой поляризации очерчивает круг за один период частоты волны, отсюда и название. На двух диаграммах ниже показаны векторы электрического поля линейно и циркулярно поляризованного света в один момент времени для ряда положений; график электрического вектора с круговой поляризацией образует спираль вдоль направления распространения . Для левоциркулярно поляризованного света (ЛЦП) при распространении к наблюдателю электрический вектор вращается против часовой стрелки . [2] Для света с правой круговой поляризацией (RCP) электрический вектор вращается по часовой стрелке.
Когда свет с круговой поляризацией проходит через поглощающую оптически активную среду, скорости между правой и левой поляризациями различаются ( ), а также их длина волны ( ) и степень их поглощения ( ). Отличие заключается в круговом дихроизме . [5] Электрическое поле светового луча вызывает линейное смещение заряда при взаимодействии с молекулой ( электрический диполь ), тогда как его магнитное поле вызывает циркуляцию заряда ( магнитный диполь ). Эти два движения в сочетании вызывают возбуждение электрона по спирали, которое включает в себя перемещение и вращение и связанные с ними операторы . Экспериментально установленная зависимость между вращательной силой образца и
Вращательная сила также была определена теоретически.
Из этих двух уравнений мы видим, что для того, чтобы иметь ненулевое значение , операторы электрического и магнитного дипольного момента ( и ) должны преобразоваться как одно и то же неприводимое представление . и являются единственными точечными группами , где это может происходить, делая активными только хиральные молекулы CD.
Проще говоря, поскольку свет с круговой поляризацией сам по себе является «хиральным», он по-разному взаимодействует с хиральными молекулами . То есть два типа света с круговой поляризацией поглощаются в разной степени. В эксперименте CD одинаковое количество левого и правого циркулярно поляризованного света выбранной длины волны поочередно излучается в (хиральный) образец. Одна из двух поляризаций поглощается больше, чем другая, и эта зависящая от длины волны разница поглощения измеряется, что дает спектр КД образца. Благодаря взаимодействию с молекулой вектор электрического поля света после прохождения через образец прослеживает эллиптическую траекторию.
Важно, что хиральность молекулы может быть конформационной, а не структурной. То есть, например, белковая молекула со спиральной вторичной структурой может иметь КД, меняющийся при изменении конформации.
По определению,
где (Дельта-поглощение) — это разница между поглощением света с левой круговой поляризацией (LCP) и правой круговой поляризацией (RCP) (это то, что обычно измеряется). является функцией длины волны , поэтому для того, чтобы измерение имело смысл, должна быть известна длина волны, на которой оно было выполнено.
Это также можно выразить, применив закон Бера , как:
где
Затем
– молярный круговой дихроизм. Это внутреннее свойство обычно подразумевается под круговым дихроизмом вещества. Поскольку это функция длины волны, значение молярного кругового дихроизма ( ) должно указывать длину волны, при которой оно действительно.
Во многих практических применениях кругового дихроизма (КД), как обсуждается ниже, измеренная КД является не просто внутренним свойством молекулы, а скорее зависит от молекулярной конформации. В таком случае CD также может быть функцией температуры, концентрации и химической среды, включая растворители. В этом случае сообщаемое значение CD должно также указывать эти другие важные факторы, чтобы быть значимым.
В упорядоченных структурах, лишенных двойной вращательной симметрии, оптическая активность, [8] [9] , включая дифференциальное пропускание [10] (и отражение [11] ) волн циркулярной поляризации, также зависит от направления распространения через материал. В этом случае так называемая внешняя 3d-хиральность связана с взаимной ориентацией светового луча и структуры.
Хотя обычно измеряется, по историческим причинам большинство измерений приводятся в градусах эллиптичности. Молярная эллиптичность представляет собой круговой дихроизм с поправкой на концентрацию. Молярный круговой дихроизм и молярная эллиптичность легко преобразуются между собой уравнением:
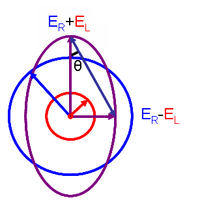
Это соотношение получается путем определения эллиптичности поляризации как:
где
При равенстве (когда нет разницы в поглощении света с право- и левополяризованным светом) оно равно 0° и свет линейно поляризован . Когда любой или равен нулю (когда имеется полное поглощение света с круговой поляризацией в одном направлении), угол составляет 45 °, и свет поляризован по кругу .
Как правило, эффект кругового дихроизма невелик, поэтому он мал и может быть аппроксимирован как в радианах . Поскольку интенсивность или освещенность света пропорциональна квадрату вектора электрического поля, эллиптичность принимает вид:
Затем, заменив I, используя закон Бера в форме натурального логарифма :
Эллиптичность теперь можно записать как:
Поскольку , это выражение можно аппроксимировать, разложив экспоненты в ряд Тейлора до первого порядка, а затем отбросив члены по сравнению с единицей и переведя радианы в градусы:
Линейная зависимость концентрации растворенного вещества и длины пути устраняется путем определения молярной эллиптичности как:
Тогда, объединив два последних выражения с законом Бера , молярная эллиптичность становится:
Исторически единицами молярной эллиптичности являются (град·см 2 /дмоль). Для расчета молярной эллиптичности необходимо знать концентрацию образца (г/л), длину пути клетки (см) и молекулярную массу (г/моль).
Если образец представляет собой белок, вместо молекулярной массы часто используется средняя масса остатка (средняя молекулярная масса содержащихся в нем аминокислотных остатков), при этом белок рассматривается как раствор аминокислот. Использование средней эллиптичности остатков облегчает сравнение CD белков с разной молекулярной массой; использование этого нормализованного CD важно при изучении структуры белка.
Методы оценки вторичной структуры полимеров, в частности белков и полипептидов, часто требуют, чтобы измеренный спектр молярной эллиптичности был преобразован в нормализованное значение, в частности, значение, не зависящее от длины полимера. Для этой цели используется средняя эллиптичность остатка; это просто измеренная молярная эллиптичность молекулы, деленная на количество мономерных единиц (остатков) в молекуле.
В общем случае это явление будет проявляться в полосах поглощения любой оптически активной молекулы. Как следствие, биологические молекулы проявляют круговой дихроизм из-за их правовращающих и левовращающих компонентов. Еще более важно то, что вторичная структура также придает отчетливый CD соответствующим молекулам. Следовательно, альфа-спираль белков и двойная спираль нуклеиновых кислот имеют спектральные характеристики CD, представляющие их структуры. Способность CD давать репрезентативную структурную подпись делает его мощным инструментом в современной биохимии, приложения которого можно найти практически во всех областях исследований.
CD тесно связан с методом оптической вращательной дисперсии (ORD) и обычно считается более продвинутым. CD измеряется в полосах поглощения интересующей молекулы или вблизи них, тогда как ORD может быть измерен вдали от этих полос. Преимущество компакт-диска очевидно при анализе данных. Структурные элементы различаются более четко, поскольку их записанные полосы не перекрываются сильно на определенных длинах волн, как это происходит в ORD. В принципе, эти два спектральных измерения могут быть взаимно преобразованы посредством интегрального преобразования ( соотношение Крамерса-Кронига ), если все поглощения включены в измерения.
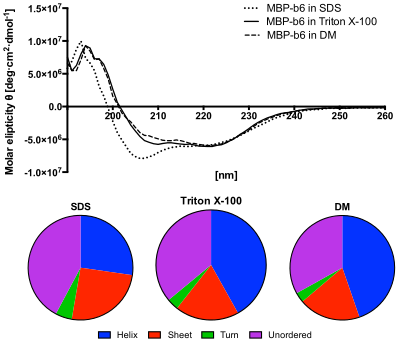
Спектр КД белков в дальнем УФ ( ультрафиолетовом ) диапазоне может выявить важные характеристики их вторичной структуры . Спектры КД можно легко использовать для оценки доли молекулы, находящейся в конформации альфа-спирали , конформации бета-листа , конформации бета-витка или какой-либо другой конформации (например, случайного клубка ). [13] [14] [15] [16] Эти дробные распределения накладывают важные ограничения на возможные вторичные конформации, в которых может находиться белок. CD, как правило, не может сказать, где обнаруженные альфа-спирали расположены внутри молекулы или даже полностью предсказать, сколько их. Несмотря на это, CD является ценным инструментом, особенно для демонстрации изменений в телосложении. Его можно, например, использовать для изучения того, как вторичная структура молекулы меняется в зависимости от температуры или концентрации денатурирующих агентов, например хлорида гуанидиния или мочевины . Таким образом, он может раскрыть важную термодинамическую информацию о молекуле (например, энтальпию и свободную энергию денатурации Гиббса), которую иначе невозможно легко получить. Любой, кто попытается изучить белок, найдет CD ценным инструментом для проверки того, что белок находится в своей нативной конформации, прежде чем проводить с ним обширные и/или дорогостоящие эксперименты. Кроме того, существует ряд других применений спектроскопии КД в химии белков, не связанных с оценкой доли альфа-спирали. Кроме того, спектроскопия КД использовалась в исследованиях бионеорганических интерфейсов. В частности, его использовали для анализа различий во вторичной структуре сконструированного белка до и после титрования реагентом. [17]
Спектр КД в ближней УФ-области (>250 нм) белков дает информацию о третичной структуре . Сигналы, полученные в области 250–300 нм, обусловлены поглощением, дипольной ориентацией и природой окружающего окружения аминокислот фенилаланина, тирозина, цистеина (или дисульфидных мостиков SS ) и триптофана . В отличие от КД в дальнем УФ-диапазоне, спектр КД в ближнем УФ-диапазоне нельзя отнести к какой-либо конкретной трехмерной структуре. Скорее, спектры КД в ближнем УФ-диапазоне предоставляют структурную информацию о природе простетических групп в белках, например, гем-групп в гемоглобине и цитохроме с .
Видимая КД-спектроскопия является очень мощным методом изучения взаимодействий металл-белок и может разрешать отдельные электронные dd-переходы как отдельные полосы. Спектры КД в видимой области света возникают только тогда, когда ион металла находится в хиральном окружении, поэтому свободные ионы металлов в растворе не обнаруживаются. Преимущество этого метода состоит в том, что он позволяет наблюдать только металл, связанный с белком, поэтому легко получить зависимость от pH и стехиометрию. Оптическая активность в комплексах ионов переходных металлов объясняется конфигурационными, конформационными и вицинальными эффектами. Клевпатинонд и Вайлс (2007) разработали набор эмпирических правил для прогнозирования появления видимых спектров КД для плоско-квадратных комплексов Cu 2+ и Ni 2+ , включающих гистидин и координацию основной цепи.
КД дает менее конкретную структурную информацию, чем, например, рентгеновская кристаллография и ЯМР-спектроскопия белков , которые оба дают данные об атомном разрешении. Однако КД-спектроскопия — быстрый метод, не требующий больших количеств белков или обширной обработки данных. Таким образом, CD можно использовать для исследования большого количества условий растворителя , варьирующейся температуры , pH , солености и присутствия различных кофакторов.
КД- спектроскопия обычно используется для изучения белков в растворе и, таким образом, дополняет методы исследования твердого состояния. Это также является ограничением, поскольку многие белки встроены в мембраны в нативном состоянии, а растворы, содержащие мембранные структуры, часто сильно рассеиваются. CD иногда измеряют в тонких пленках.
Спектроскопия КД также проводилась с использованием полупроводниковых материалов, таких как TiO 2 , для получения сильных сигналов в УФ-диапазоне длин волн, где часто происходят электронные переходы биомолекул. [18]
КД также изучался в углеводах , но с ограниченным успехом из-за экспериментальных трудностей, связанных с измерением спектров КД в вакуумной ультрафиолетовой (ВУФ) области спектра (100–200 нм), где лежат соответствующие полосы КД незамещенных углеводов. . Замещенные углеводы с полосами выше ВУФ-области были успешно измерены.
Измерение CD также осложняется тем фактом, что типичные водные буферные системы часто поглощают в диапазоне, в котором структурные особенности демонстрируют дифференциальное поглощение циркулярно поляризованного света. Фосфатный , сульфатный , карбонатный и ацетатный буферы обычно несовместимы с ЦД, если они не сильно разбавлены, например, в диапазоне 10–50 мМ. Буферную систему TRIS следует полностью избегать при выполнении CD в дальнем УФ-диапазоне. Соединения бората и ония часто используются для установления подходящего диапазона pH для экспериментов по КД. Некоторые экспериментаторы заменили ион хлорида фторидом, поскольку фторид меньше поглощает в дальнем УФ-диапазоне, а некоторые работали в чистой воде. Другой, почти универсальный метод заключается в минимизации поглощения растворителя за счет использования ячеек с более короткой длиной пути при работе в дальнем УФ-диапазоне, длина пути 0,1 мм не является редкостью в этой работе.
Помимо измерений в водных системах, КД, особенно в дальнем УФ-диапазоне, можно измерять в органических растворителях, например, этаноле, метаноле, трифторэтаноле (ТФЭ). Последний имеет то преимущество, что индуцирует структурообразование белков, индуцируя бета-листы в некоторых и альфа-спирали в других, чего они не проявляют в нормальных водных условиях. Однако наиболее распространенные органические растворители, такие как ацетонитрил , ТГФ , хлороформ , дихлорметан , несовместимы с КД в дальнем УФ-диапазоне.
Может быть интересно отметить, что спектры CD белка, используемые при оценке вторичной структуры, связаны с орбитальным поглощением от π до π* амидных связей , связывающих аминокислоты. Эти полосы поглощения частично лежат в так называемом вакуумном ультрафиолете (длины волн менее 200 нм). Интересующая область длин волн фактически недоступна в воздухе из-за сильного поглощения света кислородом на этих длинах волн. На практике эти спектры измеряются не в вакууме, а в бескислородном приборе (заполненном чистым газообразным азотом ).
После устранения кислорода, возможно, вторым наиболее важным техническим фактором при работе на длинах волн ниже 200 нм станет проектирование остальной части оптической системы с низкими потерями в этой области. Важным в этом отношении является использование алюминизированных зеркал , покрытия которых оптимизированы для обеспечения низких потерь в этой области спектра.
Обычным источником света в этих приборах является ксеноновая лампа высокого давления с короткой дугой . Обычные ксеноновые дуговые лампы непригодны для использования в условиях слабого ультрафиолета. Вместо этого необходимо использовать специально сконструированные лампы с колбой из синтетического плавленого кварца высокой чистоты.
Свет синхротронных источников имеет гораздо более высокий поток на коротких длинах волн и использовался для записи компакт-диска с длиной волны до 160 нм. В 2010 году спектрофотометр КД на установке накопителя электронов ISA в Орхусском университете в Дании использовался для регистрации спектров КД твердого тела до 120 нм. [19] На квантовомеханическом уровне плотность признаков кругового дихроизма и оптического вращения идентична. Оптическая вращающаяся дисперсия и круговой дихроизм имеют один и тот же квантовый информационный контент.