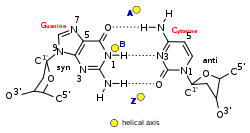
Z-ДНК — одна из многих возможных двойных спиральных структур ДНК . Это левосторонняя двойная спиральная структура, в которой спираль зигзагообразно закручивается влево, а не вправо, как в более распространенной форме B-ДНК . Z-ДНК считается одной из трех биологически активных двухспиральных структур наряду с A-ДНК и B-ДНК .
Леворукая ДНК была впервые предложена Робертом Уэллсом и его коллегами как структура повторяющегося полимера инозин - цитозин . [1] Они наблюдали «обратный» спектр кругового дихроизма для таких ДНК и неправильно интерпретировали это как означающее, что нити закручиваются друг вокруг друга левосторонним образом. На взаимосвязь между Z-ДНК и более известной B-ДНК указала работа Пола и Джовина [2] , которые показали, что ультрафиолетовый циркулярный дихроизм поли(dG-dC) почти инвертируется в 4 М растворе хлорида натрия и что структура поли d(I–C)·poly d(I–C) на самом деле представляет собой правостороннюю конформацию D-ДНК. Подозрение, что это было результатом превращения B-ДНК в Z-ДНК, было подтверждено исследованием спектров комбинационного рассеяния этих растворов и кристаллов Z-ДНК. [3] Впоследствии была опубликована кристаллическая структура «Z-ДНК», которая оказалась первой монокристаллической рентгеновской структурой фрагмента ДНК (самомлементарного ДНК-гексамера d(CG) 3 ). Она была решена как левая двойная спираль с двумя антипараллельными цепями, которые удерживались вместе парами оснований Уотсона-Крика (см. Рентгеновскую кристаллографию ). Она была решена Эндрю Х. Дж. Вангом , Александром Ричем и его коллегами в 1979 году в Массачусетском технологическом институте . [4] Кристаллизация соединения B-Z-ДНК в 2005 году [5] позволила лучше понять потенциальную роль Z-ДНК, которую играет в клетках. Всякий раз, когда формируется сегмент Z-ДНК, на его двух концах должны быть соединения B-Z, соединяющие его с B-формой ДНК, обнаруженной в остальной части генома .
В 2007 году РНК- версия Z-ДНК, Z-РНК , была описана как трансформированная версия двойной спирали А-РНК в левостороннюю спираль. [6] Однако переход от А-РНК к Z-РНК был описан уже в 1984 году. [7]
Z-ДНК сильно отличается от правосторонних форм. Фактически, Z-ДНК часто сравнивают с B-ДНК, чтобы проиллюстрировать основные различия. Спираль Z-ДНК левая и имеет структуру, повторяющую каждую вторую пару оснований. Большие и малые бороздки, в отличие от А- и В-ДНК, мало отличаются по ширине. Формирование этой структуры в целом неблагоприятно, хотя определенные условия могут этому способствовать; такие как чередующаяся пурин - пиримидиновая последовательность (особенно поли(dGC) 2 ), отрицательная сверхспирализация ДНК или высокое содержание соли и некоторые катионы (все при физиологической температуре, 37 ° C и pH 7,3–7,4). Z-ДНК может образовывать соединение с B-ДНК (называемое «соединительной коробкой B-Z») в структуре, которая включает экструзию пары оснований. [8] Конформацию Z-ДНК трудно изучать, поскольку она не существует как стабильная особенность двойной спирали. Напротив, это временная структура, которая иногда возникает в результате биологической активности, а затем быстро исчезает. [9]
Можно предсказать вероятность того, что последовательность ДНК образует структуру Z-ДНК. Алгоритм прогнозирования склонности ДНК к переходу из B-формы в Z-форму, ZHunt , был написан П. Шинг Хо в 1984 году в Массачусетском технологическом институте . [10] Этот алгоритм позже был разработан Трейси Кэмп , П. Кристофом Чампом, Сандором Морисом и Джеффри М. Варгасоном для полногеномного картирования Z-ДНК (с Хо в качестве главного исследователя). [11]
С момента открытия и кристаллизации Z-ДНК в 1979 году эта конфигурация поставила ученых в тупик относительно пути и механизма перехода от конфигурации B-ДНК к конфигурации Z-ДНК. [12] Конформационное изменение структуры B-ДНК на структуру Z-ДНК было неизвестно на атомном уровне, но в 2010 году компьютерное моделирование, проведенное Lee et al. смогли вычислительно определить, что ступенчатое распространение перехода B-Z обеспечит более низкий энергетический барьер , чем ранее предполагаемый согласованный механизм. [13] Поскольку это было доказано вычислительно, этот путь все равно необходимо будет проверить экспериментально в лаборатории для дальнейшего подтверждения и достоверности, в чем Lee et al. В своей журнальной статье, в частности, говорится: «Текущий [вычислительный] результат может быть проверен в будущем с помощью экспериментов с одиночной молекулой FRET (smFRET)». [13] В 2018 году путь от B-ДНК к Z-ДНК был экспериментально доказан с помощью анализов smFRET. [14] Это было выполнено путем измерения значений интенсивности между донорными и акцепторными флуоресцентными красителями, также известными как флуорофоры , по отношению друг к другу, когда они обмениваются электронами, будучи прикрепленными к молекуле ДНК. [15] [16] Расстояния между флуорофорами можно использовать для количественного расчета изменений близости красителей и конформационных изменений в ДНК. Высокоаффинный связывающий белок Z-ДНК , hZαADAR1, [17] использовался в различных концентрациях для индукции трансформации B-ДНК в Z-ДНК. [14] Анализ smFRET выявил переходное состояние B*, которое сформировалось в результате связывания hZαADAR1, накопленного на структуре B-ДНК, и стабилизировало ее. [14] Этот шаг делается для того, чтобы избежать высокой энергии соединения, при которой структура B-ДНК может претерпевать конформационные изменения в структуре Z-ДНК без существенного разрушительного изменения энергии. Этот результат совпадает с результатами вычислений Lee et al. доказывая, что этот механизм является поэтапным и его цель состоит в том, что он обеспечивает более низкий энергетический барьер для конформационного изменения от конфигурации B-ДНК к конфигурации Z-ДНК. [13] Вопреки предыдущему представлению, связывающие белки фактически не стабилизируют конформацию Z-ДНК после ее формирования, а вместо этого фактически способствуют образованию Z-ДНК непосредственно из конформации B*, которая образуется Структура B-ДНК связана белками с высоким сродством. [14]
Биологическая роль Z-ДНК в регуляции ответов интерферона I типа была подтверждена в исследованиях трех хорошо изученных редких менделевских заболеваний: симметричного наследственного дисхроматоза (OMIM: 127400), синдрома Айкарди-Гутьера (OMIM: 615010) и двустороннего полосатого тела. Некроз/Дистония. Семьи с гаплоидным транскриптомом ADAR позволили сопоставить варианты Zα непосредственно с заболеванием, показав, что генетическая информация кодируется в ДНК как по форме, так и последовательности. [18] Роль в регуляции реакции интерферона I типа при раке также подтверждается данными о том, что выживание 40% опухолей зависело от фермента ADAR. [19]
В предыдущих исследованиях Z-ДНК была связана как с болезнью Альцгеймера , так и с системной красной волчанкой . Чтобы продемонстрировать это, было проведено исследование ДНК, обнаруженной в гиппокампе головного мозга нормального человека, умеренно пораженного болезнью Альцгеймера и тяжело пораженного болезнью Альцгеймера. Благодаря использованию кругового дихроизма это исследование показало наличие Z-ДНК в ДНК тяжело пострадавших. [20] В этом исследовании также было обнаружено, что основные части умеренно пораженной ДНК находились в промежуточной конформации BZ. Это важно, поскольку на основе этих результатов был сделан вывод, что переход от B-ДНК к Z-ДНК зависит от прогрессирования болезни Альцгеймера. [20] Кроме того, Z-ДНК связана с системной красной волчанкой (СКВ) благодаря наличию естественных антител. Значительные количества антител против Z-ДНК были обнаружены у больных СКВ и отсутствовали при других ревматических заболеваниях. [21] Существует два типа этих антител. С помощью радиоиммуноанализа было обнаружено, что один взаимодействует с основаниями, экспонированными на поверхности Z-ДНК и денатурированной ДНК, а другой взаимодействует исключительно с зигзагообразным остовом только Z-ДНК. Подобно тому, что наблюдается при болезни Альцгеймера, антитела варьируются в зависимости от стадии заболевания: максимальное количество антител наблюдается на наиболее активных стадиях СКВ.
Обычно считается, что Z-ДНК обеспечивает облегчение торсионного напряжения во время транскрипции , и это связано с отрицательной суперспирализацией . [5] [22] Однако, хотя сверхспирализация связана как с транскрипцией, так и с репликацией ДНК, образование Z-ДНК в первую очередь связано со скоростью транскрипции . [23]
Исследование 22-й хромосомы человека показало корреляцию между областями формирования Z-ДНК и областями промотора ядерного фактора I. Это предполагает, что транскрипция в некоторых генах человека может регулироваться образованием Z-ДНК и активацией ядерного фактора I. [11]
Было показано, что последовательности Z-ДНК, расположенные выше промоторных областей, стимулируют транскрипцию. Наибольшее увеличение активности наблюдается, когда последовательность Z-ДНК располагается на три витка спирали после последовательности промотора . Кроме того, при использовании метода перекрестного сшивания микрококковой нуклеазы [24] Z-ДНК вряд ли образует нуклеосомы , которые часто располагаются до и/или после последовательности, образующей Z-ДНК. Предполагается, что из-за этого свойства Z-ДНК кодирует границу позиционирования нуклеосом. Поскольку размещение нуклеосом влияет на связывание факторов транскрипции , считается, что Z-ДНК регулирует скорость транскрипции. [24]
Было показано, что Z-ДНК, образующаяся посредством активной транскрипции, возникшая на основе пути РНК-полимеразы посредством отрицательной суперспирализации, увеличивает генетическую нестабильность, создавая склонность к мутагенезу вблизи промоторов. [25] Исследование Escherichia coli показало, что делеции генов спонтанно происходят в плазмидных областях, содержащих последовательности, образующие Z-ДНК. [26] Было обнаружено, что в клетках млекопитающих присутствие таких последовательностей приводит к делециям крупных геномных фрагментов из-за хромосомных двухцепочечных разрывов . Обе эти генетические модификации связаны с транслокациями генов, обнаруженными при таких видах рака, как лейкемия и лимфома , поскольку области разрыва в опухолевых клетках нанесены вокруг последовательностей, образующих Z-ДНК. [25] Однако меньшие делеции в бактериальных плазмидах были связаны с проскальзыванием репликации , тогда как более крупные делеции, связанные с клетками млекопитающих, вызваны негомологичной репарацией соединения концов, которая, как известно, подвержена ошибкам. [25] [26]
Токсическое действие бромистого этидия (EtBr) на трипаносомы обусловлено сдвигом их кинетопластидной ДНК в Z-форму. Сдвиг вызван интеркаляцией EtBr и последующим разрыхлением структуры ДНК, что приводит к раскручиванию ДНК, переходу в Z-форму и ингибированию репликации ДНК. [27]
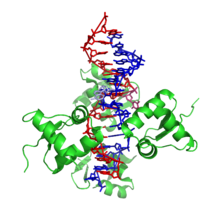
Первый домен, связывающий Z-ДНК с высоким сродством, был обнаружен в ADAR1 с использованием подхода, разработанного Аланом Гербертом. [28] [29] Кристаллографические и ЯМР исследования подтвердили биохимические данные о том, что этот домен связывает Z-ДНК неспецифичным для последовательности образом. [30] [31] [32] Родственные домены были идентифицированы в ряде других белков посредством гомологии последовательностей . [29] Идентификация домена Zα послужила инструментом для других кристаллографических исследований, которые привели к характеристике Z-РНК и соединения B-Z. Биологические исследования показали, что Z-ДНК-связывающий домен ADAR1 может локализовать этот фермент, который модифицирует последовательность вновь образованной РНК в местах активной транскрипции. [33] [34] Роль Zα, Z-ДНК и Z-РНК в защите генома от вторжения ретро-элементов Alu у людей превратилась в механизм регуляции врожденных иммунных ответов на дцРНК. Мутации в Zα являются причиной интерферопатий человека, таких как синдром Менделя Айкарди-Гутьера. [35] [18] Кроме того, показано, что домены Zα локализуются в стрессовых гранулах из-за их врожденной способности связывать нуклеиновую кислоту. Более того, разные домены Zα по-разному связываются с Z-конформацией нуклеиновой кислоты, обеспечивая важные возможности для специфического нацеливания при разработке лекарств.
Поскольку Z-ДНК была исследована более тщательно, было обнаружено, что структура Z-ДНК может связываться с белками, связывающими Z-ДНК, посредством лондонной дисперсии и водородных связей . [36] Одним из примеров белка, связывающего Z-ДНК, является белок E3L коровьей оспы , который является продуктом гена E3L и имитирует белок млекопитающих, который связывает Z-ДНК. [37] [38] Белок E3L не только имеет сродство к Z-ДНК, но также было обнаружено, что он играет роль в уровне тяжести вирулентности у мышей, вызванной вирусом коровьей оспы, разновидностью поксвируса . Двумя критическими компонентами белка E3L, определяющими вирулентность, являются N-конец и C-конец . N-конец состоит из последовательности, аналогичной последовательности домена Zα, также называемой доменом z-альфа аденозиндезаминазы , тогда как C-конец состоит из двухцепочечного мотива связывания РНК. [37] Благодаря исследованиям, проведенным Kim, Y. et al. в Массачусетском технологическом институте было показано, что замена N-конца белка E3L на последовательность домена Zα, содержащую 14 связывающих Z-ДНК остатков, аналогичных E3L, практически не влияет на патогенность вируса у мышей. [37] В отличие от этого, Ким Ю. и др. также обнаружили, что удаление всех 83 остатков N-конца E3L приводило к снижению вирулентности. Это подтверждает их утверждение о том, что N-конец, содержащий остатки связывания Z-ДНК, необходим для вирулентности. [37] В целом, эти результаты показывают, что сходные остатки связывания Z-ДНК на N-конце белка E3L и домене Zα являются наиболее важными структурными факторами, определяющими вирулентность, вызванную вирусом осповакцины, в то время как аминокислотные остатки, не участвующие в Связывание Z-ДНК практически не оказывает никакого эффекта. Будущее значение этих результатов включает снижение связывания E3L с Z-ДНК в вакцинах, содержащих вирус коровьей оспы, чтобы можно было свести к минимуму негативные реакции на вирус у людей. [37]
Кроме того, Александр Рич и Джин-А Квон обнаружили, что E3L действует как трансактиватор человеческих генов IL-6, NF-AT и p53. Их результаты показывают, что клетки HeLa , содержащие E3L, имели повышенную экспрессию человеческих генов IL-6, NF-AT и p53, а точечные мутации или делеции определенных аминокислотных остатков, связывающих Z-ДНК, снижали эту экспрессию. [36] В частности, было обнаружено, что мутации в Tyr 48 и Pro 63 снижают трансактивацию ранее упомянутых генов в результате потери водородных связей и лондонских дисперсионных сил между E3L и Z-ДНК. [36] В целом, эти результаты показывают, что уменьшение связей и взаимодействий между Z-ДНК и белками, связывающими Z-ДНК, снижает как вирулентность, так и экспрессию генов, тем самым показывая важность наличия связей между Z-ДНК и связывающим белком E3L.